(2006?天河區一模)某化學學習小組的同學為了探究氫氧化鈉溶液與稀鹽酸是否恰好完全反應,做了如下圖所示的實驗:
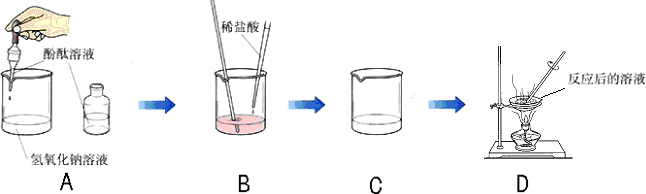
(1)實驗中酚酞溶液的作用是
指示氫氧化鈉與鹽酸何時恰好完全反應;
指示氫氧化鈉與鹽酸何時恰好完全反應;
.
(2)D中溶液蒸發后留下的固體是(寫化學式)
NaCl,
NaCl,
,能說明此結論的實驗現象是
B中的溶液由紅色變成無色.
B中的溶液由紅色變成無色.
.
(3)如果經測定,蒸發得到的固體中含有CaCl
2(其溶液為中性),那么原NaOH溶液(假定鹽酸純凈)中可能混有的雜質是(任寫一種雜質的化學式)
Ca(OH)2(或CaCl2).
Ca(OH)2(或CaCl2).
.
同學們為了嘗試測定上述食鹽(含雜質CaCl
2)的質量分數并提純,做了如下實驗.請根據實驗回答有關問題:
①準確稱取10g固體樣品,溶于適量蒸餾水中,再加入過量的下列某溶液,反應后過濾,得沉淀物1g.加入的某溶液是
C
C
(填編號).
A.NaOH B.K
2CO
3 C.Na
2CO
3 D.AgNO
3 E.HCl(稀)
其反應的化學方程式是
CaCl2+Na2CO3═CaCO3↓+2NaCl
CaCl2+Na2CO3═CaCO3↓+2NaCl
②往濾液中加入過量的稀鹽酸,加入過量稀鹽酸的原因是
將濾液中過量的Na2CO3完全除去,以便蒸發后得到純凈的食鹽
將濾液中過量的Na2CO3完全除去,以便蒸發后得到純凈的食鹽
.
③將加入稀鹽酸后的濾液放在蒸發皿里加熱蒸發.加熱過程中,要用玻璃棒不斷攪拌,其作用是
使液體受熱均勻,防止液滴飛濺
使液體受熱均勻,防止液滴飛濺
.
④計算樣品中NaCl的質量分數為
88.9%
88.9%
.


