
科目: 來源:江蘇省揚州市邵樊片2018屆九年級下學期第一次月考化學試卷 題型:單選題
6.50gZn和一定量氯化亞鐵溶液,充分反應剩余固體質量為6.05g,若將剩余固體加入到足量稀鹽酸中,產生氫氣的質量
A. 0.20g B. 0.22g C. 0.18g D. 0.21g
A 【解析】將鋅放入氯化亞鐵溶液中,鋅和氯化亞鐵溶液反應生成氯化鋅和鐵,而生成的鐵能夠和稀鹽酸反應生成氯化亞鐵,根據鐵元素的守恒可以判斷與氯化亞鐵反應消耗的鋅和鹽酸反應生成的氫氣,與鐵和鹽酸反應生成的氫氣質量相等,所以產生氫氣的質量可以直接根據鋅的質量進行計算。設生成氫氣的質量是x。 Zn+H2SO4=ZnSO4+H2↑ 65 2 6.50g x x=0.20g ...下列四個圖像的變化趨勢,能正確描述對應操作的是
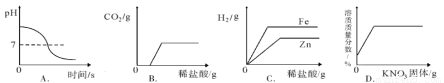
A.向一定量的氫氧化鈉溶液中不斷地滴加水
B.向一定量久置于空氣中的氫氧化鈉固體中不斷地滴加稀鹽酸
C.向等質量的鋅、鐵顆粒中分別滴加足量相同濃度的稀鹽酸
D.向t℃一定量飽和硝酸鉀溶液中不斷加入硝酸鉀固體
查看答案如圖是a、b、c三種物質的溶解度曲線,下列分析不正確的是
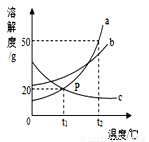
A.t2℃時,三種物質的溶解度是a>b>c
B.t2℃時,將a物質50g(不含結晶水)放入100g水中充分溶解得到a的飽和溶液
C.將t2℃時,三種物質的飽和溶液降溫至t1℃,所得溶液的溶質質量分數關系是b>a=c
D.升溫可將c的飽和溶液變為不飽和溶液
查看答案下列除去雜質的方法中,不正確的是
選項 | 物質(括號內為雜質) | 除去雜質的方法 |
A | NaOH溶液(Na2CO3) | 加入適量的Ca(OH)2溶液、過濾 |
B | CaO(CaCO3) | 加水溶解、過濾 |
C | CO(CO2) | 通過足量的NaOH溶液、干燥 |
D | FeSO4溶液(H2SO4) | 加入足量鐵粉、過濾 |
A. A B. B C. C D. D
查看答案下列說法正確的是
A. 碳酸氫銨與氫氧化鈣混合使用,既可以增加肥效又可以改良酸性土壤
B. 燃燒伴隨著發光、放熱現象,有發光、放熱現象的就是燃燒
C. 喝下汽水后常會打嗝,說明氣體的溶解度一般隨溫度的升高而減小
D. 氨氣能使濕潤的藍色石蕊試紙變紅
查看答案下列對實驗現象的描述中, 正確的是
A. 紅磷在空氣中燃燒產生濃厚的白色煙霧
B. 將紅熱的細鐵絲放在氧氣中,劇烈燃燒,火星四射,生成四氧化三鐵
C. 將氫氧化鈉固體溶于水,溶液溫度升高
D. 向氯化鐵溶液中滴加氫氧化鈉溶液, 生成藍色沉淀
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州市邵樊片2018屆九年級下學期第一次月考化學試卷 題型:填空題
(1)用化學符號填空:
①2個氮氣分子________________ ②銨根離子_______________
③標出五氧化二磷中磷元素的化合價_______ ④侯氏制堿法涉及到的“堿”_____
(2)現有A.干冰 B.生石灰 C.氮氣 D.銅 四種物質,用字母序號填空:
①用做食品保護氣的是______; ②常用來制造電線、電纜的單質____;
③用作人工降雨的是_______; ④可用來做食品干燥劑的是_____。
(3)寫出下列反應的化學方程式
①電解水_____ ②鐵與硫酸銅溶液反應______
③一氧化碳和氧化鐵在高溫下反應_____ ④硫酸銨與氫氧化鈉溶液混合加熱______
2N2 NH4+ Na2CO3 C D A B 2H2O2H2↑+O2↑ Fe+CuSO4=FeSO4+Cu 3CO+Fe2O32Fe+3CO2 (NH3)2SO4+2NaOH=Na2SO4+ 2 NH3↑+2H2O 【解析】(1)解題關鍵是分清化學用語所表達的對象是分子、原子、離子還是化合價,才能在化學符號前或其它位置加上適當的計量數來完整地表達其意義,并能根據物質化學式的書寫規則正確書...6.50gZn和一定量氯化亞鐵溶液,充分反應剩余固體質量為6.05g,若將剩余固體加入到足量稀鹽酸中,產生氫氣的質量
A. 0.20g B. 0.22g C. 0.18g D. 0.21g
查看答案下列四個圖像的變化趨勢,能正確描述對應操作的是

A.向一定量的氫氧化鈉溶液中不斷地滴加水
B.向一定量久置于空氣中的氫氧化鈉固體中不斷地滴加稀鹽酸
C.向等質量的鋅、鐵顆粒中分別滴加足量相同濃度的稀鹽酸
D.向t℃一定量飽和硝酸鉀溶液中不斷加入硝酸鉀固體
查看答案如圖是a、b、c三種物質的溶解度曲線,下列分析不正確的是

A.t2℃時,三種物質的溶解度是a>b>c
B.t2℃時,將a物質50g(不含結晶水)放入100g水中充分溶解得到a的飽和溶液
C.將t2℃時,三種物質的飽和溶液降溫至t1℃,所得溶液的溶質質量分數關系是b>a=c
D.升溫可將c的飽和溶液變為不飽和溶液
查看答案下列除去雜質的方法中,不正確的是
選項 | 物質(括號內為雜質) | 除去雜質的方法 |
A | NaOH溶液(Na2CO3) | 加入適量的Ca(OH)2溶液、過濾 |
B | CaO(CaCO3) | 加水溶解、過濾 |
C | CO(CO2) | 通過足量的NaOH溶液、干燥 |
D | FeSO4溶液(H2SO4) | 加入足量鐵粉、過濾 |
A. A B. B C. C D. D
查看答案下列說法正確的是
A. 碳酸氫銨與氫氧化鈣混合使用,既可以增加肥效又可以改良酸性土壤
B. 燃燒伴隨著發光、放熱現象,有發光、放熱現象的就是燃燒
C. 喝下汽水后常會打嗝,說明氣體的溶解度一般隨溫度的升高而減小
D. 氨氣能使濕潤的藍色石蕊試紙變紅
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州市邵樊片2018屆九年級下學期第一次月考化學試卷 題型:填空題
生活中處處有化學,化學與生活密切相關。
(1)下表為某品牌燕麥片標簽中的一部分。
每100 g含 有營養成分 | 糖類 | 油脂 | 蛋白質 | 維生素C | 鈣 | 鎂 | 鈉 | 鋅 |
7.6 g | 7.8 g | 7.4 g | 18 mg | 201 mg | 18.2 mg | 30.8 mg | 8.1 mg |
①人體所需的六大營養素在上表中未列出的是 ;②表中出現了人體所必需的微量元素,該元素是 ;③檢驗燕麥片中是否含有淀粉需用到試劑是 。
(2)民生熱詞:“舌尖上的安全”。下列做法符合食品安全要求的是
A.用碳酸氫鈉作發酵粉
B.用霉變油菜籽生產食用油
C.用碳酸鋇代替純堿蒸饅頭
D.用工業酒精勾兌飲用白酒
(3)用化學方法鑒別“冰蠶絲”(衣服面料,主要成分為合成纖維)和天然蠶絲: 。
(1)①水。 ② 鋅。 ③ 碘酒(或碘水)(2)A。(3)取樣灼燒,若聞到燒焦羽毛氣味則為天然蠶絲;若聞到特殊氣味,則為冰蠶絲。 【解析】 試題分析∶(1)六大營養素缺水,鋅是人體所需微量元素,淀粉遇碘酒變藍。①水。 ② 鋅。 ③ 碘酒(或碘水)(2)碳酸氫鈉是發酵粉的主要成分,霉變油菜籽,鋇鹽,工業酒精均有毒,故A正確。(3)灼燒是檢驗突然蛋白質的常用方法。 考點∶考查人體所需...(1)用化學符號填空:
①2個氮氣分子________________ ②銨根離子_______________
③標出五氧化二磷中磷元素的化合價_______ ④侯氏制堿法涉及到的“堿”_____
(2)現有A.干冰 B.生石灰 C.氮氣 D.銅 四種物質,用字母序號填空:
①用做食品保護氣的是______; ②常用來制造電線、電纜的單質____;
③用作人工降雨的是_______; ④可用來做食品干燥劑的是_____。
(3)寫出下列反應的化學方程式
①電解水_____ ②鐵與硫酸銅溶液反應______
③一氧化碳和氧化鐵在高溫下反應_____ ④硫酸銨與氫氧化鈉溶液混合加熱______
查看答案6.50gZn和一定量氯化亞鐵溶液,充分反應剩余固體質量為6.05g,若將剩余固體加入到足量稀鹽酸中,產生氫氣的質量
A. 0.20g B. 0.22g C. 0.18g D. 0.21g
查看答案下列四個圖像的變化趨勢,能正確描述對應操作的是

A.向一定量的氫氧化鈉溶液中不斷地滴加水
B.向一定量久置于空氣中的氫氧化鈉固體中不斷地滴加稀鹽酸
C.向等質量的鋅、鐵顆粒中分別滴加足量相同濃度的稀鹽酸
D.向t℃一定量飽和硝酸鉀溶液中不斷加入硝酸鉀固體
查看答案如圖是a、b、c三種物質的溶解度曲線,下列分析不正確的是

A.t2℃時,三種物質的溶解度是a>b>c
B.t2℃時,將a物質50g(不含結晶水)放入100g水中充分溶解得到a的飽和溶液
C.將t2℃時,三種物質的飽和溶液降溫至t1℃,所得溶液的溶質質量分數關系是b>a=c
D.升溫可將c的飽和溶液變為不飽和溶液
查看答案下列除去雜質的方法中,不正確的是
選項 | 物質(括號內為雜質) | 除去雜質的方法 |
A | NaOH溶液(Na2CO3) | 加入適量的Ca(OH)2溶液、過濾 |
B | CaO(CaCO3) | 加水溶解、過濾 |
C | CO(CO2) | 通過足量的NaOH溶液、干燥 |
D | FeSO4溶液(H2SO4) | 加入足量鐵粉、過濾 |
A. A B. B C. C D. D
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州市邵樊片2018屆九年級下學期第一次月考化學試卷 題型:簡答題
化學與我們的生活密切相關。
(1)①香煙煙氣中含有多種有害物質,不吸煙的人能聞到煙味的原因是____________;
②隨手丟棄的煙頭還容易引發火災,原因是(選填以下字母)_____________。
A.提供可燃物 B.提供氧氣 C.使可燃物的溫度達到著火點
(2)銅常用于制作導線,因為其有良好的__________性;
(3)日常生活中,常用__________的方法降低水的硬度;
(4)用洗沽精除去餐具上的油污是因為洗沽精在水中對油污具有______作用;
(5)防毒面具中使用活性炭,這是利用了活性炭的______作用;
(6)用過的鐵鍋保護不當很容易生銹,鐵生銹的實質是鐵與______和_____發生復雜的化學變化。說出一種防止鐵鍋生銹的方法____________________________________。
微粒在不斷運動 C 導電 煮沸 乳化 吸附 氧氣或O2 水或H2O 保持鐵鍋表面潔凈、干燥等 【解析】(1)①根據微粒在不斷運動的解答;②根據燃燒的條件分析解答;(2)根據銅具有導電性解答;(3)根據日常生活中,降低水的硬度的方法解答;(4)根據洗沽精具有乳化作用解答;(5)根據活性炭有吸附性解答;(6)根據鐵生銹的條件及防止鐵生銹的方法解答。(1)①香煙煙氣中含有多種有害物質,不吸煙的人能...生活中處處有化學,化學與生活密切相關。
(1)下表為某品牌燕麥片標簽中的一部分。
每100 g含 有營養成分 | 糖類 | 油脂 | 蛋白質 | 維生素C | 鈣 | 鎂 | 鈉 | 鋅 |
7.6 g | 7.8 g | 7.4 g | 18 mg | 201 mg | 18.2 mg | 30.8 mg | 8.1 mg |
①人體所需的六大營養素在上表中未列出的是 ;②表中出現了人體所必需的微量元素,該元素是 ;③檢驗燕麥片中是否含有淀粉需用到試劑是 。
(2)民生熱詞:“舌尖上的安全”。下列做法符合食品安全要求的是
A.用碳酸氫鈉作發酵粉
B.用霉變油菜籽生產食用油
C.用碳酸鋇代替純堿蒸饅頭
D.用工業酒精勾兌飲用白酒
(3)用化學方法鑒別“冰蠶絲”(衣服面料,主要成分為合成纖維)和天然蠶絲: 。
查看答案(1)用化學符號填空:
①2個氮氣分子________________ ②銨根離子_______________
③標出五氧化二磷中磷元素的化合價_______ ④侯氏制堿法涉及到的“堿”_____
(2)現有A.干冰 B.生石灰 C.氮氣 D.銅 四種物質,用字母序號填空:
①用做食品保護氣的是______; ②常用來制造電線、電纜的單質____;
③用作人工降雨的是_______; ④可用來做食品干燥劑的是_____。
(3)寫出下列反應的化學方程式
①電解水_____ ②鐵與硫酸銅溶液反應______
③一氧化碳和氧化鐵在高溫下反應_____ ④硫酸銨與氫氧化鈉溶液混合加熱______
查看答案6.50gZn和一定量氯化亞鐵溶液,充分反應剩余固體質量為6.05g,若將剩余固體加入到足量稀鹽酸中,產生氫氣的質量
A. 0.20g B. 0.22g C. 0.18g D. 0.21g
查看答案下列四個圖像的變化趨勢,能正確描述對應操作的是

A.向一定量的氫氧化鈉溶液中不斷地滴加水
B.向一定量久置于空氣中的氫氧化鈉固體中不斷地滴加稀鹽酸
C.向等質量的鋅、鐵顆粒中分別滴加足量相同濃度的稀鹽酸
D.向t℃一定量飽和硝酸鉀溶液中不斷加入硝酸鉀固體
查看答案如圖是a、b、c三種物質的溶解度曲線,下列分析不正確的是

A.t2℃時,三種物質的溶解度是a>b>c
B.t2℃時,將a物質50g(不含結晶水)放入100g水中充分溶解得到a的飽和溶液
C.將t2℃時,三種物質的飽和溶液降溫至t1℃,所得溶液的溶質質量分數關系是b>a=c
D.升溫可將c的飽和溶液變為不飽和溶液
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州市邵樊片2018屆九年級下學期第一次月考化學試卷 題型:實驗題
請根據裝置圖回答下列有關問題(K、K1、K2、K3為止水夾):
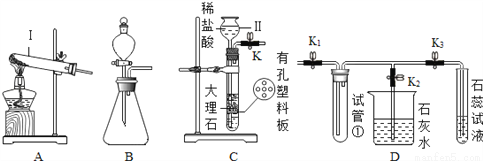
(1)寫出圖中標號儀器的名稱:I_____、II______.
(2)欲用過氧化氫溶液制氧氣,可選用_____發生裝置(填“A”或“B”),請寫出該反應的化學方程式______。
(3)將C和D裝置相連接能制備CO2并驗證CO2的性質.連接C和D裝置,關閉K2,打開K、K1、K3,用試管①收集CO2,此收集方法說明_____。石蕊試液最終呈_____色,使石蕊試液變色的微粒符號是______。
(4)關閉K3,打開K1、K2,燒杯中反應的化學方程式_______。
I試管、 II長頸漏斗 B, 2H2O MnO2 2H2O+O2↑。 密度大于空氣。 紅色, H+。 CO2+Ca(OH)2===CaCO3↓+H2O。 【解析】(1)根據常見儀器解答;(2)根據反應物的狀態和反應條件選擇發生裝置;根據過氧化氫在二氧化錳的催化下分解生成水和氧氣解答;(3)根據收集裝置分析氣體的性質;根據二氧化碳與水反應生成碳酸解答;(4)根據二氧化碳與澄清石灰水反應生成碳酸...化學與我們的生活密切相關。
(1)①香煙煙氣中含有多種有害物質,不吸煙的人能聞到煙味的原因是____________;
②隨手丟棄的煙頭還容易引發火災,原因是(選填以下字母)_____________。
A.提供可燃物 B.提供氧氣 C.使可燃物的溫度達到著火點
(2)銅常用于制作導線,因為其有良好的__________性;
(3)日常生活中,常用__________的方法降低水的硬度;
(4)用洗沽精除去餐具上的油污是因為洗沽精在水中對油污具有______作用;
(5)防毒面具中使用活性炭,這是利用了活性炭的______作用;
(6)用過的鐵鍋保護不當很容易生銹,鐵生銹的實質是鐵與______和_____發生復雜的化學變化。說出一種防止鐵鍋生銹的方法____________________________________。
查看答案生活中處處有化學,化學與生活密切相關。
(1)下表為某品牌燕麥片標簽中的一部分。
每100 g含 有營養成分 | 糖類 | 油脂 | 蛋白質 | 維生素C | 鈣 | 鎂 | 鈉 | 鋅 |
7.6 g | 7.8 g | 7.4 g | 18 mg | 201 mg | 18.2 mg | 30.8 mg | 8.1 mg |
①人體所需的六大營養素在上表中未列出的是 ;②表中出現了人體所必需的微量元素,該元素是 ;③檢驗燕麥片中是否含有淀粉需用到試劑是 。
(2)民生熱詞:“舌尖上的安全”。下列做法符合食品安全要求的是
A.用碳酸氫鈉作發酵粉
B.用霉變油菜籽生產食用油
C.用碳酸鋇代替純堿蒸饅頭
D.用工業酒精勾兌飲用白酒
(3)用化學方法鑒別“冰蠶絲”(衣服面料,主要成分為合成纖維)和天然蠶絲: 。
查看答案(1)用化學符號填空:
①2個氮氣分子________________ ②銨根離子_______________
③標出五氧化二磷中磷元素的化合價_______ ④侯氏制堿法涉及到的“堿”_____
(2)現有A.干冰 B.生石灰 C.氮氣 D.銅 四種物質,用字母序號填空:
①用做食品保護氣的是______; ②常用來制造電線、電纜的單質____;
③用作人工降雨的是_______; ④可用來做食品干燥劑的是_____。
(3)寫出下列反應的化學方程式
①電解水_____ ②鐵與硫酸銅溶液反應______
③一氧化碳和氧化鐵在高溫下反應_____ ④硫酸銨與氫氧化鈉溶液混合加熱______
查看答案6.50gZn和一定量氯化亞鐵溶液,充分反應剩余固體質量為6.05g,若將剩余固體加入到足量稀鹽酸中,產生氫氣的質量
A. 0.20g B. 0.22g C. 0.18g D. 0.21g
查看答案下列四個圖像的變化趨勢,能正確描述對應操作的是

A.向一定量的氫氧化鈉溶液中不斷地滴加水
B.向一定量久置于空氣中的氫氧化鈉固體中不斷地滴加稀鹽酸
C.向等質量的鋅、鐵顆粒中分別滴加足量相同濃度的稀鹽酸
D.向t℃一定量飽和硝酸鉀溶液中不斷加入硝酸鉀固體
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州市邵樊片2018屆九年級下學期第一次月考化學試卷 題型:流程題
自來水廠常用氯氣殺菌消毒,用明礬、氯化鐵等凈化水。以硫鐵礦(主要成分是FeS2)為原料制備氯化鐵晶體(FeCl3·6H2O)的流程如圖:
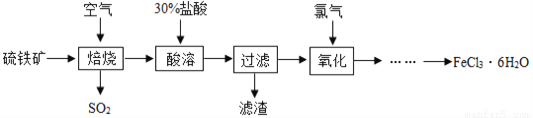
(1)已知“焙燒”階段就是硫鐵礦的燃燒,生成物是Fe2O3和SO2,寫出該反應的化學方程式 _________________,硫鐵礦進行燃燒前要將其粉碎,其目的是____________。
(2)大量排放出的SO2能形成_________,危害環境,可將含SO2的廢氣通入氨水中,氨水的pH______7,反應后生成的亞硫酸銨[(NH4)2SO3]在農業上可做__________肥。
(3)①流程中用30%鹽酸“酸溶”焙燒后的殘渣,寫出化學方程式_________;
②在“酸溶”時是否可以用硫酸代替鹽酸?________(填“可以”或“不可以”),原因是____;
③若在實驗室欲用38%(密度為1.18 g/ml)的鹽酸配制30%的鹽酸,則需要的玻璃儀器有燒杯、膠頭滴管、________、________等。
(4)實際上“焙燒”階段很難做到將硫鐵礦完全反應,因“酸溶”后的混合物中有FeCl2,將其在“氧化”階段與氯氣(Cl2)反應生成FeCl3,寫出化學方程式__________________。
4 FeS2 + 11 O2 點燃 2 Fe2O3 + 8 SO2 加快反應速率,使反應更充分 酸雨 > 氮 Fe2O3 + 6 HCl = 2 FeCl3 + 3 H2O 不可以 反應后不能生成FeCl3 玻璃棒 量筒 2 FeCl2 + Cl2 = 2 FeCl3 【解析】(1)根據題中的敘述找出反應物、生成物以及反應條件,然后依據質量守恒定律書寫化學方程式;根據增大反應物的接觸面積可以...請根據裝置圖回答下列有關問題(K、K1、K2、K3為止水夾):

(1)寫出圖中標號儀器的名稱:I_____、II______.
(2)欲用過氧化氫溶液制氧氣,可選用_____發生裝置(填“A”或“B”),請寫出該反應的化學方程式______。
(3)將C和D裝置相連接能制備CO2并驗證CO2的性質.連接C和D裝置,關閉K2,打開K、K1、K3,用試管①收集CO2,此收集方法說明_____。石蕊試液最終呈_____色,使石蕊試液變色的微粒符號是______。
(4)關閉K3,打開K1、K2,燒杯中反應的化學方程式_______。
查看答案化學與我們的生活密切相關。
(1)①香煙煙氣中含有多種有害物質,不吸煙的人能聞到煙味的原因是____________;
②隨手丟棄的煙頭還容易引發火災,原因是(選填以下字母)_____________。
A.提供可燃物 B.提供氧氣 C.使可燃物的溫度達到著火點
(2)銅常用于制作導線,因為其有良好的__________性;
(3)日常生活中,常用__________的方法降低水的硬度;
(4)用洗沽精除去餐具上的油污是因為洗沽精在水中對油污具有______作用;
(5)防毒面具中使用活性炭,這是利用了活性炭的______作用;
(6)用過的鐵鍋保護不當很容易生銹,鐵生銹的實質是鐵與______和_____發生復雜的化學變化。說出一種防止鐵鍋生銹的方法____________________________________。
查看答案生活中處處有化學,化學與生活密切相關。
(1)下表為某品牌燕麥片標簽中的一部分。
每100 g含 有營養成分 | 糖類 | 油脂 | 蛋白質 | 維生素C | 鈣 | 鎂 | 鈉 | 鋅 |
7.6 g | 7.8 g | 7.4 g | 18 mg | 201 mg | 18.2 mg | 30.8 mg | 8.1 mg |
①人體所需的六大營養素在上表中未列出的是 ;②表中出現了人體所必需的微量元素,該元素是 ;③檢驗燕麥片中是否含有淀粉需用到試劑是 。
(2)民生熱詞:“舌尖上的安全”。下列做法符合食品安全要求的是
A.用碳酸氫鈉作發酵粉
B.用霉變油菜籽生產食用油
C.用碳酸鋇代替純堿蒸饅頭
D.用工業酒精勾兌飲用白酒
(3)用化學方法鑒別“冰蠶絲”(衣服面料,主要成分為合成纖維)和天然蠶絲: 。
查看答案(1)用化學符號填空:
①2個氮氣分子________________ ②銨根離子_______________
③標出五氧化二磷中磷元素的化合價_______ ④侯氏制堿法涉及到的“堿”_____
(2)現有A.干冰 B.生石灰 C.氮氣 D.銅 四種物質,用字母序號填空:
①用做食品保護氣的是______; ②常用來制造電線、電纜的單質____;
③用作人工降雨的是_______; ④可用來做食品干燥劑的是_____。
(3)寫出下列反應的化學方程式
①電解水_____ ②鐵與硫酸銅溶液反應______
③一氧化碳和氧化鐵在高溫下反應_____ ④硫酸銨與氫氧化鈉溶液混合加熱______
查看答案6.50gZn和一定量氯化亞鐵溶液,充分反應剩余固體質量為6.05g,若將剩余固體加入到足量稀鹽酸中,產生氫氣的質量
A. 0.20g B. 0.22g C. 0.18g D. 0.21g
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州市邵樊片2018屆九年級下學期第一次月考化學試卷 題型:科學探究題
過氧化鈣(CaO2)廣泛應用于水產養殖、污水處理等領域,是優良的供氧劑。
【資料】過氧化鈣(CaO2)常溫下能與水反應生成氫氧化鈣和氧氣。
【探究一】證明某種供氧劑的主要成分為過氧化鈣
(1)取一定量該供氧劑放置于試管中,向其中加水,再將帶火星的木條伸入試管口中,觀察到____,證明該供氧劑的主要成分為過氧化鈣。
(2)此供氧劑的保存方法是______。
(3)此供氧劑長期暴露在空氣中,會變質生成CaCO3。為檢驗此供氧劑是否變質,可向其加入稀鹽酸,若觀察到有氣泡生成,則判斷此供氧劑已變質。你是否認同上述方案,理由___。
【探究二】此類供氧劑中過氧化鈣(CaO2)的含量測定
【方案一】通過測定產生氧氣的體積,最終計算出供氧劑中過氧化鈣的含量。
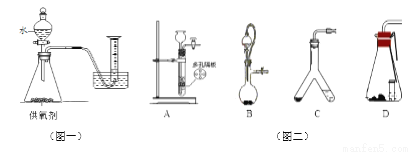
(1)取一定質量的供氧劑溶于水,按照圖一裝置進行裝配。充分反應后,待量筒中液面不再變化,還要______,再讀出體積。
(2)為保證測量結果的準確性,收集氣體的時機是___________。
a.導管口還沒有氣泡產生時 b.導管口連續均勻冒出氣泡時
c.導管口冒出氣泡很多時
(3)用此裝置測得的含量會偏大,如果將發生裝置換成圖二中的裝置__________(填序號)可以避免此誤差。
【方案二】把樣品中的過氧化鈣轉化為碳酸鈣,通過測定碳酸鈣沉淀的質量,進而求得過氧化鈣的質量。具體流程如下圖:

(1)寫出供氧劑與水反應的化學方程式__________;
(2)滴加的Na2CO3溶液要過量的原因是 __________;
(3)洗滌沉淀的目的是 __________;
(4)檢驗沉淀已經洗滌干凈的方法是:取最后一次洗滌液,滴加_____溶液,若無明顯現象,則表示已經洗凈。
(5)若供氧劑的質量m=5 g, 碳酸鈣質量n=5 g,請通過計算得出供氧劑中的過氧化鈣的含量。__________________(實驗過程)
(6)若CaCO3沉淀過濾后不洗滌,則過氧化鈣的含量將 ______ (填“偏大”、“偏小”或“無影響”)。
(7)此方案排除所加試劑和操作的原因,測定的過氧化鈣含量也可能偏大,原因是___ 。
帶火星的木條復燃 密封、干燥保存 不認同,因為鹽酸中的水與CaO2反應會生成O2,即使沒有CaCO3與鹽酸反應生成CO2,也會有氣泡生成。 使量筒內外液面相平 a BCD 2CaO2+2H2O=2Ca(OH)2+O2↑ 使氯化鈣完全轉化為沉淀 除去沉淀表面的可溶性雜質,測量結果更準確 硝酸銀溶液 72.0% 偏大 所測樣品中Ca元素還可能還來源于變質生成的Ca(OH)2、CaCO3,從而所測過氧化...自來水廠常用氯氣殺菌消毒,用明礬、氯化鐵等凈化水。以硫鐵礦(主要成分是FeS2)為原料制備氯化鐵晶體(FeCl3·6H2O)的流程如圖:

(1)已知“焙燒”階段就是硫鐵礦的燃燒,生成物是Fe2O3和SO2,寫出該反應的化學方程式 _________________,硫鐵礦進行燃燒前要將其粉碎,其目的是____________。
(2)大量排放出的SO2能形成_________,危害環境,可將含SO2的廢氣通入氨水中,氨水的pH______7,反應后生成的亞硫酸銨[(NH4)2SO3]在農業上可做__________肥。
(3)①流程中用30%鹽酸“酸溶”焙燒后的殘渣,寫出化學方程式_________;
②在“酸溶”時是否可以用硫酸代替鹽酸?________(填“可以”或“不可以”),原因是____;
③若在實驗室欲用38%(密度為1.18 g/ml)的鹽酸配制30%的鹽酸,則需要的玻璃儀器有燒杯、膠頭滴管、________、________等。
(4)實際上“焙燒”階段很難做到將硫鐵礦完全反應,因“酸溶”后的混合物中有FeCl2,將其在“氧化”階段與氯氣(Cl2)反應生成FeCl3,寫出化學方程式__________________。
查看答案請根據裝置圖回答下列有關問題(K、K1、K2、K3為止水夾):

(1)寫出圖中標號儀器的名稱:I_____、II______.
(2)欲用過氧化氫溶液制氧氣,可選用_____發生裝置(填“A”或“B”),請寫出該反應的化學方程式______。
(3)將C和D裝置相連接能制備CO2并驗證CO2的性質.連接C和D裝置,關閉K2,打開K、K1、K3,用試管①收集CO2,此收集方法說明_____。石蕊試液最終呈_____色,使石蕊試液變色的微粒符號是______。
(4)關閉K3,打開K1、K2,燒杯中反應的化學方程式_______。
查看答案化學與我們的生活密切相關。
(1)①香煙煙氣中含有多種有害物質,不吸煙的人能聞到煙味的原因是____________;
②隨手丟棄的煙頭還容易引發火災,原因是(選填以下字母)_____________。
A.提供可燃物 B.提供氧氣 C.使可燃物的溫度達到著火點
(2)銅常用于制作導線,因為其有良好的__________性;
(3)日常生活中,常用__________的方法降低水的硬度;
(4)用洗沽精除去餐具上的油污是因為洗沽精在水中對油污具有______作用;
(5)防毒面具中使用活性炭,這是利用了活性炭的______作用;
(6)用過的鐵鍋保護不當很容易生銹,鐵生銹的實質是鐵與______和_____發生復雜的化學變化。說出一種防止鐵鍋生銹的方法____________________________________。
查看答案生活中處處有化學,化學與生活密切相關。
(1)下表為某品牌燕麥片標簽中的一部分。
每100 g含 有營養成分 | 糖類 | 油脂 | 蛋白質 | 維生素C | 鈣 | 鎂 | 鈉 | 鋅 |
7.6 g | 7.8 g | 7.4 g | 18 mg | 201 mg | 18.2 mg | 30.8 mg | 8.1 mg |
①人體所需的六大營養素在上表中未列出的是 ;②表中出現了人體所必需的微量元素,該元素是 ;③檢驗燕麥片中是否含有淀粉需用到試劑是 。
(2)民生熱詞:“舌尖上的安全”。下列做法符合食品安全要求的是
A.用碳酸氫鈉作發酵粉
B.用霉變油菜籽生產食用油
C.用碳酸鋇代替純堿蒸饅頭
D.用工業酒精勾兌飲用白酒
(3)用化學方法鑒別“冰蠶絲”(衣服面料,主要成分為合成纖維)和天然蠶絲: 。
查看答案(1)用化學符號填空:
①2個氮氣分子________________ ②銨根離子_______________
③標出五氧化二磷中磷元素的化合價_______ ④侯氏制堿法涉及到的“堿”_____
(2)現有A.干冰 B.生石灰 C.氮氣 D.銅 四種物質,用字母序號填空:
①用做食品保護氣的是______; ②常用來制造電線、電纜的單質____;
③用作人工降雨的是_______; ④可用來做食品干燥劑的是_____。
(3)寫出下列反應的化學方程式
①電解水_____ ②鐵與硫酸銅溶液反應______
③一氧化碳和氧化鐵在高溫下反應_____ ④硫酸銨與氫氧化鈉溶液混合加熱______
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州江都區邵樊片2018屆九年級下學期第一次月考(七校聯考)化學試卷 題型:單選題
下列一些行為和舉措,有利于改善空氣質量的是
A. 燃放煙花爆竹 B. 大力發展火力發電
C. 露天焚燒垃圾 D. 提高電動汽車的比例
D 【解析】A、燃放煙花爆竹會產生大量的污染空氣的二氧化硫等氣體和粉塵,不利于改善空氣質量,錯誤;B、火力發電一般為燃煤發電,煤燃燒過程中會產生大量的污染空氣的氣體和粉塵,不利于改善空氣質量,錯誤;C、焚燒垃圾中會產生大量的污染空氣的氣體和粉塵,不利于改善空氣質量,錯誤;D、電動汽車的使用可有效的降低汽車尾氣排放,改善能源結構,改善空氣的質量,利于改善空氣質量,正確。故選D。過氧化鈣(CaO2)廣泛應用于水產養殖、污水處理等領域,是優良的供氧劑。
【資料】過氧化鈣(CaO2)常溫下能與水反應生成氫氧化鈣和氧氣。
【探究一】證明某種供氧劑的主要成分為過氧化鈣
(1)取一定量該供氧劑放置于試管中,向其中加水,再將帶火星的木條伸入試管口中,觀察到____,證明該供氧劑的主要成分為過氧化鈣。
(2)此供氧劑的保存方法是______。
(3)此供氧劑長期暴露在空氣中,會變質生成CaCO3。為檢驗此供氧劑是否變質,可向其加入稀鹽酸,若觀察到有氣泡生成,則判斷此供氧劑已變質。你是否認同上述方案,理由___。
【探究二】此類供氧劑中過氧化鈣(CaO2)的含量測定
【方案一】通過測定產生氧氣的體積,最終計算出供氧劑中過氧化鈣的含量。

(1)取一定質量的供氧劑溶于水,按照圖一裝置進行裝配。充分反應后,待量筒中液面不再變化,還要______,再讀出體積。
(2)為保證測量結果的準確性,收集氣體的時機是___________。
a.導管口還沒有氣泡產生時 b.導管口連續均勻冒出氣泡時
c.導管口冒出氣泡很多時
(3)用此裝置測得的含量會偏大,如果將發生裝置換成圖二中的裝置__________(填序號)可以避免此誤差。
【方案二】把樣品中的過氧化鈣轉化為碳酸鈣,通過測定碳酸鈣沉淀的質量,進而求得過氧化鈣的質量。具體流程如下圖:

(1)寫出供氧劑與水反應的化學方程式__________;
(2)滴加的Na2CO3溶液要過量的原因是 __________;
(3)洗滌沉淀的目的是 __________;
(4)檢驗沉淀已經洗滌干凈的方法是:取最后一次洗滌液,滴加_____溶液,若無明顯現象,則表示已經洗凈。
(5)若供氧劑的質量m=5 g, 碳酸鈣質量n=5 g,請通過計算得出供氧劑中的過氧化鈣的含量。__________________(實驗過程)
(6)若CaCO3沉淀過濾后不洗滌,則過氧化鈣的含量將 ______ (填“偏大”、“偏小”或“無影響”)。
(7)此方案排除所加試劑和操作的原因,測定的過氧化鈣含量也可能偏大,原因是___ 。
查看答案自來水廠常用氯氣殺菌消毒,用明礬、氯化鐵等凈化水。以硫鐵礦(主要成分是FeS2)為原料制備氯化鐵晶體(FeCl3·6H2O)的流程如圖:

(1)已知“焙燒”階段就是硫鐵礦的燃燒,生成物是Fe2O3和SO2,寫出該反應的化學方程式 _________________,硫鐵礦進行燃燒前要將其粉碎,其目的是____________。
(2)大量排放出的SO2能形成_________,危害環境,可將含SO2的廢氣通入氨水中,氨水的pH______7,反應后生成的亞硫酸銨[(NH4)2SO3]在農業上可做__________肥。
(3)①流程中用30%鹽酸“酸溶”焙燒后的殘渣,寫出化學方程式_________;
②在“酸溶”時是否可以用硫酸代替鹽酸?________(填“可以”或“不可以”),原因是____;
③若在實驗室欲用38%(密度為1.18 g/ml)的鹽酸配制30%的鹽酸,則需要的玻璃儀器有燒杯、膠頭滴管、________、________等。
(4)實際上“焙燒”階段很難做到將硫鐵礦完全反應,因“酸溶”后的混合物中有FeCl2,將其在“氧化”階段與氯氣(Cl2)反應生成FeCl3,寫出化學方程式__________________。
查看答案請根據裝置圖回答下列有關問題(K、K1、K2、K3為止水夾):

(1)寫出圖中標號儀器的名稱:I_____、II______.
(2)欲用過氧化氫溶液制氧氣,可選用_____發生裝置(填“A”或“B”),請寫出該反應的化學方程式______。
(3)將C和D裝置相連接能制備CO2并驗證CO2的性質.連接C和D裝置,關閉K2,打開K、K1、K3,用試管①收集CO2,此收集方法說明_____。石蕊試液最終呈_____色,使石蕊試液變色的微粒符號是______。
(4)關閉K3,打開K1、K2,燒杯中反應的化學方程式_______。
查看答案化學與我們的生活密切相關。
(1)①香煙煙氣中含有多種有害物質,不吸煙的人能聞到煙味的原因是____________;
②隨手丟棄的煙頭還容易引發火災,原因是(選填以下字母)_____________。
A.提供可燃物 B.提供氧氣 C.使可燃物的溫度達到著火點
(2)銅常用于制作導線,因為其有良好的__________性;
(3)日常生活中,常用__________的方法降低水的硬度;
(4)用洗沽精除去餐具上的油污是因為洗沽精在水中對油污具有______作用;
(5)防毒面具中使用活性炭,這是利用了活性炭的______作用;
(6)用過的鐵鍋保護不當很容易生銹,鐵生銹的實質是鐵與______和_____發生復雜的化學變化。說出一種防止鐵鍋生銹的方法____________________________________。
查看答案生活中處處有化學,化學與生活密切相關。
(1)下表為某品牌燕麥片標簽中的一部分。
每100 g含 有營養成分 | 糖類 | 油脂 | 蛋白質 | 維生素C | 鈣 | 鎂 | 鈉 | 鋅 |
7.6 g | 7.8 g | 7.4 g | 18 mg | 201 mg | 18.2 mg | 30.8 mg | 8.1 mg |
①人體所需的六大營養素在上表中未列出的是 ;②表中出現了人體所必需的微量元素,該元素是 ;③檢驗燕麥片中是否含有淀粉需用到試劑是 。
(2)民生熱詞:“舌尖上的安全”。下列做法符合食品安全要求的是
A.用碳酸氫鈉作發酵粉
B.用霉變油菜籽生產食用油
C.用碳酸鋇代替純堿蒸饅頭
D.用工業酒精勾兌飲用白酒
(3)用化學方法鑒別“冰蠶絲”(衣服面料,主要成分為合成纖維)和天然蠶絲: 。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州江都區邵樊片2018屆九年級下學期第一次月考(七校聯考)化學試卷 題型:單選題
下列變化過程中主要發生物理變化的是
A. 石油分餾 B. 火藥爆炸 C. 糧食釀酒 D. 百煉成鋼
A 【解析】A、石油分餾是利用石油中各組分的沸點不同,進行分餾,分餾的過程中沒有新物質生成,屬于物理變化,正確;B、火藥爆炸是利用火藥與氧氣發生劇烈的氧化反應,屬于化學變化,錯誤;C、糧食釀酒有新的物質乙醇生成,屬于化學變化,錯誤;D、百煉成鋼的過程中有新物質生成,屬于化學變化,錯誤。故選A。下列一些行為和舉措,有利于改善空氣質量的是
A. 燃放煙花爆竹 B. 大力發展火力發電
C. 露天焚燒垃圾 D. 提高電動汽車的比例
查看答案過氧化鈣(CaO2)廣泛應用于水產養殖、污水處理等領域,是優良的供氧劑。
【資料】過氧化鈣(CaO2)常溫下能與水反應生成氫氧化鈣和氧氣。
【探究一】證明某種供氧劑的主要成分為過氧化鈣
(1)取一定量該供氧劑放置于試管中,向其中加水,再將帶火星的木條伸入試管口中,觀察到____,證明該供氧劑的主要成分為過氧化鈣。
(2)此供氧劑的保存方法是______。
(3)此供氧劑長期暴露在空氣中,會變質生成CaCO3。為檢驗此供氧劑是否變質,可向其加入稀鹽酸,若觀察到有氣泡生成,則判斷此供氧劑已變質。你是否認同上述方案,理由___。
【探究二】此類供氧劑中過氧化鈣(CaO2)的含量測定
【方案一】通過測定產生氧氣的體積,最終計算出供氧劑中過氧化鈣的含量。

(1)取一定質量的供氧劑溶于水,按照圖一裝置進行裝配。充分反應后,待量筒中液面不再變化,還要______,再讀出體積。
(2)為保證測量結果的準確性,收集氣體的時機是___________。
a.導管口還沒有氣泡產生時 b.導管口連續均勻冒出氣泡時
c.導管口冒出氣泡很多時
(3)用此裝置測得的含量會偏大,如果將發生裝置換成圖二中的裝置__________(填序號)可以避免此誤差。
【方案二】把樣品中的過氧化鈣轉化為碳酸鈣,通過測定碳酸鈣沉淀的質量,進而求得過氧化鈣的質量。具體流程如下圖:

(1)寫出供氧劑與水反應的化學方程式__________;
(2)滴加的Na2CO3溶液要過量的原因是 __________;
(3)洗滌沉淀的目的是 __________;
(4)檢驗沉淀已經洗滌干凈的方法是:取最后一次洗滌液,滴加_____溶液,若無明顯現象,則表示已經洗凈。
(5)若供氧劑的質量m=5 g, 碳酸鈣質量n=5 g,請通過計算得出供氧劑中的過氧化鈣的含量。__________________(實驗過程)
(6)若CaCO3沉淀過濾后不洗滌,則過氧化鈣的含量將 ______ (填“偏大”、“偏小”或“無影響”)。
(7)此方案排除所加試劑和操作的原因,測定的過氧化鈣含量也可能偏大,原因是___ 。
查看答案自來水廠常用氯氣殺菌消毒,用明礬、氯化鐵等凈化水。以硫鐵礦(主要成分是FeS2)為原料制備氯化鐵晶體(FeCl3·6H2O)的流程如圖:

(1)已知“焙燒”階段就是硫鐵礦的燃燒,生成物是Fe2O3和SO2,寫出該反應的化學方程式 _________________,硫鐵礦進行燃燒前要將其粉碎,其目的是____________。
(2)大量排放出的SO2能形成_________,危害環境,可將含SO2的廢氣通入氨水中,氨水的pH______7,反應后生成的亞硫酸銨[(NH4)2SO3]在農業上可做__________肥。
(3)①流程中用30%鹽酸“酸溶”焙燒后的殘渣,寫出化學方程式_________;
②在“酸溶”時是否可以用硫酸代替鹽酸?________(填“可以”或“不可以”),原因是____;
③若在實驗室欲用38%(密度為1.18 g/ml)的鹽酸配制30%的鹽酸,則需要的玻璃儀器有燒杯、膠頭滴管、________、________等。
(4)實際上“焙燒”階段很難做到將硫鐵礦完全反應,因“酸溶”后的混合物中有FeCl2,將其在“氧化”階段與氯氣(Cl2)反應生成FeCl3,寫出化學方程式__________________。
查看答案請根據裝置圖回答下列有關問題(K、K1、K2、K3為止水夾):

(1)寫出圖中標號儀器的名稱:I_____、II______.
(2)欲用過氧化氫溶液制氧氣,可選用_____發生裝置(填“A”或“B”),請寫出該反應的化學方程式______。
(3)將C和D裝置相連接能制備CO2并驗證CO2的性質.連接C和D裝置,關閉K2,打開K、K1、K3,用試管①收集CO2,此收集方法說明_____。石蕊試液最終呈_____色,使石蕊試液變色的微粒符號是______。
(4)關閉K3,打開K1、K2,燒杯中反應的化學方程式_______。
查看答案化學與我們的生活密切相關。
(1)①香煙煙氣中含有多種有害物質,不吸煙的人能聞到煙味的原因是____________;
②隨手丟棄的煙頭還容易引發火災,原因是(選填以下字母)_____________。
A.提供可燃物 B.提供氧氣 C.使可燃物的溫度達到著火點
(2)銅常用于制作導線,因為其有良好的__________性;
(3)日常生活中,常用__________的方法降低水的硬度;
(4)用洗沽精除去餐具上的油污是因為洗沽精在水中對油污具有______作用;
(5)防毒面具中使用活性炭,這是利用了活性炭的______作用;
(6)用過的鐵鍋保護不當很容易生銹,鐵生銹的實質是鐵與______和_____發生復雜的化學變化。說出一種防止鐵鍋生銹的方法____________________________________。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:江蘇省揚州江都區邵樊片2018屆九年級下學期第一次月考(七校聯考)化學試卷 題型:單選題
空氣中體積分數最大的是( )
A. 氮氣 B. 氧氣 C. 稀有氣體 D. 水蒸氣
A 【解析】空氣的成分按體積計算,大約是:氮氣占78%、氧氣占21%、稀有氣體占0.94%、二氧化碳占0.03%、其它氣體和雜質占0.03%。故選A。下列變化過程中主要發生物理變化的是
A. 石油分餾 B. 火藥爆炸 C. 糧食釀酒 D. 百煉成鋼
查看答案下列一些行為和舉措,有利于改善空氣質量的是
A. 燃放煙花爆竹 B. 大力發展火力發電
C. 露天焚燒垃圾 D. 提高電動汽車的比例
查看答案過氧化鈣(CaO2)廣泛應用于水產養殖、污水處理等領域,是優良的供氧劑。
【資料】過氧化鈣(CaO2)常溫下能與水反應生成氫氧化鈣和氧氣。
【探究一】證明某種供氧劑的主要成分為過氧化鈣
(1)取一定量該供氧劑放置于試管中,向其中加水,再將帶火星的木條伸入試管口中,觀察到____,證明該供氧劑的主要成分為過氧化鈣。
(2)此供氧劑的保存方法是______。
(3)此供氧劑長期暴露在空氣中,會變質生成CaCO3。為檢驗此供氧劑是否變質,可向其加入稀鹽酸,若觀察到有氣泡生成,則判斷此供氧劑已變質。你是否認同上述方案,理由___。
【探究二】此類供氧劑中過氧化鈣(CaO2)的含量測定
【方案一】通過測定產生氧氣的體積,最終計算出供氧劑中過氧化鈣的含量。

(1)取一定質量的供氧劑溶于水,按照圖一裝置進行裝配。充分反應后,待量筒中液面不再變化,還要______,再讀出體積。
(2)為保證測量結果的準確性,收集氣體的時機是___________。
a.導管口還沒有氣泡產生時 b.導管口連續均勻冒出氣泡時
c.導管口冒出氣泡很多時
(3)用此裝置測得的含量會偏大,如果將發生裝置換成圖二中的裝置__________(填序號)可以避免此誤差。
【方案二】把樣品中的過氧化鈣轉化為碳酸鈣,通過測定碳酸鈣沉淀的質量,進而求得過氧化鈣的質量。具體流程如下圖:

(1)寫出供氧劑與水反應的化學方程式__________;
(2)滴加的Na2CO3溶液要過量的原因是 __________;
(3)洗滌沉淀的目的是 __________;
(4)檢驗沉淀已經洗滌干凈的方法是:取最后一次洗滌液,滴加_____溶液,若無明顯現象,則表示已經洗凈。
(5)若供氧劑的質量m=5 g, 碳酸鈣質量n=5 g,請通過計算得出供氧劑中的過氧化鈣的含量。__________________(實驗過程)
(6)若CaCO3沉淀過濾后不洗滌,則過氧化鈣的含量將 ______ (填“偏大”、“偏小”或“無影響”)。
(7)此方案排除所加試劑和操作的原因,測定的過氧化鈣含量也可能偏大,原因是___ 。
查看答案自來水廠常用氯氣殺菌消毒,用明礬、氯化鐵等凈化水。以硫鐵礦(主要成分是FeS2)為原料制備氯化鐵晶體(FeCl3·6H2O)的流程如圖:

(1)已知“焙燒”階段就是硫鐵礦的燃燒,生成物是Fe2O3和SO2,寫出該反應的化學方程式 _________________,硫鐵礦進行燃燒前要將其粉碎,其目的是____________。
(2)大量排放出的SO2能形成_________,危害環境,可將含SO2的廢氣通入氨水中,氨水的pH______7,反應后生成的亞硫酸銨[(NH4)2SO3]在農業上可做__________肥。
(3)①流程中用30%鹽酸“酸溶”焙燒后的殘渣,寫出化學方程式_________;
②在“酸溶”時是否可以用硫酸代替鹽酸?________(填“可以”或“不可以”),原因是____;
③若在實驗室欲用38%(密度為1.18 g/ml)的鹽酸配制30%的鹽酸,則需要的玻璃儀器有燒杯、膠頭滴管、________、________等。
(4)實際上“焙燒”階段很難做到將硫鐵礦完全反應,因“酸溶”后的混合物中有FeCl2,將其在“氧化”階段與氯氣(Cl2)反應生成FeCl3,寫出化學方程式__________________。
查看答案請根據裝置圖回答下列有關問題(K、K1、K2、K3為止水夾):

(1)寫出圖中標號儀器的名稱:I_____、II______.
(2)欲用過氧化氫溶液制氧氣,可選用_____發生裝置(填“A”或“B”),請寫出該反應的化學方程式______。
(3)將C和D裝置相連接能制備CO2并驗證CO2的性質.連接C和D裝置,關閉K2,打開K、K1、K3,用試管①收集CO2,此收集方法說明_____。石蕊試液最終呈_____色,使石蕊試液變色的微粒符號是______。
(4)關閉K3,打開K1、K2,燒杯中反應的化學方程式_______。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com