
科目: 來源: 題型:計算題
(5分)某化學興趣小組為了測定一工廠廢水中硫酸的質量分數,取100g廢水于燒杯中,加入80g質量分數為10%的氫氧化鈉溶液,恰好完全反應(廢水中無不溶物,其它成份不與氫氧化鈉反應)。試計算廢水中硫酸的質量分數。
查看答案和解析>>
科目: 來源: 題型:計算題
我國北方某鹽湖生產的純堿(Na2CO3)產品中常含有少量的氯化鈉(其它雜質忽略不計)。為測定該產品中碳酸鈉的質量分數,現稱取6g試樣放在燒杯中并滴入稀鹽酸。當鹽酸滴加至36.5g時,燒杯內溶液的總質量為40.3g,(假設產生的氣體全部逸出),產生氣體的質量與滴入稀鹽酸的質量關系如下圖所示。試計算: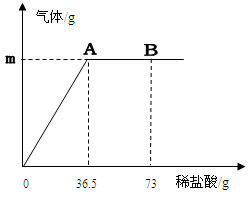
(1)A點產生氣體的質量m=_________。
(2)試樣中碳酸鈉的質量分數(結果精確至0.1%)。
(3)B點時,燒杯內溶液中的溶質是__________(寫出化學式)。
查看答案和解析>>
科目: 來源: 題型:計算題
(7分)某煉鐵企業以焦炭、赤鐵礦等為主要原材料煉鐵,反應過程如下:
(1)過程①中發生的反應屬于_______反應(選填“化合”、“分解”、“置換”、“復分解”之一),過程③是利用了一氧化碳的______(選填“氧化性” “還原性”之一)。
(2)列舉一例防止鋼鐵銹蝕的具體措施:________________________________。
(3)試用化學方程式計算:該企業用 1000t 含氧化鐵 80%的赤鐵礦可煉得金屬鐵多少噸?
查看答案和解析>>
科目: 來源: 題型:計算題
(8分)某環保小組監測到一工廠排放的廢水中含有H2SO4和CuSO4 。為了測定廢水中CuSO4的質量分數,該小組取了100g廢水,逐滴加入10%的NaOH溶液至過量。測得生成Cu(OH)2沉淀質量與所加NaOH溶液質量關系如下圖所示。 
(1)與H2SO4反應的NaOH溶液質量為 g;100g廢水中H2SO4的質量為 g。
(2)計算廢水中CuSO4的質量分數。
查看答案和解析>>
科目: 來源: 題型:計算題
某化學興趣小組為了測定鎂銅合金中鎂的質量分數,取出3g合金樣品,將60g稀硫酸分6次加入樣品中,充分反應后過濾、洗滌、干燥、稱重,得到的實驗數據如下:
| 稀硫酸用量 | 剩余固體質量 | 稀硫酸用量 | 剩余固體質量 |
| 第一次加入10g | mg | 第四次加入10g | 1.0g |
| 第二次加入10g | 2.0g | 第五次加入10g | 0.6g |
| 第三次加入10g | 1.5g | 第六次加入10g | 0.6g |
查看答案和解析>>
科目: 來源: 題型:計算題
(5分)醫學上常用雙氧水來清洗創口和局部抗菌。小美同學為了測定一瓶醫用雙氧水溶液的溶質質量分數,取該雙氧水69g放入燒杯中,然后加入2g二氧化錳,完全反應后,稱得燒杯內剩余物質的總質量為69.4g。請回答下列問題;
(1)二氧化錳在反應中的作用是 。
(2)該雙氧水溶液的溶質質量分數(結果精確到0.1%)。
查看答案和解析>>
科目: 來源: 題型:計算題
實驗室用過量的稀鹽酸和大理石制取CO2,取50g反應后的濾液,逐滴滴入碳酸鈉溶液,測得滴入碳酸鈉溶液的質量與產生沉淀
質量的關系曲線如圖所示。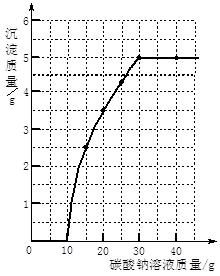
回答下列問題:
(1)從圖中看出生成沉淀的最大質量是 g。
(2)開始加入碳酸鈉溶液至10g時,還沒有沉淀的原
因是 。
(3)計算原濾液中氯化鈣的質量分數。
查看答案和解析>>
科目: 來源: 題型:計算題
(5分)現將一定質量含氫氧化鈉的碳酸鈉固體中加入100g水充分溶解,向該溶液中逐滴加入溶質質量分數為10%的鹽酸,生成氣體的質量與加入鹽酸的質量關系如圖所示。
⑴當鹽酸質量為150g時,溶液中溶質化學式為 ;
⑵求固體中碳酸鈉的質量?(寫出計算過程,保留一位小數)
⑶當充分反應后溶液中氯化鈉的質量為 g。
查看答案和解析>>
科目: 來源: 題型:計算題
(6分)某地一輛滿載濃硫酸的罐車翻倒,導致溶質質量分數為98%的濃硫酸25t泄漏,并向路基兩邊蔓延。接到報警后消防官兵立即趕來并用石灰漿(主要成分為氫氧化鈣)中和硫酸解除了險情。請回答:
(1)溶質質量分數為98%的濃硫酸25t中含H2SO4的質量為 ;
(2)計算:中和泄漏的硫酸,理論上需要多少噸氫氧化鈣?
查看答案和解析>>
科目: 來源: 題型:計算題
(6分)某純堿樣品中含有一定量的食鹽,為測定其中氯化鈉的含量,化學小組的同學將某純堿樣品12.3g放入燒杯中,逐滴加入75g稀鹽酸,恰好完全反應,待不再產生氣泡時,得到84g的食鹽溶液。計算原混合物中氯化鈉的質量分數(CO2的溶解忽略不計)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com