
某石灰廠有一批石灰石原料,為了測定該石灰石的純度,廠化驗室技術員稱取6.25 g研碎的石灰石粉末,進行四次高溫煅燒(雜質沒有變化)、冷卻、稱量剩余固體質量的重復操作,記錄數據如下:
| 操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余固體質量 | 5.55g | 4.35g | 4.05g | 4.05g |
2.2 80%
解析試題分析:(1)根據題意可知,CaCO3 CaO+CO2↑,由于反應后有氣體逸出,故反應后的固體質量會減小;分析圖表可知,第三次與第四次反應后剩余固體質量相等,說明第三次已是完全反應;再根據質量守恒定律,在化學反應中,參加反應的各物質的質量總和等于反應后生成的各物質的質量總和,可知完全反應后生成二氧化碳的質量=反應前物質的質量總和-反應后固體物質的質量總和=6.25g-4.05g=2.2g;
CaO+CO2↑,由于反應后有氣體逸出,故反應后的固體質量會減小;分析圖表可知,第三次與第四次反應后剩余固體質量相等,說明第三次已是完全反應;再根據質量守恒定律,在化學反應中,參加反應的各物質的質量總和等于反應后生成的各物質的質量總和,可知完全反應后生成二氧化碳的質量=反應前物質的質量總和-反應后固體物質的質量總和=6.25g-4.05g=2.2g;
(2)根據碳酸鈣高溫煅燒的化學反應方程式和生成的二氧化碳的質量,可計算出反應的碳酸鈣的質量,然后根據質量分數公式計算即可。
解:設生成2.2g二氧化碳,需碳酸鈣的質量為x
CaCO3 CaO+CO2↑
CaO+CO2↑
100 44
X 2.2g
100:44=X:2.2g
解得,X=5g
則石灰石樣品中碳酸鈣的質量分數=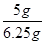 ×100%=80%。
×100%=80%。
答:石灰石樣品中碳酸鈣的質量分數為80%。
考點:質量守恒定律及其應用,根據化學反應方程式的計算
點評:此題是關于化學方程式的計算題,要求學生要有較強的圖表分析能力,解題的關鍵是,要會利用質量守恒定律,結合表格分析判斷反應的進行情況,以及反應放出的二氧化碳的質量;然后再根據相關的化學反應方程式,并依據已知量對未知的應求量進行求解計算即可,注意解題要規(guī)范。


科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
 化學興趣小組的同學在綜合實踐中了解到,某石灰廠有一批石灰石原料,其中含有的雜質是二氧化硅(二氧化硅不溶于水,不與鹽酸反應,高溫時不發(fā)生分解反應).為了測定該石灰石的純度,興趣小組同學取用2g這種石灰石樣品,并取稀鹽酸20g分4次加入樣品中進行實驗,結果如下:
化學興趣小組的同學在綜合實踐中了解到,某石灰廠有一批石灰石原料,其中含有的雜質是二氧化硅(二氧化硅不溶于水,不與鹽酸反應,高溫時不發(fā)生分解反應).為了測定該石灰石的純度,興趣小組同學取用2g這種石灰石樣品,并取稀鹽酸20g分4次加入樣品中進行實驗,結果如下:| 稀鹽酸的用量/g | 剩余固體的質量/g |
| 第一次加入5 | 1.5 |
| 第二次加入5 | 1.0 |
| 第三次加入5 | 0.5 |
| 第四次加入5 | 0.3 |
查看答案和解析>>
科目:初中化學 來源: 題型:
 化學興趣小組同學在綜合實踐活動中了解到,某石灰廠有一批石灰石原料,其中含有的雜質是二氧化硅(二氧化硅不溶于水,不能與鹽酸反應,高溫時不發(fā)生分解反應).為了測定該石灰石的純度,興趣小組同學取用2g這種石灰石樣品,用實驗室現有的未知溶質質量分數的稀鹽酸20g分4次加入,充分反應后,經過濾、干燥等操作后稱量,每次稀鹽酸用量及剩余固體的質量見下表,利用實驗數據繪制的圖象見下圖.(保留一位有效數字)
化學興趣小組同學在綜合實踐活動中了解到,某石灰廠有一批石灰石原料,其中含有的雜質是二氧化硅(二氧化硅不溶于水,不能與鹽酸反應,高溫時不發(fā)生分解反應).為了測定該石灰石的純度,興趣小組同學取用2g這種石灰石樣品,用實驗室現有的未知溶質質量分數的稀鹽酸20g分4次加入,充分反應后,經過濾、干燥等操作后稱量,每次稀鹽酸用量及剩余固體的質量見下表,利用實驗數據繪制的圖象見下圖.(保留一位有效數字)| 稀鹽酸的用量 | 剩余固體的質量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | 0.5g |
| 第四次加入5g | 0.3g |
查看答案和解析>>
科目:初中化學 來源: 題型:
 某石灰廠有一批石灰石原料,其中含有的雜質不與鹽酸反應.為了測定該石灰石的純度,興趣小組的同學取用2g這種石灰石樣品,并把20g稀鹽酸分四次加入,充分反應后,經過濾、干燥等操作后,根據每次稀鹽酸用量及剩余固體質量和實驗數據繪制成圖象(如圖).計算:
某石灰廠有一批石灰石原料,其中含有的雜質不與鹽酸反應.為了測定該石灰石的純度,興趣小組的同學取用2g這種石灰石樣品,并把20g稀鹽酸分四次加入,充分反應后,經過濾、干燥等操作后,根據每次稀鹽酸用量及剩余固體質量和實驗數據繪制成圖象(如圖).計算:查看答案和解析>>
科目:初中化學 來源: 題型:
| 操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余固體質量 | 11.1g | 8.7g | 8.1g | 8.1g |
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com