7.2克碳和一定量的氧氣在某密閉容器內恰好完全反應,生成的氣體的質量不可能是( )
A.44克
B.16.8克
C.17.8克
D.26.4克
【答案】
分析:因為已知碳在氧氣中充分燃燒生成二氧化碳,不充分燃燒生成一氧化碳,而此題最終生成的氣體可能是二氧化碳,也可能是一氧化碳,也可能是二者的混合物.
所以首先假設7.2g碳在氧氣中完全燃燒,計算出所得二氧化碳的質量;然后假設7.2g碳在氧氣中不完全燃燒,計算出所得一氧化碳的質量,那么最終氣體的質量就在這兩個數值之間.
解答:解:設7.2g碳在氧氣中完全燃燒生成二氧化碳的質量為x
C+O
2
CO
212 44
7.2g x
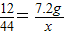
x=26.4g
再假設7.2g碳在氧氣中不充分燃燒產生的一氧化碳的質量為y
2C+O
2
2CO
2×12 2×28
7.2g y
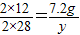
y=16.8g
7.2克碳和氧氣完全反應生成的氣體的質量應該≥16.8g,而≤26.4g所以A不正確
故選A
點評:此題考查的是利用化學方程式的計算,此題中因為碳和氧氣反應的方程式有兩個,所以要判斷最后所得氣體的質量一般用的方法就是極端假設法,同學們只要掌握了這個方法就可以解決這一類的問題.

 CO2
CO2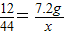
 2CO
2CO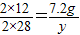


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案