
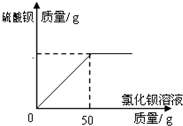
 (6)現實驗探究產品中硫酸鉀的質量分數,取該樣品10g配成溶液.滴入稍過量的質量分數為20.8%氯化鋇溶液充分反應,得到的數據如下圖,求樣品中硫酸鉀的質量分數?
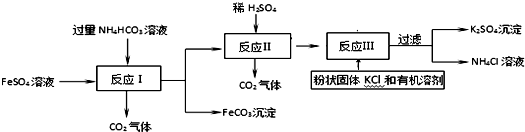
(6)現實驗探究產品中硫酸鉀的質量分數,取該樣品10g配成溶液.滴入稍過量的質量分數為20.8%氯化鋇溶液充分反應,得到的數據如下圖,求樣品中硫酸鉀的質量分數? 分析 (1)為了不帶入新的雜質,應該用鐵除去FeSO4 溶液中的雜質Fe2(SO4)3;
(2)反應Ⅰ所得混合物過濾后所得濾液的溶質有反應生成的硫酸銨和過量的碳酸氫銨;
(3)碳酸氫銨能和稀硫酸反應生成硫酸銨、水和二氧化碳;
(4)硫酸銨和氯化鉀反應生成硫酸鉀和氯化銨;
因為硫酸鉀在有機溶劑中的溶解度很小,因此加入有機溶劑能使硫酸鉀從溶液中析出;
(5)飽和硫酸鉀溶液中不能溶解硫酸鉀,但是能夠溶解其它一些溶質;
(6)硫酸鉀和氯化鋇反應生成白色沉淀硫酸鋇和氯化鉀,根據圖中提供的信息和提供的數據及其反應的化學方程式可以進行相關方面的計算.
解答 解:(1)反應I前除去FeSO4 溶液中的雜質Fe2(SO4)3需加入鐵屑,而加入鋅、銅會帶入新的雜質.
故填:B.
(2)反應Ⅰ所得混合物過濾后所得濾液的溶質有過量的碳酸氫銨和反應生成的硫酸銨.
故填:NH4HCO3和(NH4)2SO4.
(3)反應Ⅱ中,碳酸氫銨能和稀硫酸反應生成硫酸銨、水和二氧化碳,因此加入稀硫酸的作用是除去過量的碳酸氫銨.
故填:除去過量的碳酸氫銨.
(4)硫酸銨和氯化鉀反應生成硫酸鉀和氯化銨,反應的化學方程式為:(NH4)2SO4+2KCl=K2SO4+2NH4Cl;
工業生產上常在反應Ⅲ過程中加入一定量的有機溶劑,其目的是減小硫酸鉀的溶解度,使硫酸鉀析出.
故填:(NH4)2SO4+2KCl=K2SO4+2NH4Cl;減小硫酸鉀的溶解度,使硫酸鉀析出.
(5)反應Ⅲ得到的K2SO4固體沉淀需要經過洗滌,才能得到純度高的產品.洗滌時最好用K2SO4飽和溶液,這樣既能夠保證硫酸鉀不損失,又能夠除去硫酸鉀中的雜質.
故填:C.
(6)設樣品中硫酸鉀質量為x,
BaCl2+K2SO4═BaSO4↓+2KCl,
208 174
50g×20.8% x
$\frac{208}{174}=\frac{50g×20.8%}{x}$
x=8.7g,
樣品中硫酸鉀的質量分數為:$\frac{8.7g}{10g}$×100%=87%,
答:樣品中硫酸鉀的質量分數為87%.
點評 本題主要考查物質的性質和根據化學方程式進行計算的能力,解答時要根據各種物質的性質,結合各方面條件進行分析、判斷,從而得出正確的結論,計算時要注意規范性和準確性.


 桃李文化快樂暑假武漢出版社系列答案
桃李文化快樂暑假武漢出版社系列答案 優秀生快樂假期每一天全新寒假作業本系列答案
優秀生快樂假期每一天全新寒假作業本系列答案 暑假接力賽新疆青少年出版社系列答案
暑假接力賽新疆青少年出版社系列答案科目:初中化學 來源: 題型:推斷題
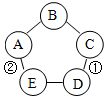 如圖表示的物質A~E相互的關系(“-”表示兩端的物質能發生化學反應).其中A廣泛用于玻璃、造紙、紡織和洗滌劑的生產等;C是一種藍色溶液;D是使用最多的金屬材料.
如圖表示的物質A~E相互的關系(“-”表示兩端的物質能發生化學反應).其中A廣泛用于玻璃、造紙、紡織和洗滌劑的生產等;C是一種藍色溶液;D是使用最多的金屬材料.查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
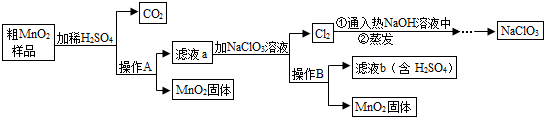
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
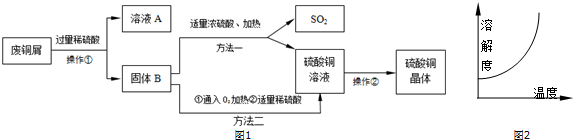
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
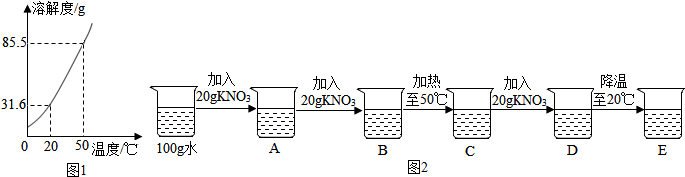
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
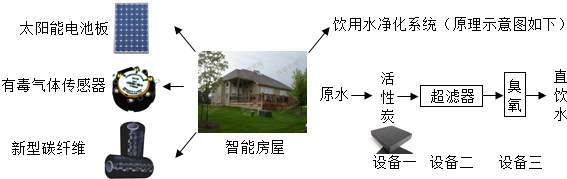
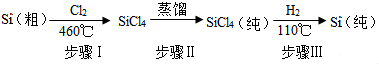
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com