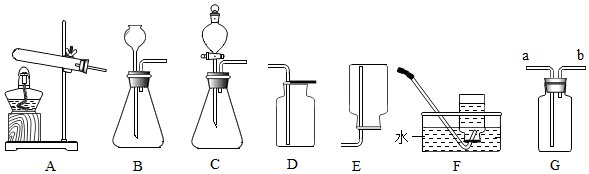
8.探究一、請根據下列實驗裝置圖答問題.
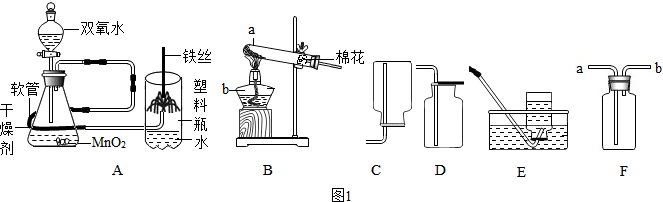
(1)寫出圖1中儀器a、b、名稱:a試管,b酒精燈.
(2)用圖1中B裝置制取O
2的文字(或符號)表達式為高錳酸鉀$\stackrel{加熱}{→}$錳酸鉀+二氧化錳+氧氣(2KMnO
4$\frac{\underline{\;\;△\;\;}}{\;}$K
2MnO
4+MnO
2+O
2↑),若要收集干燥的氧氣應選用的收集裝置為D(填裝置序號),如果用F裝置收集氧氣,則應從a端通入,其驗滿的操作方法是將帶火星的木條放在導管口,木條復燃,證明集滿.
(3)如圖1中A時“鐵絲在氧氣中燃燒”實驗的改進裝置,實驗時打開分液漏斗活塞,通入干燥氧氣約10秒,引燃鐵絲下端火柴桿,伸入塑料瓶內,并對準玻璃管扣正上方,觀察到的現象是鐵絲劇烈燃燒,火星四射,生成黑色固體.
改進后的優點是①②③(填序號).
①氧氣無需提前制備和收集,操作更方便
②塑料瓶代替集氣瓶,防止集氣瓶炸裂,更安全
③裝置集氧氣的制取、干燥、和性質驗證于一體,實驗更優化.
(4)某興趣小組同學將帶火星的木條伸入到收集滿氧氣的集氣瓶中,木條復燃,拿出木條,蓋好集氣瓶,過一會兒,再用帶火星的木條伸入瓶中,木條仍然復燃,重復以上操作,直到木條不再復燃,據此現象你能得到的結論是帶火星的木條是否復燃與氧氣的濃度有關.
(5)該興趣小組同學還做了如圖2中的趣味實驗,圖中現象是在量筒中涌出柱狀的泡沫,可形象地稱為“大象牙膏”,其原理主要是雙氧水在某些催化劑作用下迅速分解產生水和氧氣,反應的文字(或符號)表達式為過氧化氫$\stackrel{二氧化錳}{→}$水+氧氣(2H
2O
2$\frac{\underline{\;MnO_2\;}}{\;}$2H
2O+O
2↑).
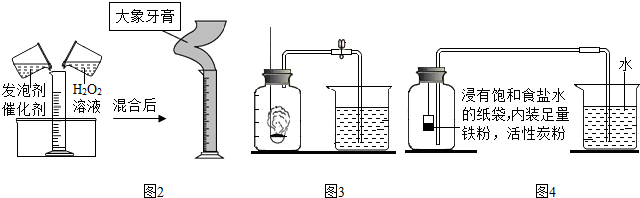
探究二、如圖3是小紅同學設計的某探究實驗的裝置,請你協助他共同完成下列實驗相關的內容.
(1)實驗探究的目的是探究空氣中氧氣的含量.
(2)收集的信息數據:①空氣中N
2占78%,O
2占21%,其它其它及雜質占1%(按體積計)②O2可支持燃燒③紅磷、硫、木炭都可以在空氣中燃燒
(3)方案設計:利用A在空氣中燃燒以消耗空氣中O
2的實驗完成(填寫字母).
A、紅磷 B、硫 C、木炭
(4)實驗現象:紅磷燃燒放出熱量,生成大量的白煙,燒杯中的水會進入到瓶中約占瓶中體積的五分之一
(5)實驗結論:氧氣約占空氣體積的五分之一
(6)寫出該反應的文字(或符號)表達式是4P+5O
2$\frac{\underline{\;點燃\;}}{\;}$2P
2O
5.
(7)結論分析:若實驗所得結論與實際結論偏高,可能的原因是:
a、紅磷的量不足
b、沒有等裝置冷卻就打開止水夾
(8)啟示:通過該實驗,我們預測瓶中剩余氮氣的一個性質:難溶于水,不支持燃燒.
【實驗改進】小剛同學查得實驗資料表明:燃燒過程中當氧氣體積分數低于7%時,紅磷就無法繼續燃燒,因此通過上述實驗,測置結果與理論值誤差較大.
【實驗改進】
Ⅰ.根據鐵在空氣中生銹的二元論設計如圖4實驗裝置,再次測定空氣中氧氣含量,裝置中飽和食鹽水、活性炭會加速鐵生銹.
Ⅱ.測得實驗數據如表
| 測量項目 | 實驗前 | 實驗后 |
| 燒杯中水的體積 | 燒杯中剩余水的體積 | 集氣瓶(扣除內容物)和導管的容積 |
| 體積 | 80.0 | 54.5 | 126.0 |
(9)【交流表達】
①鐵生銹過程發生復雜的化學反應,首先是鐵與氧氣、水反應生成氫氧化亞鐵[Fe(OH)
2],寫出該反應的文字表達式為2Fe+2H
2O+O
2=2Fe(OH)
2.
②根據表中數據計算,改進實驗后測得的空氣中氧氣的體積分數是20.2%(計算結果精確到0.1%).
③從實驗原理角度分析,改進后的實驗結果比前者準確度更高的原因是:(寫出一個即可)①鐵的緩慢氧化使集氣瓶中的氧氣消耗更徹底,使實驗結果更準確.②測量時考慮到導管容積和扣除內容物后的集氣瓶容積,使實驗結果更準確.

 實驗室常用于制取氧氣的方法有:a、加熱氯酸鉀晶體和二氧化錳粉末;b、加熱高錳酸鉀固體;c、用二氧化錳粉末作催化劑使過氧化氫(H2O2)溶液分解產生水和氧氣.
實驗室常用于制取氧氣的方法有:a、加熱氯酸鉀晶體和二氧化錳粉末;b、加熱高錳酸鉀固體;c、用二氧化錳粉末作催化劑使過氧化氫(H2O2)溶液分解產生水和氧氣.