將25g大理石加入到100g稀鹽酸中恰好完全反應,測得生成二氧化碳的質量為2.2g,求:該大理石中碳酸鈣的質量為多少克?
解:設大理石中碳酸鈣的質量為x
CaCO
3+2HCl═CaCl
2+CO
2↑+H
2O
100 44
x 2.2g
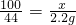
x=5g
答:該大理石中碳酸鈣的質量為5g.
分析:根據大理石中碳酸鈣的質量分數=
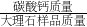
×100%,所以,需要利用反應的化學方程式根據生成二氧化碳氣體的質量計算出參加反應的碳酸鈣的質量,即樣品中所含碳酸鈣的質量.
點評:根據化學方程式進行計算時,所使用的物質的質量都是純凈物的質量,含雜質的物質的質量不能直接代入化學方程式進行計算.

 閱讀快車系列答案
閱讀快車系列答案