
【題目】A﹣G是初中化學常見物質,其中,A的濃溶液揮發出刺激性氣味的氣體,從C→D的反應過程中有黃色沉淀生成,E為白色沉淀.如圖是這些物質的轉化關系,部分反應物、生成物及反應物條件已省略.
(1)請寫出化學式:A、G .
(2)寫出D→E的化學方程式:
(3)寫出C→B的化學方程式: .
【答案】
(1)HCl;AgNO3
(2)NaCl+AgNO3=NaNO3+AgCl↓
(3)2FeCl3+Fe=3FeCl2
【解析】(1)A﹣G是初中化學常見物質,A的濃溶液能揮發出刺激性氣味的氣體,A和鐵粉、氫氧化鈉會反應,所以A是鹽酸,從C→D的反應過程中有黃色沉淀生成,依據復分解反應原理可知C中含有鐵離子,鹽酸和F會生成含有鐵離子的C,所以F可以是氧化鐵或氫氧化鐵,C就是氯化鐵,氯化鐵和氫氧化鈉反應生成黃色的氫氧化鐵沉淀和氯化鈉,鹽酸和氫氧化鈉反應也會生成氯化鈉和水,所以D是氯化鈉,氯化鐵和鐵粉反應會生成氯化亞鐵,鹽酸和鐵反應會生成氯化亞鐵和氫氣,所以B是氯化亞鐵,E為白色沉淀,A、B、D中都含有氯離子,和G反應會生成白色沉淀,所以G是硝酸銀,經過驗證,推導正確,所以A是HCl,G是AgNO3;(2)D→E的反應是氯化鈉和硝酸銀反應生成氯化銀沉淀和硝酸鈉,化學方程式為:NaCl+AgNO3=NaNO3+AgCl↓;(3)C→B的反應是氯化鐵和鐵反應生成氯化亞鐵,化學方程式為:2FeCl3+Fe=3FeCl2 .
所以答案是:(1)HCl,AgNO3;(2)NaCl+AgNO3=NaNO3+AgCl↓;(3)2FeCl3+Fe=3FeCl2 .
【考點精析】認真審題,首先需要了解書寫化學方程式、文字表達式、電離方程式(注意:a、配平 b、條件 c、箭號).


科目:初中化學 來源: 題型:
【題目】如圖是甲、乙的溶解度曲線,下列說法不正確的是( )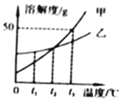
A.t1℃時,乙的溶解度大于甲的溶解度
B.t2℃時,甲、乙飽和溶液中溶質質量分數相等
C.降低溫度能使接近飽和的甲溶液變為飽和溶液
D.t2℃時,75g甲的飽和溶液中加入50g水,可以得到質量分數為25%的溶液
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】糕點疏松的主要成分中含有碳酸氫鈉,某化學興趣小組對碳酸氫鈉的化學性質進行探究.
(1)【探究實驗一】碳酸氫鈉溶液的酸堿性:用玻璃棒蘸取碳酸氫鈉溶液在pH試紙測上并與對比,讀出其pH值約為10,由此得出結論是:碳酸氫鈉溶液呈堿性.
(2)【探究實驗二】碳酸氫鈉能否與酸反應:取少量固體放入試管中,滴加足量的稀鹽酸,現象為 . 結論:碳酸氫鈉能與酸反應.
(3)【探究實驗三】碳酸氫鈉的熱穩定性:取一定量的碳酸氫鈉放在銅片上加熱,如圖所示.
①加熱一段時間后,觀察到燒杯內壁有水珠.
②充分加熱后,將燒杯迅速倒轉過來,加入適量的澄清石灰水,振蕩,觀察到石灰水變渾濁.
③通過進一步實驗來確定充分加熱后的固體產物的成分.限選試劑及儀器:稀鹽酸、氯化鈣溶液、澄清石灰水、酚酞溶液、蒸餾水、試管、膠頭滴管.
序號 | 實驗操作 | 預期現象 | 結論 |
① | 取少量加熱后的固體產物放入試管A中,加入適量蒸餾水,充分振蕩溶解,滴加足量 | 產生白色沉淀 | 產物含 |
② | 取操作①后的上層清液于試管B中,滴加 | 產物不含NaOH |
請分析上述操作①中不能用澄清石灰水替代氯化鈣溶液的理由 .
④根據上述實驗結論,寫出碳酸氫鈉受熱分解的化學方程式 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】重質碳酸鈣粉體產業為我市一大支柱產業,產品遠銷全國各地.某化學興趣小組對粉體中碳酸鈣含量進行了探究,小組成員從一包粉體產品中取出樣品5.10g放入燒杯中,并逐滴加入相同濃度的稀鹽酸(假設樣品中的雜質不參與鹽酸反應),實驗測得燒杯中物質總質量與加入稀鹽酸的總質量關系如表所示.
稀鹽酸的總質量(g) | 10.00 | 20.00 | 30.00 | 40.00 | 50.00 | 60.00 | 70.00 |
燒杯中物質總質量(g) | 14.66 | 24.22 | m | 43.34 | 52.90 | 62.90 | 72.90 |
(1)碳酸鈣的相對分子質量為 .
(2)表中m= .
(3)求樣品中碳酸鈣的質量分數(結果保留兩位小數).
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如表是硝酸鉀、氯化鈉在不同溫度下的溶解度.
溫度/℃ | 10 | 20 | 30 | 40 | 50 |
硝酸鉀的溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
氯化鈉的溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)從表中數據分析,溶解度受溫度影響較大的物質是 , 硝酸鉀和氯化鈉溶解度曲線的交點在(填字母序號)之間.
A.20℃~30℃B.30℃~40℃C.40℃~50℃
(2)20℃,將50g硝酸鉀與100g水混合,充分攪拌后靜置,得到的溶液是硝酸鉀的(“飽和”或“不飽和”)溶液,若將溫度升高到40℃,該溶解溶質的質量分數為(精確到0.1%).
(3)保持溫度為20℃,將氯化鈉的不飽和溶液變成飽和溶液,寫出一種可行的方法 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com