
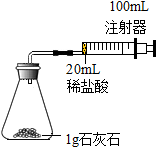
 某化學實驗小組對“影響石灰石與鹽酸反應速率的因素--鹽酸的濃度和石灰石的顆粒大小等”進行了如下實驗探究,請你參與.
某化學實驗小組對“影響石灰石與鹽酸反應速率的因素--鹽酸的濃度和石灰石的顆粒大小等”進行了如下實驗探究,請你參與.| 實驗編號 | 鹽酸溶質質量分數 (均取20mL) | 石灰石固體形狀 (均取1g) | 二氧化碳體積(mL) (均收集前30S的氣體) |
| a | 4% | 顆粒 | 64.0 |
| b | 4% | 塊狀 | 40.4 |
| c | 6% | 顆粒 | 98.2 |
| d | 6% | 塊狀 | 65.3 |
| 時間/S | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| 氣體體積/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
分析 根據影響化學反應速率的因素進行分析解答,設計實驗必須注意控制變量,據此解答.
解答 解:(1)石灰石與鹽酸反應生成氯化鈣、水和二氧化碳,其反應的化學方程式為CaCO3+2HCl═CaCl2+H2O+CO2↑,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)在裝藥品前應檢查該裝置的氣密性,具體的做法是將將注射器活塞向外拉出一段,松開手一會后,若活塞又回到原位,證明裝置氣密性良好;開始實驗時,因為鹽酸和碳酸鈣反應生成的二氧化碳會使裝置內的壓強增大,故應將20ml的稀鹽酸快速的推入錐形瓶中,以保證鹽酸能全部推入錐形瓶中,故填:將注射器活塞向外拉出一段,松開手一會后,若活塞又回到原位,證明裝置氣密性良好;快速.
(3)①要比較不同溶質質量分數的鹽酸對反應速率的影響,需要鹽酸的溶質質量分數不同,石灰石固體的顆粒相同,故可選擇的實驗編號是ac或是bd,根據相同的時間收集的二氧化碳的體積可以看出,溶質質量分數越大,反應的速率越大,故填:溶質質量分數越大,反應的速率越大.
②當顆粒大小相同時,相同的時間收集的二氧化碳的氣體的體積可以看出,顆粒越小,反應的速率越大,故填:顆粒越小,反應的速率越大.
(4)從表格數據可以分析得出,開始反應的速率大,后來的反應速率小,主要是因為隨著反應的進行,反應物被消耗,濃度減小,故填:小,反應物的濃度減小;
(5)影響石灰石與鹽酸反應速率的因素還有石灰石的純度,可以取不同地區的石灰石,保持顆粒大小以及質量相同,加入相同的鹽酸,記錄生成相同的二氧化碳氣體體積所需要的時間,純度越大,速率越大,故填:石灰石的純度;取不同地區的石灰石,保持顆粒大小以及質量相同,加入相同的鹽酸,記錄生成相同的二氧化碳氣體體積所需要的時間,純度越大,速率越大.
點評 本題考查的是實驗速率的實驗探究,完成此題,可以依據已有的知識進行.


科目:初中化學 來源: 題型:推斷題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com