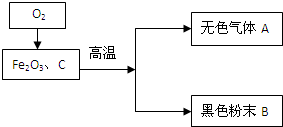
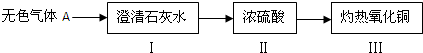
某校化學興趣小組的同學準備對某生鐵樣品中鐵的含量進行探究.請你按要求幫助他們完成下列探究報告.
[提出問題]生鐵是純鐵嗎?若不是純鐵則該生鐵樣品中鐵單質的質量分數是多少?
[查閱資料](1)生鐵中除鐵外,還含有碳、硅、錳等元素.
(2)碳在生鐵中以兩種形態存在,一種是游離碳(石墨),另一種是化合碳(如Fe
3C等);硅、錳等存在形式較為復雜.
(3)含有硅、錳等元素的物質通常都不與稀硫酸發生化學反應.
[制定方案]使生鐵樣品與過量的稀硫酸反應,稱量反應前后物質的質量差.
[實驗過程]
(1)取一只燒杯,稱得其質量為70.4g,加入一定量生鐵樣品碎屑,稱得燒杯和樣品的總質量為102.4g;
(2)向盛有生鐵樣品的燒杯中加入稀硫酸,邊加邊攪拌,直到燒杯中不再產生氣泡,再加入稀硫酸以確保過量,測得共用去稀硫酸247.3g;
(3)靜置,稱量.稱得燒杯和剩余物質的總質量為348.7g.
[數據處理]通過對以上數據的分析和計算,該生鐵樣品中鐵單質的質量分數為
%.
[交流討論]
(1)實驗稱量時稱量物應放在托盤天平的
盤(選填“左”或“右”).
(2)實驗過程中稀硫酸要過量的原因是
.
(3)反應過程中可看到有氣泡冒出,溶液由無色變為淺綠色,由此得知反應一定生成了氫氣和
(寫名稱).
(4)經質檢部門精確測定,該樣品中鐵元素的總質量分數為95.2%.對此有同學產生了疑問,請你幫他分析:
.
[實驗結論]經過以上探究,同學們知道了生鐵不是純鐵,實際上它屬于鐵的重要
.

 三點一測快樂周計劃系列答案
三點一測快樂周計劃系列答案