
【題目】(1)下表是CO2氣體在水中的幾組溶解度數據(單位:mL/100mL水)
溶解度 溫度(℃) 大氣壓 | 0 | 25 | 50 | 75 | 100 |
1 | 1.79 | 0.752 | 0.423 | 0.307 | 0.231 |
10 | 15.92 | 7.14 | 4.095 | 2.99 | 2.28 |
25 | 29.30 | 16.20 | 9.71 | 6.82 | 5.73 |
①根據CO2的溶解度表,可以得出氣體的溶解度隨外界條件的變化規律是:__________、____。
②打開可樂瓶有氣體逸出,說明原瓶中的壓強_________(填“>”、“<”或“=”)瓶外大氣壓強。
(2)甲、乙兩物質(均不含結晶水)的溶解度曲線如下圖,請回答
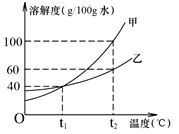
① t2℃時,甲、乙兩物質溶解度較大的是___________。
② t1℃時,50g水中加入30g乙,充分溶解所得溶液的質量是___________g。
③ t2℃時,將乙的不飽和溶液轉化為飽和溶液一定可行的方法 是___________(填編號)。
A.加足量溶質乙 B.蒸發溶劑至晶體析出 C.降溫
④ t2℃時,甲、乙溶液的溶質質量分數相等且均為a%,則甲溶液一定為__________(填“飽和”或“不飽和”)溶液,a%的取值范圍為___________。
⑤ 將t2℃等質量的甲、乙飽和溶液分別降溫到t1℃,有關說法正確的是___________。
A.t1℃時溶質質量:甲=乙 B.t1℃時溶劑質量:甲>乙
C.t1℃時溶液質量:甲<乙 D.析出晶體質量:甲>乙
【答案】 壓強相同時氣體的溶解度隨溫度升高而減小 溫度相同時氣體溶解度隨壓強的增大而增大 > 甲 70 AB 不飽和 0<a%≤37.5% CD
【解析】(1)①由題目中提供的數據可知,影響CO2的溶解度的因素是溫度與壓強,即溫度升高,氣體的溶解度減小;壓強增大,氣體的溶解度增大;壓強相同時氣體的溶解度隨溫度升高而減小;②打開可樂瓶有氣體溢出,說明壓強減小了,二氧化碳在水中的溶解度變小,從水中逸出,說明原瓶中的壓強大于瓶外大氣壓強;(2)①由甲、乙兩種物質的溶解度曲線可知,t2℃時,甲、乙兩種物質溶解度較大的是甲;②由乙物質的溶解度曲線可知,t1℃時,乙物質的溶解度是40g,t1℃時,50g水中放入30g乙,只能溶解20g,充分溶解后所得溶液的質量是50g+20g=70g;③③由圖示信息可知t2℃時,將乙的不飽和溶液轉化為飽和溶液一定可行的方法是:加足量溶質乙;蒸發溶劑至晶體析出;④由甲、乙兩種物質的溶解度曲線可知,t2℃時,甲的溶解度大于乙,乙的溶解度是60g,甲、乙溶液的溶質質量分數相等均為a%,其中一定是不飽和溶液的是甲,a%的取值范圍是不大于t2℃時乙的飽和溶液的質量分數,即: ![]() ;⑤A、由上述分析可知,將t2℃等質量的甲、乙溶液分別降溫到t1℃,甲的溶解度受溫度的影響較大,甲析出固體的質量多,t1℃時溶質質量:甲<乙,錯誤; B、將t2℃等質量的甲、乙溶液分別降溫到t1℃,甲析出固體的質量多,t1℃時溶劑質量:甲<乙,錯誤;C、將t2℃等質量的甲、乙溶液分別降溫到t1℃,甲析出固體的質量多,t1℃時溶劑質量:甲<乙,t1℃時溶質質量:甲<乙,故t1℃時溶液質量:甲<乙,正確;D、由上述分析可知,將t2℃等質量的甲、乙溶液分別降溫到t1℃,析出晶體質量:甲>乙。正確。
;⑤A、由上述分析可知,將t2℃等質量的甲、乙溶液分別降溫到t1℃,甲的溶解度受溫度的影響較大,甲析出固體的質量多,t1℃時溶質質量:甲<乙,錯誤; B、將t2℃等質量的甲、乙溶液分別降溫到t1℃,甲析出固體的質量多,t1℃時溶劑質量:甲<乙,錯誤;C、將t2℃等質量的甲、乙溶液分別降溫到t1℃,甲析出固體的質量多,t1℃時溶劑質量:甲<乙,t1℃時溶質質量:甲<乙,故t1℃時溶液質量:甲<乙,正確;D、由上述分析可知,將t2℃等質量的甲、乙溶液分別降溫到t1℃,析出晶體質量:甲>乙。正確。


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:初中化學 來源: 題型:
【題目】氫能是理想的清潔能源。以太陽能為熱源,經由鐵氧化合物循環分解水的過程如下:
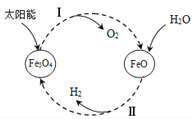
(1)反應Ⅰ的基本反應類型為_____________。
(2)寫出在一定條件下發生的反應Ⅱ的化學方程式_______________。
(3)在上述循環過程中,最終得到的產品是_______________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】煙氣脫硫工藝可實現消除SO2的同時生產新產品(如CaSO4),實現“綠色化學”生產。主要生產流程如下:
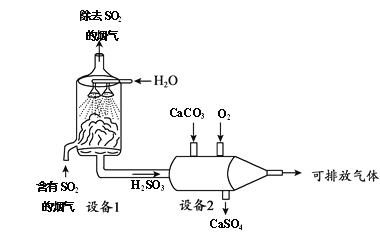
(1)設備1中,通過噴水除去煙氣中的SO2,該反應的化學方程式為____________。
(2)設備2中,發生的化學反應之一為:2CaSO3+O2==2CaSO4,此反應屬于基本類型中的__________________反應。
(3)此生產流程制得的CaSO4中硫元素的化合價為_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】汽車尾氣凈化裝置中裝有鉑催化劑,尾氣在催化劑表面反應的微觀過程可用下圖表示。下列有關說法正確的是
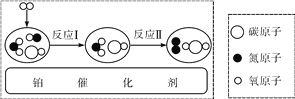
A. 反應Ⅰ中的反應物分子有三種
B. 反應Ⅰ屬于分解反應
C. 反應Ⅱ中參加反應的二氧化氮與一氧化碳的分子個數比為1∶2
D. 此凈化裝置無法消除尾氣中一氧化氮對空氣的污染
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】向1molFe2O3中通入CO并加熱,隨著CO的通入,有關量的變化如下圖,分析正確的是
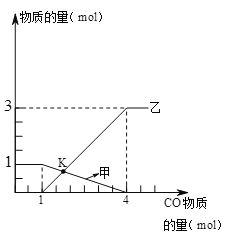
A. 曲線甲表示生成鐵物質的量 B. 曲線乙表示氧化鐵物質的量
C. K點時生成鐵與剩余氧化鐵物質的量相等 D. K點時固體中鐵元素物質的量是2mol
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某同學利用石灰石和稀鹽酸進行如下實驗,操作過程和數據如圖(樣品中雜質不與酸反應也不溶于水)。
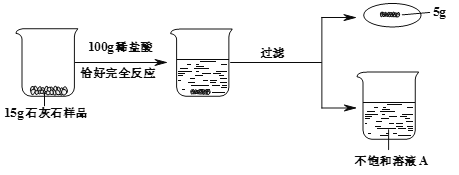
(1)15g石灰石樣品中CaCO3物質的量。
(2)列式計算不飽和溶液A的溶質質量分數(結果準確到0.1%)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】微觀示意圖有助于我們認識化學物質和理解化學反應。
甲是一種比較清潔的燃料,已知甲和乙能在一定條件下反應生成丙和丁。
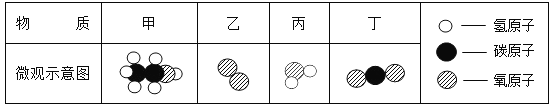
(1)甲、乙、丙、丁中屬于單質的是__________(填序號)。
(2)甲中碳、氫、氧元素的質量比為__________。
(3)在化學反應前后,可能變化的是 __________(填序號)。
a. 原子種類 b. 原子數目 c. 分子數目 d. 元素種類
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在人們擔心化石能源將被耗盡的時候,科學家發現海底埋藏著大量可燃燒的“冰”——“可燃冰”,其中主要含有甲烷水合物,可燃冰將成為未來新能源,但在開采技術上還存在著困難,2017年我國在可燃冰開采技術上有了較大突破。

(1)寫出CH4燃燒的化學方程式________________________________。
(2)可燃冰作為未來新能源,與煤、石油相比其優點是________。(答一點即可)
(3)天然氣作為家用燃枓,有時燃氣灶的火焰出現黃色或橙色,鍋底出現黑色,為避免這種現象的發生,你將如何操作?_______________________
【答案】 CH4+2O2![]() CO2+2H2O 污染小(或熱值大等) 調大燃氣灶的進風口等(合理即可)
CO2+2H2O 污染小(或熱值大等) 調大燃氣灶的進風口等(合理即可)
【解析】(1)根據甲烷燃燒生成二氧化碳和水及化學方程式的書寫方法解答;
(2)根據可燃冰是一種比較理想的燃料分析解答;
(3)根據增大氧氣的濃度或增大可燃物與氧氣的接觸面積,可以促進燃燒分析解答。
解:(1)甲烷燃燒生成二氧化碳和水,反應的化學方程式為:CH4+2O2![]() CO2+2H2O;
CO2+2H2O;
(2)可燃冰作為未來新能源,與煤、石油相比其優點是:同等條件下燃燒產生的熱量比煤和石油多,燃燒后幾乎不產生任何殘渣和廢氣,故填:污染小(或熱值大等);
(3)天然氣作為家用燃枓,有時燃氣灶的火焰出現黃色或橙色,鍋底出現黑色,說明氧氣不足,燃氣燃燒不充分,此時,可將灶具的進風口調大,這樣做的目的是增加進入的空氣的量,使燃氣燃燒更充分。
【題型】簡答題
【結束】
13
【題目】氨氣在化學工業中用途廣泛。合成氨反應的微觀過程如下圖所示,請結合圖示回答問題:

(1)圖中的![]() 屬于___________(填“單質”或“化合物”)。
屬于___________(填“單質”或“化合物”)。
(2)該反應所屬的化學反應基本類型是___________反應。
(3)根據物質變化的微觀圖示,可知化學反應前后肯定發生變化的是______(填序號)。
①元素的種類 ②原子的質量 ③分子的種類 ④原子的數目
(4)工業上常用氨氣來處理有毒氣體NO2,反應原理是8NH3+6NO2 ![]() 7X+12H2O,其中X的化學式是______________。
7X+12H2O,其中X的化學式是______________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲烷(化學式為CH4)不完全燃燒時生成水和其它氧化物。某實驗小組對此展開研究:
①常用___________檢驗生成物中是否含有水②對燃燒產物中的其它氧化物進行探究:(圖中固定試管的儀器已略去)
假設 | 實驗 | 現象 | 結論 |
生成物中有一氧化碳 | 用下圖裝置進行實驗
| A中的現象是 ________ | 生成物中含有一氧化碳。寫出A中的反應化學方程式是______ |
進一步查閱資料,發現CO能溶于銅液(醋酸二氨合銅和氨水的混合液)。因此可在裝置B后再連接下圖裝置D,其目的是______,裝置B、D的連接順序:導管C連接____(填“E”或“F”)。

實驗小組通過裝置B中石灰水變渾濁判斷燃燒產物中一定含有二氧化碳,你覺得該實驗小組的判斷是否正確?若不正確,請設計簡單實驗判斷燃燒產物中是否含有二氧化碳______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com