
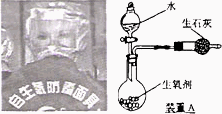
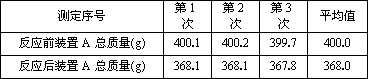
下圖是一種“化學氧自救器”(又稱“自生氧防毒面具”),其使用的生氧劑(主要成分是KO2)的作用原理為:4KO2+2CO2=2K2CO3+3O2某研究小組取100 g生氧劑,放人裝置A中,加入足量水與生氧劑充分反應(化學方程式為:4KO2+2H2O=4KOH+3O2↑),測定反應前后裝置A的總質量,他們進行了三次實驗.測定結果如下:
請根據上述實驗結果計算:(假設雜質不與水反應產生氣體)
(1)100 g生氧劑與足量水反應生成的氧氣質量;
(2)生氧劑中KO2的質量分數;
(3)若成人每分鐘正常需氧量為0.32 g,則能維持成人正常呼吸20分鐘的“化學氧自救器”,至少要裝入這種生氧劑多少克?(注:第(3)小題不必寫出解題過程)
科目:初中化學 來源: 題型:058
(2007
,福建省廈門市,25)下圖是一種“化學氧自救器”(又稱“自生氧防毒面具”),其使用的生氧劑(主要成分是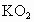 )的作用原理為:
)的作用原理為: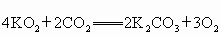
某研究小組取
100g生氧劑,放入裝置A中,加入足量水與生氧劑充分反應(化學方程式為: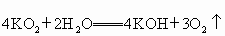 ),測定反應前后裝置A的總質量,他們進行了三次實驗.
),測定反應前后裝置A的總質量,他們進行了三次實驗.

測定結果如下:

請根據上述實驗結果計算:
(假設雜質不與水反應產生氣體)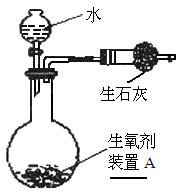
(1)100g
生氧劑與水反應生成的氧氣質量;(2)
生氧劑中含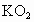 的質量分數;
的質量分數;
(3)
若成人每分鐘正常需氧量約為0.32g,則能維持成人正常呼吸20分鐘的“化學氧自救器”,至少要裝入這種生氧劑多少克?(注:第(3)小題不必寫出解題過程)查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com