
分析 (1)根據題意可以知道鎂已與稀硫酸完全反應,所以根據鎂的質量結合鎂與硫酸反應的化學方程式可以求算出稀硫酸中含有的硫酸的質量,進而結合溶質的質量分數的計算公式可以求算出硫酸溶液中的溶質的質量分數.
(2)根據氧化鎂與硫酸反應的化學方程式可求出生成的硫酸鎂的質量.
解答 解:
(1)鎂與硫酸反應的化學方程式為:Mg+H2SO4═MgSO4+H2↑
設這種硫酸溶液中硫酸的質量為x,
Mg+H2SO4═MgSO4+H2↑
24 98
4.8g x
$\frac{24}{4.8g}=\frac{98}{x}$
x=19.6g
這種硫酸溶液中溶質的質量分數為$\frac{19.6g}{100g}$×100%=19.6%;
(2)氧化美與硫酸反應的化學方程式為:MgO+H2SO4=MgSO4+H2O;
設氧化美與硫酸反應生成的硫酸鎂的質量為z
MgO+H2SO4=MgSO4+H2O
40 120
4g z
$\frac{40}{4g}=\frac{120}{z}$
z=12g
反應后所得溶液的濃度是$\frac{12g}{4g+96g}×$100%=12%
答案:
(1)Mg+H2SO4═MgSO4+H2↑;19.6%;
(2)MgO+H2SO4=MgSO4+H2O;12%;
點評 本題主要考查學生運用化學方程式和溶質質量分數公式進行計算的能力,屬基礎性知識考查題.


 智慧小復習系列答案
智慧小復習系列答案科目:初中化學 來源: 題型:解答題
 以化合價為縱坐標,物質的類別為橫坐標所繪制的圖象叫價類圖.如圖為硫的價類圖,請分析該圖后填空:
以化合價為縱坐標,物質的類別為橫坐標所繪制的圖象叫價類圖.如圖為硫的價類圖,請分析該圖后填空:查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
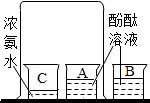
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | $\frac{12×2.6561×1{0}^{-26}}{1.9927×1{0}^{-26}}$kg | |
| B. | $\frac{2.6561×1{0}^{-26}}{1.9927×1{0}^{-26}}$ | |
| C. | $\frac{12×2.6561×1{0}^{-26}}{1.9927×1{0}^{-26}}$ | |
| D. | $\frac{12×1.9927×1{0}^{-26}}{2.6561×1{0}^{-26}}$kg |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
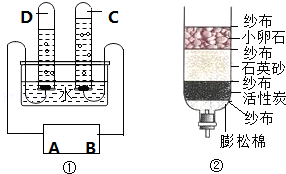 水對于我們的生產和生活都非常重要.根據圖示填寫下列空格.
水對于我們的生產和生活都非常重要.根據圖示填寫下列空格.查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 用濾紙折成蝴蝶并噴灑某種溶液或試劑后,懸掛于鐵架臺上.另取一只盛有某未知溶液的燒杯,放在紙蝴蝶的下方(如圖所示).一段時間后,紙蝴蝶的顏色發生變化,請回答:
用濾紙折成蝴蝶并噴灑某種溶液或試劑后,懸掛于鐵架臺上.另取一只盛有某未知溶液的燒杯,放在紙蝴蝶的下方(如圖所示).一段時間后,紙蝴蝶的顏色發生變化,請回答:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com