解;(1)熟記常見儀器的名稱和用途;
(2)雙氧水是液體,二氧化錳是固體所以不需要加熱;寫方程式要注意一寫二配三注明四等號.用過氧化氫制氧氣時,反應物是過氧化氫,生成物是水和氧氣,配平方法是用觀察法配平,反應條件是二氧化錳作催化劑,氧氣后面標上上升符號;二氧化錳是催化劑,催化劑所起的作用叫做催化作用;由于氧氣密度比空氣大所以用向上排空氣法收集,由于氧氣具有助燃性,能使帶火星的木條復燃,所以驗滿方法是將帶火星的木條放到集氣瓶口,復燃說明滿了;
(3)①根據反應前后各原子個數是不變的,由方程式可知生成物中缺少4個氫,2個氧,因為X的前面系數是2所以X的化學式為:H
2O;
②制取NH
3的反應條件需要加熱,所以選擇有酒精燈的裝置;由于氨氣易溶于水,不能用排水法收集,密度比空氣小用向下排空氣法收集;
(4)氯酸鉀制取氧氣的反應物是氯酸鉀,生成物是氯化鉀和氧氣,用最小公倍數法配平即可,反應條件是二氧化錳作催化劑加熱,氧氣后面標上上升符號;①產生的氧氣的質量是0.075mol×32g/mol=2.4g;②設分解的氯酸鉀物質的量為X則:
2KClO
3
2KCl+3O
2↑
2 3
X 0.075mol
根據:

解得X=0.05mol.
故答案為:(1)酒精燈;長頸漏斗;(2)B;2H
2O
2
2H
2O+O
2↑;催化作用;氧氣的密度比空氣大;將帶火星的木條放到集氣瓶口,復燃說明滿了;(3)①H
2O;②A;D;(4)2KClO
3
2KCl+3O
2↑;2.4;0.05.
分析:(1)熟記常見儀器的名稱;(2)根據反應物的狀態確定發生裝置,根據方程式的寫法寫出反應原理,根據催化劑所起的作用考慮二氧化錳的作用,根據氧氣的性質和密度考慮收集方法和驗滿方法;(3)①根據質量守恒定律考慮化學式寫法;②根據發生裝置和收集裝置的選取方法考慮;(4)根據物質的量、質量、摩爾質量的關系解答本題.
點評:通過回答本題識記了常見儀器的名稱,熟悉了制取氧氣的反應原理,氧氣的驗滿方法,知道了發生裝置和收集裝置的選取方法,了解了物質的質量、物質量、摩爾質量三者的關系.


 CaCl2+2NH3↑+2X.X的化學式為:______.
CaCl2+2NH3↑+2X.X的化學式為:______. 2KCl+3O2↑
2KCl+3O2↑ 解得X=0.05mol.
解得X=0.05mol. 2H2O+O2↑;催化作用;氧氣的密度比空氣大;將帶火星的木條放到集氣瓶口,復燃說明滿了;(3)①H2O;②A;D;(4)2KClO3
2H2O+O2↑;催化作用;氧氣的密度比空氣大;將帶火星的木條放到集氣瓶口,復燃說明滿了;(3)①H2O;②A;D;(4)2KClO3 2KCl+3O2↑;2.4;0.05.
2KCl+3O2↑;2.4;0.05.


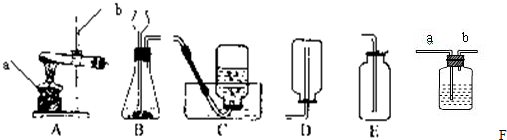

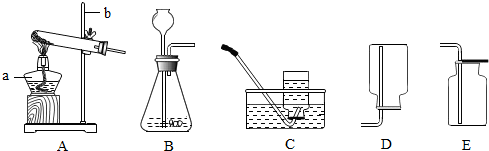
 實驗室常用下列裝置來制取氧氣:
實驗室常用下列裝置來制取氧氣: