
分析 首先正確寫出方程式,然后根據題干內容分析得出反應前后的質量差即為生成二氧化碳氣體的質量,再根據方程式中CaCO3和CO2的質量比求出生成的貝殼樣品中主要物質CaCO3的質量,進一步可求鈣元素的質量,就可以進一步求出貝殼中鈣元素的質量分數.
解答 解:(1)由質量守恒定律可知CO2=25g+200g-216.2g=8.8g;二氧化碳的體積為$\frac{8.8g}{2g/L}$=4.4L;
(2)設碳酸鈣的質量為x,生成氯化鈣的質量為y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}$=$\frac{44}{8.8g}$
x=20g
CaCO3中鈣元素的質量20g×$\frac{40}{100}$×100%=8g
貝殼中鈣元素的質量分數$\frac{8g}{25g}$×100%=32%
答:(1)二氧化碳的體積為4.4L;
(2)貝殼中鈣元素的質量分數32%;
點評 根據化學方程式進行計算時,只能使用純凈物的質量進行計算,而不能把混合物的質量直接代入化學方程式進行計算,質量守恒定律在計算中的運用是化學計算的一個常見內容,一般的規律是依據質量的變化求出某一生成的質量,再結合反應方程式分析解答.


科目:初中化學 來源: 題型:選擇題
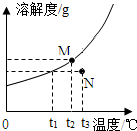 如圖為X物質的溶解度曲線,M,N兩點分別表示X物質溶于100g水中所形成的兩種溶液.下列做法不能實現M,N間的相互轉化的是(X從溶液中析出時不帶結晶水)( )
如圖為X物質的溶解度曲線,M,N兩點分別表示X物質溶于100g水中所形成的兩種溶液.下列做法不能實現M,N間的相互轉化的是(X從溶液中析出時不帶結晶水)( )| A. | 從M→N:先將M降溫到t1過濾后再將其升溫至t3 | |
| B. | 從M→N:先將M恒溫蒸發掉適量的水再升溫到t3 | |
| C. | 從N→M:先向N中加入適量的固體X再降溫到t2 | |
| D. | 從N→M:先將N降溫到t2再加入適量固體X |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | ①③④⑤ | B. | ①②⑤⑥ | C. | ③⑤⑥⑦ | D. | ①④⑤ |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 實驗室有半瓶敞口放置的標簽殘缺的白色固體(標簽如圖),小明、小亮根據初中所學的知識進行下列探究.
實驗室有半瓶敞口放置的標簽殘缺的白色固體(標簽如圖),小明、小亮根據初中所學的知識進行下列探究.| 實驗步驟 | 實驗現象 | 結論 |
| A.取少量濾液加入過量的BaCl2溶液 | 產生白色沉淀 | 一定有Na2CO3 |
| B.將A中的混合物過濾,向濾液中加酚酞試液 | 溶液變成紅色 | 一定有NaOH |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氧氣、純堿、空氣 | B. | 氫氣、硫酸、石灰水 | ||
| C. | 水、燒堿、生鐵 | D. | 銅絲、熟石灰、石油 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
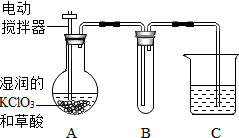 世界環保聯盟建設全面禁止用氯氣(常溫下是一種黃綠色有毒氣體)對飲用水消毒,推廣使用安全、高效殺菌消毒劑ClO2.ClO2是一種黃綠色,有刺激性氣味的氣體,冷卻至11.0℃以下時變成紅色液體,易溶于水,見光易分解,易與堿反應,殺菌、漂白能力均優于氯氣.
世界環保聯盟建設全面禁止用氯氣(常溫下是一種黃綠色有毒氣體)對飲用水消毒,推廣使用安全、高效殺菌消毒劑ClO2.ClO2是一種黃綠色,有刺激性氣味的氣體,冷卻至11.0℃以下時變成紅色液體,易溶于水,見光易分解,易與堿反應,殺菌、漂白能力均優于氯氣.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com