
【題目】下列說法正確的是
A. 等質量的鎂與氧化鎂混合,其混合物中鎂、氧兩種元素的質量比為![]()
B. 等質量的![]() 和
和![]() 分別與足量稀硫酸充分反應,生成
分別與足量稀硫酸充分反應,生成![]() 的質量相等
的質量相等
C. 質量和質量分數均相等的氫氧化鋇溶液和稀硝酸,充分反應后,向所得溶液中滴加硫酸銅溶液,會出現藍色沉淀
D. 將一定量的氫氧化鈉和氫氧化鈣的混合物溶于足量水中,再向溶液中加入過量的碳酸鈉溶液,充分反應后,生成的沉淀質量與原混合物的質量相等,則原混合物中氫氧化鈉的質量分數為![]()
【答案】AD
【解析】
A、設鎂與氧化鎂的質量均為a,氧化鎂中鎂元素的質量為![]() ;
;
氧化鎂中氧元素的質量為![]() ,所以混合物中鎂元素的總質量為a+
,所以混合物中鎂元素的總質量為a+![]() ,
,
鎂、氧兩種元素的質量比為(a+![]() ):
):![]() =4:1,故正確;
=4:1,故正確;
B、Zn、Fe分別與稀硫酸反應的關系式為:
![]()
![]()
由于稀硫酸足量,故產生氫氣的質量由金屬決定,每65分質量的Zn產生2分質量的H2,每56分質量的Fe產生2分質量的H2,所以,等質量的Zn與Fe分別與足量稀硫酸充分反應,生成![]() 的質量不相等,故錯誤;
的質量不相等,故錯誤;
C、氫氧化鋇與硝酸的反應關系式如下:
![]()
可見質量和質量分數均相等的氫氧化鋇溶液和稀硝酸,充分反應后硝酸有剩余,滴加硫酸銅溶液,不會出現藍色沉淀,故錯誤;
D、氫氧化鈣與碳酸鈉反應的關系式如下:
![]()
每生成100份質量的碳酸鈣,需要氫氧化鈣74份質量,由于生成的沉淀質量與原混合物的質量相等,故氫氧化鈉占26份質量,則原混合物中氫氧化鈉的質量分數為![]() ,故正確。
,故正確。
故選AD。


科目:初中化學 來源: 題型:
【題目】隨著人們生活水平的提高,哈爾濱市私家車數量不斷增加,給人們出行帶來很多方便。請回答下列問題:

(1)汽車表面噴漆主要是為了防銹,其原理是_____;
(2)金屬鐵是從鐵礦石中提煉出來的,請寫出高爐中用赤鐵礦煉鐵的主要反應的化學方程式①_____。其中反應前鐵元素的化合價是②_____價,該反應的反應類型為③_____反應。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】晶體硅是一種重要的非金屬材料。制備純硅的主要步驟如下:
①高溫下用碳還原二氧化硅制得粗硅,同時得到一種可燃性氣體。
②粗硅與干燥HCl氣體反應制得SiHCl3:Si+3HCl![]() SiHCl3+H2
SiHCl3+H2
③SiHCl3與過量H2在1000~1100℃反應制得純硅。
已知SiHCl3能與H2O強烈反應,在空氣中易自燃。
請回答下列問題:
(1)第①步制備粗硅的化學反應方程式為_____。
(2)粗硅與HCl反應完全后,經冷凝得到的SiHCl3(沸點33.0℃)中含有少量SiCl4(沸點57.6℃)和HCl(沸點-84.7℃),提純SiHCl3采用的方法為:_____。
(3)用SiHCl3與過量H2反應制備純硅的裝置如下(熱源及夾持裝置略去):
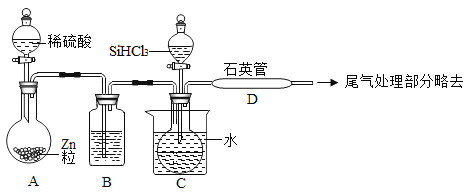
①裝置B中的試劑是_____,裝置C中的燒瓶需要加熱,其目的是:_____。
②裝置D不能采用普通玻璃管的原因是_____,裝置D中發生反應的化學方程式為_____。
③為保證制備純硅實驗的成功,操作的關鍵是檢查實驗裝置的氣密性,控制好反應溫度以及_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知草酸(H2C2O4)固體與濃硫酸共熱發生化學反應:H2C2O4![]() CO2↑+CO↑+H2O.某化學興趣小組設計如下實驗裝置,用于制取純凈干燥的CO氣體來還原氧化鐵。請根據題目要求回答下列問題:
CO2↑+CO↑+H2O.某化學興趣小組設計如下實驗裝置,用于制取純凈干燥的CO氣體來還原氧化鐵。請根據題目要求回答下列問題:

(1)按裝置圖組裝好實驗儀器,實驗前必須要_____,點燃E處酒精燈前必須_____。
(2)裝置B中的試劑是_____溶液,反應的化學方程式為_____;裝置C中所盛的液體是_____,其作用是_____;
(3)E裝置玻璃管中觀察到的現象是_____,反應的化學方程式為_____;
(4)A裝置中連通管的作用是_____;
(5)F裝置的作用是_____、_____(只答二條即可);
(6)利用這套裝置還可以測定氧化鐵樣品中氧化鐵的質量分數。某同學的測定方法是:稱量氧化鐵樣品10.0 g,E裝置中玻璃管與樣品的總質量為80.0 g,完全反應并冷卻后再稱量E裝置中玻璃管與剩余固體的總質量為78.2 g.由該實驗可計算出氧化鐵樣品中氧化鐵的質量分數為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室制備氣體,結合以下裝置回答問題:
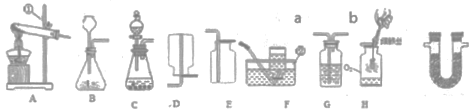
(1)寫出標號儀器名稱①_____②_____。
(2)請寫出用裝置A制取氧氣的化學反應方程式_____;
(3)如果要想得到平穩的二氧化碳氣流,應該選用的制取裝置為_____實驗室制取二氧化碳的化學方程式為_____;若在![]() 裝置中裝滿水,收集氫氣時應該從那端通入_____(填“a”或“b”)
裝置中裝滿水,收集氫氣時應該從那端通入_____(填“a”或“b”)
(4)做鐵絲燃燒實驗時,需要用較純凈的氧氣則選用的氣體收集裝置為_____,在裝置中留少量水的目的是_____。
(5)實驗完畢,清洗儀器,洗過的玻璃儀器內壁附著的水_____時,表明儀器已洗干凈
(6)實驗室常用氯化銨固體和熟石灰固體混合加熱制取極易溶于水的氨氣。請根據以上裝置圖選擇,在實驗室制取氨氣時的發生裝置和收集裝置為_____(填字母代號),若要制取干燥的氨氣,![]() 形管中應加入_____干燥劑。
形管中應加入_____干燥劑。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某實驗室欲配制一定溶質質量分數的![]() 溶液,現實驗室只有含少量
溶液,現實驗室只有含少量![]() 的
的![]() 固體藥品.
固體藥品.
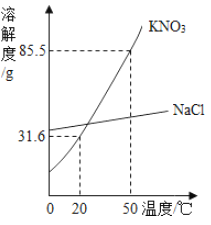
(1)如圖所示為![]() 和
和![]() 的溶解度曲線,50℃時,將85.5g固體藥品溶于100g水中,得到的是
的溶解度曲線,50℃時,將85.5g固體藥品溶于100g水中,得到的是![]() ______的溶液(填“飽和”或“不飽和”).
______的溶液(填“飽和”或“不飽和”).
(2)將![]() 提純的方法是______.
提純的方法是______.
(3)小明用提純后的![]() 固體配制100g溶質質量分數為5%的
固體配制100g溶質質量分數為5%的![]() 溶液,其操作步驟是:計算、_____、量取、溶解.經檢測,小明所配溶液中
溶液,其操作步驟是:計算、_____、量取、溶解.經檢測,小明所配溶液中![]() 溶質質量分數偏小,其原因可能是______.
溶質質量分數偏小,其原因可能是______.
①![]() 固體仍然不純; ②溶解前,燒杯中有水;
固體仍然不純; ②溶解前,燒杯中有水;
③量取水時,俯視讀數; ④裝瓶時,有少量溶液灑出.
(4)將所配制的硝酸鉀溶液的溶質質量分數變為3%,需加入溶質質量分數為1%的硝酸鉀溶液______g。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】水是生命之源,也是工農業生產不可缺少的物質。合理利用和保護水資源是我們義不容辭的責任。
(1)下列做法不合理的是______(填序號)。
①嚴格監管化肥和農藥的使用 ②積極探索污水處理的新技術 ③不間斷地放水洗衣服
(2)利用右圖所示的簡易裝置可把海水轉化為淡水。下列說法錯誤的是______(填序號)。
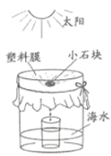
A.小容器中的水為淡水 B.大容器中得到的溶液一定是氯化鈉的飽和溶液
C.獲得淡水的快慢與溫度有關
(3)市售“自熱米飯”的自加熱原理:飯盒夾層中的水與生石灰接觸,反應放出大量熱。該反應的化學方程式為_________。
(4)自來水廠生產自來水的過程中,常加入_______,用來吸附水中一些溶解性的雜質,除去臭味。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】中國首位諾貝爾醫學獎獲得者屠呦呦繼發現青蒿素后又發明了雙氫青蒿素.圖示是雙氫青蒿素片的部分說明,請回答:

(1)雙氫青蒿素中C:H:O的原子個數比為_____;
(2)雙氫青蒿素分子的相對分子質量為_____;
(3)雙氫青蒿素中H:O元素的質量比為_____;
(4)雙氫青蒿素中所含碳元素的質量分數為_____;
(5)3片雙氫青蒿素所含碳元素的質量為_____mg。(計算結果精確到0.1mg)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com