
【題目】銅、鐵是人類使用最早、應用廣泛的金屬.
(一)對古代制品的認識
青銅鑄件、絲綢織品、陶瓷器皿是我國古代勞動人民創造的輝煌成就.
(1)上述制品不涉及到的材料是______(選填序號).
A、金屬材料 B、無機非金屬材料 C、復合材料
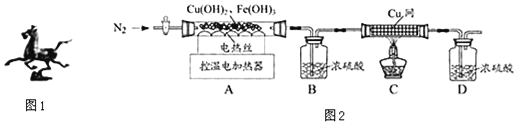
(2)如圖1為出土文物古代青銅鑄件“馬踏飛燕”.該文物能保存至今的原因可能是_____(選填序號).
A、銅的活潑性弱 B、銅不會生銹 C、深埋于地下,隔絕空氣
(二)鐵、銅的冶煉
①我國古代曾用孔雀石煉銅,涉及主要反應的化學方程式:_________,2CuO+C![]() 2Cu+CO2↑.
2Cu+CO2↑.
②鐵、銅礦石有赤鐵礦(Fe2O3)、磁鐵礦(Fe3O4)、黃鐵礦(FeS2)、黃銅礦(CuFeS2)等.CuFeS2為二硫化亞鐵銅,其中S元素的化合價為______.
(1)工業煉鐵大多采用赤鐵礦、磁鐵礦.以磁鐵礦為原料煉鐵反應的化學方程式為______________.
煉鐵不采用黃鐵礦、黃銅礦,可能的原因是:
①黃鐵礦、黃銅礦含鐵量相對低;②________________________________.
(2)以黃銅礦為原料,采用生物煉銅是現代煉銅的新工藝,原理為:4CuFeS2+17O2+2H2SO4![]() 4CuSO4+2Fe2(SO4)3+2H2O.
4CuSO4+2Fe2(SO4)3+2H2O.
向上述反應后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①發生主要反應的化學方程式:Fe+Fe2(SO4)3=3FeSO4,________________________.
②FeSO4溶液經蒸發濃縮、___________、過濾等操作得到FeSO47H2O晶體.
(三)黃銅礦中鐵、銅含量的測定
在科研人員指導下,興趣小組稱取25.00g黃銅礦(含少量Fe2O3和其它不含金屬元素的雜質)模擬生物煉銅,使其全部轉化為CuSO4、Fe2(SO4)3溶液.向溶液中加入過量NaOH溶液得到Cu(OH)2、Fe(OH)3固體.
(1)證明NaOH溶液過量的方法:靜置,向上層清液中滴加________溶液,無現象.
(2)用圖2裝置對固體進行熱分解實驗.
【資料】
①在68℃時,Cu(OH)2分解為CuO;在500℃時,Fe(OH)3分解為Fe2O3.
②在1400℃時,CuO分解為Cu2O和O2,Fe2O3分解為復雜的鐵的氧化物和O2.
(1)裝配好實驗裝置后,先要________________.
(2)停止加熱后仍需繼續通N2,可防止倒吸和______________________________.
(3)控制不同的溫度對A中固體加熱,測得裝置B和C中銅網的質量變化如表.
溫度/℃ | 室溫 | 100 | 550 | 1400 |
B裝置/g | 200.00 | 201.80 | 205.04 | 205.04 |
C中銅網/g | 100.00 | 100.00 | 100.00 | 101.28 |
①此黃銅礦中銅、鐵元素的質量分數:ω(Cu)%=________;ω(Fe)%=__________.
②復雜的鐵的氧化物化學式為__________.
【答案】 C AC Cu2(OH)2CO3![]() H2O+CO2↑+2CuO ﹣2 Fe3O4+4CO
H2O+CO2↑+2CuO ﹣2 Fe3O4+4CO![]() 3Fe+4CO2 冶煉過程中會產生有毒氣體二氧化硫,污染環境 Fe+CuSO4=Cu+FeSO4 降溫結晶 NaOH 檢查裝置的氣密性 使生成的氣體全部被B和C裝置吸收 25.60% 26.88% Fe4O5
3Fe+4CO2 冶煉過程中會產生有毒氣體二氧化硫,污染環境 Fe+CuSO4=Cu+FeSO4 降溫結晶 NaOH 檢查裝置的氣密性 使生成的氣體全部被B和C裝置吸收 25.60% 26.88% Fe4O5
【解析】(一)(1)青銅是合金,屬于金屬材料;絲綢屬于天然材料;陶瓷屬于無機非金屬材料;(2)銅的活動性弱,且深埋于地下隔絕了空氣,所以青銅器不易生銹;(二)①堿式碳酸銅受熱分解生成氧化銅、二氧化碳和水,反應的化學方程式為:Cu2(OH)2CO3![]() H2O+CO2↑+2CuO;②CuFeS2為二硫化亞鐵銅,其中銅元素顯+2價,鐵元素顯+2價,設硫元素的化合價為x,則(+2)+(+2)+2x=0,x=-2;(1)工業上用CO和磁鐵礦煉鐵,主要是利用CO的還原性,在高溫下和氧化鐵反應生成鐵和二氧化碳,反應的化學方程式為Fe3O4+4CO
H2O+CO2↑+2CuO;②CuFeS2為二硫化亞鐵銅,其中銅元素顯+2價,鐵元素顯+2價,設硫元素的化合價為x,則(+2)+(+2)+2x=0,x=-2;(1)工業上用CO和磁鐵礦煉鐵,主要是利用CO的還原性,在高溫下和氧化鐵反應生成鐵和二氧化碳,反應的化學方程式為Fe3O4+4CO![]() 3Fe+4CO2;②黃鐵礦、黃銅礦含鐵量低,含有對環境有害的元素硫,并且在冶煉過程中會產生有毒氣體二氧化硫,污染環境,因此黃鐵礦、黃銅礦不宜煉鐵;(2)①加入的鐵粉能與硫酸銅反應生成銅和硫酸亞鐵,反應的化學方程式: Fe+CuSO4=Cu+FeSO4;②FeSO4溶液經蒸發濃縮、降溫結晶、過濾等操作得到FeSO47H2O晶體;(三)(1)可以向上層清液中滴加氫氧化鈉溶液,若產生沉淀則氫氧化鈉的量不足,若沒有沉淀產生則氫氧化鈉已經過量;【資料】(1)對于有氣體生成的反應,在實驗前,一定要檢查裝置的氣密性; (2)為了使得生成水蒸氣、氧氣被完全吸收,所以停止加熱后仍需繼續通N2,使生成的氣體全部被B和C裝置吸收;(3)①設其中銅元素的質量為x.氫氧化銅受熱會分解為氧化銅和水,方程式為Cu(OH)2
3Fe+4CO2;②黃鐵礦、黃銅礦含鐵量低,含有對環境有害的元素硫,并且在冶煉過程中會產生有毒氣體二氧化硫,污染環境,因此黃鐵礦、黃銅礦不宜煉鐵;(2)①加入的鐵粉能與硫酸銅反應生成銅和硫酸亞鐵,反應的化學方程式: Fe+CuSO4=Cu+FeSO4;②FeSO4溶液經蒸發濃縮、降溫結晶、過濾等操作得到FeSO47H2O晶體;(三)(1)可以向上層清液中滴加氫氧化鈉溶液,若產生沉淀則氫氧化鈉的量不足,若沒有沉淀產生則氫氧化鈉已經過量;【資料】(1)對于有氣體生成的反應,在實驗前,一定要檢查裝置的氣密性; (2)為了使得生成水蒸氣、氧氣被完全吸收,所以停止加熱后仍需繼續通N2,使生成的氣體全部被B和C裝置吸收;(3)①設其中銅元素的質量為x.氫氧化銅受熱會分解為氧化銅和水,方程式為Cu(OH)2 ![]() CuO+H2O,從室溫加熱到100℃時,裝置B中增重的質量為氫氧化銅分解生成水的質量位x;由題干信息可知,經過一系列化學反應時,物質的關系是:
CuO+H2O,從室溫加熱到100℃時,裝置B中增重的質量為氫氧化銅分解生成水的質量位x;由題干信息可知,經過一系列化學反應時,物質的關系是:
Cu~CuFeS2~CuSO4~Cu(OH)2~H2O
64 18
x (201.80-200.00)g
![]()
x=6.4g,
則此黃銅礦中銅元素的質量分數:ω(Cu)%=![]() ×100%=25.60%;
×100%=25.60%;
設其中鐵元素的質量為y,氫氧化鐵受熱會分解為氧化鐵和水,方程式為2Fe(OH)3 ![]() Fe2O3+3H2O,從100℃加熱到550℃時,裝置B中增重的質量為氫氧化鐵分解生成水的質量;由題干信息可知,經過一系列化學反應時,物質的關系是:
Fe2O3+3H2O,從100℃加熱到550℃時,裝置B中增重的質量為氫氧化鐵分解生成水的質量;由題干信息可知,經過一系列化學反應時,物質的關系是:
2Fe~2CuFeS2~Fe2(SO4)3~Fe(OH)3~3H2O
112 54
y (205.04-201.80)g
![]()
y=6.72g
則此黃銅礦中鐵元素的質量分數:ω(Fe)%=![]() ×100%=26.88%;
×100%=26.88%;
②氧化銅受熱分解的方程式為:4CuO![]() Cu2O+O2↑
Cu2O+O2↑
設氧化銅分解生成氧氣的質量為z,則
4Cu~4CuO~2Cu2O~O
256 32
6.4g z
![]()
z=0.8g,
因為裝置C增重的質量為氧化銅、氧化鐵分解產生氧氣的總質量,所以氧化鐵分解生成氧氣的質量為:(101.28g-100.00g-0.8g)=0.48g;氧化鐵的質量為:6.72g÷112160×100%=9.6g;
生成的復雜鐵的氧化物中含氧元素的質量為:9.6g-0.48g-6.72g=2.4g;
復雜的鐵的氧化物中鐵原子與氧原子的個數比為:6.72g56:2.4g16=4:5;
則復雜的鐵的氧化物化學式為:Fe4O5。


 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:初中化學 來源: 題型:
【題目】為測定某鐵合金樣品(除鐵外,其余成分不溶于水,且不參與任何反應)中單質鐵的含量,小冰同學進行實驗如下:

請回答下列問題:
(1)上述實驗過程中發生反應的化學方程式為_____;
(2)樣品中單質鐵的質量分數為_____;
(3)根據已知條件列出求解加入的稀硫酸中溶質質量(x)的比例式為_____;
(4)最終所得到的不飽和溶液中溶質的質量分數為_____;
(5)若用含氧化鐵80%的赤鐵礦煉出上述實驗中所需要的鐵合金160t,則理論上需要赤鐵礦的質量為_____.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學就在我們身邊,人類的衣、食、住、行都離不開化學。
(1)在廚房里蘊藏著許多化學知識。
①下列食物中,能提供大量維生素的是________________(填字母)。
②加鐵醬油中的“鐵”是指______(填“元素”或“原子”), 身體缺鐵會引起貧血。
③廚房中能用來除水垢的物質是____________。
④為防止菜刀生銹,可采用的一種措施是__________。
(2)汽車、高鐵、飛機等已成為人們出行的常用交通工具。
①汽油是汽車常用的一種燃料。將石油加熱,利用各成分的沸點不同將它們分離可得到汽油,該過程屬于______變化。汽車的鉛蓄電池工作時,發生如下化學反應:Pb+bO2+2H2SO4=2PbSO4+2H2O該反應涉及的物質中屬于氧化物的有__________。
②高鐵車頭的玻璃是用無機玻璃、樹脂、塑料等粘合而成,能耐受強大的撞擊力,這種玻璃屬于___________(填字母)。
A.復合材料 B.合成材料 C.金屬材料·
③制造飛機使用了硬鋁(鋁銅鎂硅合金),其中鎂元素的某種粒子結構示意圖為![]() ,鎂原子的最外層電子數是___________。
,鎂原子的最外層電子數是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖為A、B、C三種物質的溶解度曲線,試回答:
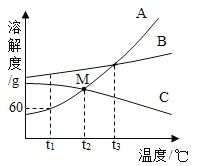
(1)t1℃時A、B、C三種物質的溶解度大小關系是________;。
(2)M點的含義是___________;
(3)t1℃時將40gA物質加入到50g水中充分攪拌,形成溶液的溶質質量分數是___________。
(4)將t3℃時A、B、C三種物質的飽和溶液降溫到t1℃,所得溶液的溶質質量分數大小關系是______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知:Cu2O+H2SO4═Cu+CuSO4+H2O.16.0g CuO與CO反應得到Cu、Cu2O混合物13.6g,將此混合物溶于足量的100.0g稀H2SO4得9.6gCu.下列說法正確的是( )
A. 生成2.4g CO2
B. 混合物中含9.6g銅元素
C. 混合物中Cu與Cu2O的質量之比為8:9
D. 反應后溶液中CuSO4的質量分數約為7.0%
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】用化學符號表示:
(1)兩個氦原子 _____
(2)3個氯分子 _____
(3)硝酸根離子 _____
(4)+2價的鎂元素 _____
(5)硫酸鋁 _____
(6)氯化亞鐵 _____
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】益陽市桃江縣硫鐵礦廠開采的黃鐵礦(主要成分是FeS2),是生產H2SO4的重要原料.利用黃鐵礦生產H2SO4的第一步反應為:4FeS2+11O2═2Fe2O3+8X.所得產物Fe2O3是冶煉鐵的重要原料.回答下列問題:
(1)已知FeS2中Fe的化合價為+2,則S的化合價為________.
(2)X的化學式是_________.
(3)寫出高爐中Fe2O3轉化成鐵的化學方程式__________________________.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知在常溫下A為液體,B、C、F是氣體; 其中C是最輕的氣體,F是造成溫室效應的主要氣體;G為黑色固體單質,H是白色不溶于水的固體,它們之間的轉變關系如圖,請回答下列問題:
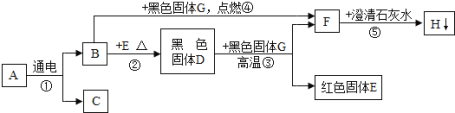
(1)寫出有關物質的化學式:C是 ;G是 ;H是 。
(2)寫出反應②的化學方程式 ,該反應的基本反應類型是 。
(3)寫出反應③的化學方程式: 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列觀點符合質量守恒定律的是
A.某物質在空氣中燃燒只生成CO2和H2O,則該物質一定含有碳、氫、氧元素
B.一定條件下,CO和O2生成CO2,反應前后分子總數不變
C.1gH2和1g O2完全反應后生成2g H2O
D.石灰石與適量鹽酸反應后,固體的質量減輕了
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com