
 ×100%,進行分析解答.
×100%,進行分析解答.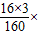 100%=30%、
100%=30%、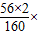 100%=70%.
100%=70%.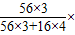 100%=x×70%,x=48g.
100%=x×70%,x=48g.

 超能學典應用題題卡系列答案
超能學典應用題題卡系列答案科目:初中化學 來源:不詳 題型:單選題
| A.兩個氧分子:O2 |
| B.水通電得到氧氣的化學方程式是2H2O=O2↑+2H2↑ |
| C.CO2中氧元素的化合價為+2價 |
| D.氫氧化鐵的化學式:Fe(OH)3 |
查看答案和解析>>
科目:初中化學 來源:2011-2012學年江蘇省常州市西藏民族中學九年級(上)期中化學試卷(解析版) 題型:選擇題
查看答案和解析>>
科目:初中化學 來源:2011-2012學年云南省昭通市魯甸縣茨院中學九年級(上)期末化學試卷(解析版) 題型:選擇題
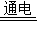 O2↑+2H2↑
O2↑+2H2↑查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com