
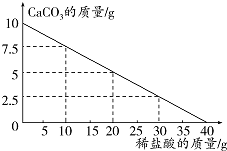
 向10g碳酸鈣中不斷加入稀鹽酸,其質量變化如圖所示.請計算:
向10g碳酸鈣中不斷加入稀鹽酸,其質量變化如圖所示.請計算:分析 (1)由圖象可知:當CaCO3質量為0時,即為鹽酸與CaCO3恰好完全反應的時刻,此時所用稀鹽酸的量即是所消耗的稀鹽酸,故10g CaCO3完全反應時,所加稀鹽酸的質量為40g.
(2)根據碳酸鈣與鹽酸反應的化學方程式,由碳酸鈣的質量科求出生成的氯化鈣、二氧化碳的質量,再根據溶質的質量分數計算公式計算.
解答 解:(1)如圖象所示:當10gCaCO3恰好完全反應時,所加稀鹽酸的質量40g;
(2)設生成氯化鈣的質量為x,生成二氧化碳的質量為y
2HCl+CaCO3=CaCl2+H2O+CO2↑
100 111 44
10g x y
$\frac{100}{10g}=\frac{111}{x}=\frac{44}{y}$
x=11.1g
y=4.4g
恰好完全反應后所得溶液中的溶質質量分數為:$\frac{11.1g}{10g+40g-4.4g}×$100%≈24.3%
答案:
(1)40;
(2)恰好完全反應后所得溶液中的溶質質量分數為:24.3%.
點評 本題考查內容簡單注重基礎,熟練掌握有關化學方程式的計算,以及溶質質量分數的計算是解題關鍵.


 互動課堂系列答案
互動課堂系列答案 激活思維智能訓練課時導學練系列答案
激活思維智能訓練課時導學練系列答案科目:初中化學 來源: 題型:選擇題
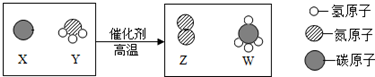
| A. | 化學反應前后原子的種類、數目、質量均保持不變 | |
| B. | W物質中碳元素的質量分數為75% | |
| C. | 參加反應的X、Y兩物質的粒子個數比為3:4 | |
| D. | 反應前后各元素的化合價均不變 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
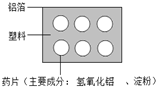 《奔跑吧 兄弟》是一檔熱播的娛樂節目,其中蘊含著許多化學知識.
《奔跑吧 兄弟》是一檔熱播的娛樂節目,其中蘊含著許多化學知識.查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 某化學興趣小組利用如圖所示的改進裝置測定空氣中氧氣的體積分數.關于該實驗有下列說法:
某化學興趣小組利用如圖所示的改進裝置測定空氣中氧氣的體積分數.關于該實驗有下列說法:| A. | ①②③④ | B. | ②③④⑤ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氣態時密度比空氣大 | B. | 沸點較低,容易氣化 | ||
| C. | 不支持燃燒 | D. | 可燃性 |
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
 右圖中A~G均是初中化學常見物質,它們之間的轉化或相互反應關系均為初中常見反應,其中G屬于單質,且被稱為最理想能源,其余均為化合物,B是胃酸的主要成分,B和C物質類別相同,D是常用的食品干燥劑,E溶于水所得溶液的pH大于7.圖中“-”表示兩端的物質能發生化學反應,“→”表示物質間存在轉化關系,反應條件、部分反應物和生成物已略去.
右圖中A~G均是初中化學常見物質,它們之間的轉化或相互反應關系均為初中常見反應,其中G屬于單質,且被稱為最理想能源,其余均為化合物,B是胃酸的主要成分,B和C物質類別相同,D是常用的食品干燥劑,E溶于水所得溶液的pH大于7.圖中“-”表示兩端的物質能發生化學反應,“→”表示物質間存在轉化關系,反應條件、部分反應物和生成物已略去.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com