
| 序號 | 反應前A的質量 | 反應前B的質量 | 反應后A3B2的質量 |
| ① | 8g | 2g | 6g |
| ② | 4g | 6g | 6g |
| ③ | xg | yg | 9g |
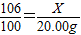 x=21.2g
x=21.2g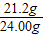 ×100%=88.3%.
×100%=88.3%.

科目:初中化學 來源: 題型:閱讀理解
| 序號 | 反應前A的質量 | 反應前B的質量 | 反應后A3B2的質量 |
| ① | 8g | 2g | 6g |
| ② | 4g | 6g | 6g |
| ③ | xg | yg | 9g |
查看答案和解析>>
科目:初中化學 來源: 題型:
 化學中質量守恒定律是一個非常重要的定量定律.右圖為托盤天平,使用托盤天平稱物品的正確操作順序為(填序號)
化學中質量守恒定律是一個非常重要的定量定律.右圖為托盤天平,使用托盤天平稱物品的正確操作順序為(填序號)查看答案和解析>>
科目:初中化學 來源: 題型:
 化學中質量守恒定律是一個非常重要的定量定律.
化學中質量守恒定律是一個非常重要的定量定律.
| ||
| △ |
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
 化學中質量守恒定律是一個非常重要的定量定律。
化學中質量守恒定律是一個非常重要的定量定律。
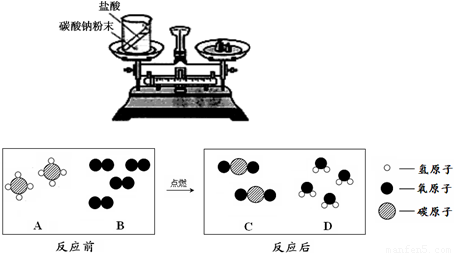
(1)如右圖裝置中,稱量小燒杯中所有物質的質量m1,然
后將小燒杯中的碳酸鈉與鹽酸完全混合,反應發生一
段時間后,再稱量小燒杯及燒瓶內物質的總質量為
m2,則(填“=” “>”“<”)m1 m2 ,其原
因為 。
(2)天然氣的主要成分是甲烷(CH4),可直接用作氣體燃
料。燃燒反應前后分子種類變化的微觀示意圖如下所示。

①1個B分子中含有 個原子。
②四種物質中屬于化合物的是 (填圖中字母)。
(3)A和B可發生如下反應:3A+2B=A3B2,某學生做了3次該實驗(每次均充分反應),反應前A和B的質量 和都是l0g。有關實驗數據見下表:
序號 反應前A的質量 反應前B的質量 反應后A3B2的質量
① 8g 2g 6g
② 4g 6g 6g
③ xg yg 9g
X∶Y的比值可能為 或 。
(4)為了測定某品牌食用純堿中碳酸鈉的質量分數,某校化學研究性學習小組的探究過程如下:
【提出問題】樣品中碳酸鈉的質量分數是多少?
【知識準備】食用純堿的主要成分是碳酸鈉,另外還含有少量的氯化鈉;反應過程中不考慮水和氯化氫的揮發。
【設計方案】(1)方案一:向一定量樣品中加入過量澄清石灰水,根據反應生成碳酸鈣的質量,先求出碳酸鈉的質量,再計算樣品中碳酸鈉的質量分數。
(2)方案二:向一定量樣品中加入足量的稀鹽酸,根據反應生成二氧化碳的質量,先求出碳酸鈉的質量,再計算樣品中碳酸鈉的質量分數。
【進行實驗】甲組同學:稱取24.00g樣品,加水配成溶液,在溶液中加入過量的澄清石灰水。過濾、洗滌、干燥,共得到白色沉淀20.00g。
乙組同學:稱取24.00g樣品,加入足量的稀鹽酸直到反應停止,共收集到8.80g二氧化碳。
【解決問題】請你任選一組同學的實驗結果,幫助他們計算出樣品中碳酸鈉的質量分數。(寫出計算過程。計算結果精確到0.1% )
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
化學中質量守恒定律是一個非常重要的定量定律。
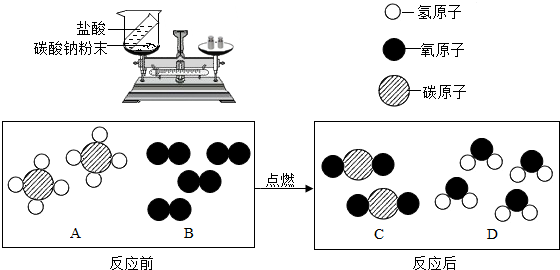
(1)如右圖裝置中,稱量小燒杯中所有物質的質量m1,然后將小燒杯中的碳酸鈉與鹽酸完全混合,反應發生一段時間后,再稱量小燒杯及燒瓶內物質的總質量為 m2,則(填“=” “>”“<”)m1 m2 ,其原因為 。

(2)天然氣的主要成分是甲烷(CH4),可直接用作氣體燃
料。燃燒反應前后分子種類變化的微觀示意圖如下所示。

①1個B分子中含有 個原子。
②四種物質中屬于化合物的是 (填圖中字母)。
(3)A和B可發生如下反應:3A+2B=A3B2,某學生做了3次該實驗(每次均充分反應),反應前A和B的質量![]() 和都是l0g。有關實驗數據見下表:
和都是l0g。有關實驗數據見下表:
| 序號 | 反應前A的質量 | 反應前B的質量 | 反應后A3B2的質量 |
| ① | 8g | 2g | 6g |
| ② | 4g | 6g | 6g |
| ③ | xg | yg | 9g |
X∶Y的比值可能為 或 。
(4)為了測定某品牌食用純堿中碳酸鈉的質量分數,某校化學研究性學習小組的探究過程如
下:
【提出問題】樣品中碳酸鈉的質量分數是多少?
【知識準備】食用純堿的主要成分是碳酸鈉,另外還含有少量的氯化鈉;反應過程中不考慮水和氯化氫的揮發。
【設計方案】(1)方案一:向一定量樣品中加入過量澄清石灰水,根據反應生成碳酸鈣的質量,先求出碳酸鈉的質量,再計算樣品中碳酸鈉的質量分數。
(2)方案二:向一定量樣品中加入足量的稀鹽酸,根據反應生成二氧化碳的質量,先求出碳酸鈉的質量,再計算樣品中碳酸鈉的質量分數。
【進行實驗】甲組同學:稱取24.00g樣品,加水配成溶液,在溶液中加入過量的澄清石灰水。過濾、洗滌、干燥,共得到白色沉淀20.00g。
乙組同學:稱取24.00g樣品,加入足量的稀鹽酸直到反應停止,共收集到8.80g二氧化碳。
【解決問題】請你任選一組同學的實驗結果,幫助他們計算出樣品中碳酸鈉的質量分數。(寫出計算過程。計算結果精確到0.1% )
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com