
氯化鈉是一種重要的資源,在海水中儲量很豐富。
(1)海水曬鹽是海水在常溫下蒸發得到氯化鈉的過程,實驗室用氯化鈉溶液模擬該過程(如圖1)。已知B溶液恰好是氯化鈉的飽和溶液,與B溶液中溶質質量相等的溶液是________(填字母,下同),與B溶液中溶質質量分數相等的溶液是________。
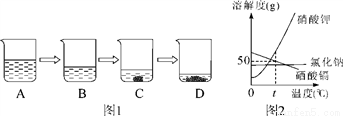
(2)氯化鈉、硝酸鉀、硒酸鎘的溶解度曲線如圖2所示。據圖回答:
①溶解度變化受溫度影響最大的是________,t℃時,溶解度最小的是________;
②t℃時,將25g硒酸鎘加入________g水中,完全溶解后,恰好得到飽和溶液。要進一步提高該溶液的溶質質量分數,可進行的操作是_________________________;
③硝酸鉀溶液中含有少量氯化鈉雜質,提純的方法是____________________。
科目:初中化學 來源:廣東省佛山市南海區2018屆九年級上學期期末考試化學試卷 題型:綜合題
為了除去二氧化碳中的少量氧氣,并探究二氧化碳的性質,某同學設計了如圖所示這套裝置。
實驗步驟 | 實驗現象 | 現象分析 |
①點燃A處酒精燈,緩緩通入混合氣體 | A中硬質玻璃管內固體 ___,B、C、D無明顯現象,E中石灰水變渾濁。 | A硬質玻璃管中銅粉的作用是_____。E中發生反應的化學方程式是___。 |
②點燃B中酒精噴燈 | B中木炭粉減少,E中石灰水渾濁,液面下降。 | B硬質玻璃管中發生反應的化學方程式是_____。 |
③點燃C中酒精燈 | C中現象___,E中石灰水變澄清,液面下降 | C硬質玻璃管中發生反應的化 學方程式是__ |
④停止通入混合氣體,并用止水夾夾緊進氣口,熄滅A,B,C處的酒精燈和酒精噴燈 | ___ 處有液體導入(填A﹣F) | D裝置的作用是__ |
【拓展與思考】
(1)從步驟②開始E中液面開始下降的原因:_____
(2)有同學認為該裝置需要添加尾氣處理理裝置,你認為是否需要并說明理由:_____。
查看答案和解析>>
科目:初中化學 來源:河南省南陽市內鄉縣2018屆九年級上學期期末質量評估化學試卷 題型:單選題
實驗室制取某些氣體的裝置如圖。下列說法正確的是
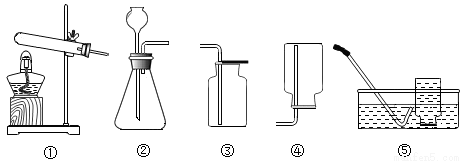
A. 裝置①和⑤組合可以用來制取氧氣 B. 裝置②和③組合可以用來制取氫氣
C. 裝置②和④組合可以用來制取二氧化碳 D. 裝置②可以較好地控制反應速率
查看答案和解析>>
科目:初中化學 來源:人教版2018屆九年級下冊化學單元測試:第8單元 金屬和金屬材料 題型:單選題
將一定質量的鐵粉加至H2SO4、MgSO4和CuSO4的混和溶液中,充分反應后過濾,得到濾液M和濾渣N,下列有關說法中,不合理的是
A. 濾液M中一定存在Fe2+
B. 濾渣N的質量一定小于加入鐵粉的質量
C. 濾渣N中一定沒有單質鎂
D. 濾液M中至少含有兩種金屬陽離子
查看答案和解析>>
科目:初中化學 來源:人教版2018屆九年級下冊化學單元測試:第9單元 溶液 題型:單選題
小明在實驗操作技能考試中抽中的題目是“用固體氯化鈉配制50g溶質質量分數為6%的氯化鈉溶液”。他的有關做法正確的是( )
A. 選擇的玻璃儀器有燒杯、量筒、玻璃棒、膠頭滴管、試劑瓶
B. 將氯化鈉直接放在托盤天平左盤上稱量3.0g
C. 用100mL量筒量取所需水的體積
D. 用內壁附有水珠的燒杯配制溶液
查看答案和解析>>
科目:初中化學 來源:人教版2018屆九年級下冊化學單元測試:第9單元 溶液 題型:單選題
某溫度下,在100g質量分數為20%的KNO3不飽和溶液甲中加入10gKNO3固體,恰好得到飽和溶液乙。下列說法正確的是( )
A. 該溫度下,KNO3的溶解度為30g
B. 乙溶液的質量分數為30%
C. 降低溫度,可以使甲溶液變成飽和溶液
D. 升高溫度,甲、乙兩溶液的質量分數都增大
查看答案和解析>>
科目:初中化學 來源:人教版2018屆九年級下冊化學單元測試:第10單元 酸和堿 題型:單選題
小凱整理歸納得出的規律合理的是( )
A. 溶液中的溶劑一定是水
B. 水既能跟某些金屬氧化物反應生成堿,也能跟某些非金屬氧化物反應生成酸
C. 酸、堿中一定都含有氧元素
D. 不能使酚酞溶液變紅的溶液一定是酸溶液
查看答案和解析>>
科目:初中化學 來源:石家莊新世紀外國語學校2017-2018年度九年級第一學期第三次質量檢測化學試卷 題型:簡答題
下圖表示有關物質的轉化關系(反應條件及部分生成物已省略)。已知甲、乙、丙為單質,其它均為化合物,A、C都是無色液體,且所含元素種類完全相同:D是無色有毒氣體。
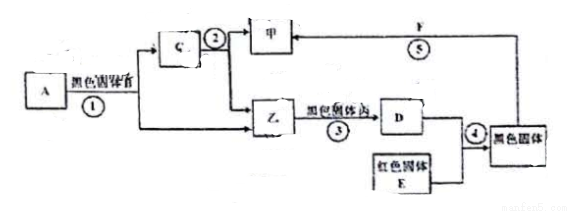
(1)F的化學式可能為(填一個即可)________。
(2)反應②的化學方程式________。
(3)反應④的化學方程式__________。
(4)反應①-⑤中屬于分解反應的是_______________(填序號)。
(5)反應⑤的現象為___________。
【答案】 HCl或H2SO4 2H2O 2H2↑+O2↑
2H2↑+O2↑  ①②色 有氣泡產生,溶液由無色變為淺綠、黑色固體減少
①②色 有氣泡產生,溶液由無色變為淺綠、黑色固體減少
【解析】本題是推斷題,解題時往往需要從題目中挖出一些明顯或隱含的條件,抓住突破口(突破口往往是現象特征、反應特征等),獲得結論,最后把結論代入原題中驗證。
A與C的組成元素相同的液體,乙為單質,可判斷A為過氧化氫、 C為水,乙為氧氣;由C分解生成氧氣和甲,則甲是氫氣;根據丙為黑色粉末且D是無色有毒氣體,丙是碳,則D是一氧化碳;一氧化碳與紅色固體E反應生成黑色固體,則紅色固體為氧化鐵,黑色固體是鐵,鐵能與酸溶液反應生成氫氣 ,則F為酸溶液,可能為稀硫酸或稀鹽酸,代入框圖,假設合理。因此:
(1)F是硫酸或鹽酸,化學式為HCl或H2SO4;
(2)反應②是水在通電條件下生成了氧氣和氫氣,化學方程式是2H2O 通電 2H2↑+ O2 ↑ ;
(3)反應④是一氧化碳和氧化鐵在高溫條件下生成了二氧化碳和鐵,化學方程式是 ;
;
(4)反應①-⑤中①②都是由一種物質生成兩種物質,屬于分解反應;。
(5)反應⑤是鐵與酸溶液反應的現象為有氣泡產生,溶液由無色變為淺綠色,黑色固體減少
。
【題型】推斷題
【結束】
35
小明過生日,吹蠟燭時怎么吹也吹不滅,小明同學帶著疑問與化學興趣小組的老師和同學一起對“吹不滅的蠟燭”展開了探究。
【查閱資料】普通蠟燭由石蠟和蠟燭芯制成,而吹不滅的蠟燭是在蠟燭芯上包裹一層打火石的粉末,打火石是由某種金屬摻入少量稀土元素制成的合金,它的著火點只有150℃,當蠟燭吹滅后,未冷卻的金屬繼續燃燒,從而使蠟燭復燃。吹不滅的蠟燭芯外的金屬可能是鎂、鋁、鐵或銅中的一種,為確定該金屬的成分,他們進行了下面的探究。(不考慮打火石中稀土元素對探究金屬性質的影響)
【提出問題】“吹不滅蠟燭”打火石中含有哪種金屬?
【做出猜想】
猜想一:該金屬是Cu 猜想二:該金屬是Fe
猜想三:該金屬是Mg 猜想四:該金屬是Al
【實驗探究】同學們根據所學的化學知識設計并進行如下實驗確定該金屬的成分.
(1)甲同學切開蠟燭,取出打火石,用砂紙打磨,打火石呈銀白色,猜想一不成立,原因是_________。
(2)乙同學取少量打磨后的打火石于試管中,滴加稀鹽酸,觀察現象,經過對現象的分析后,他們認為該金屬一定不是鐵,他們觀察到的現象是_______,猜想二不成立。
(3)為了進一步確定該金屬的種類,小明提議用硫酸銅溶液進行試驗,請你預測,將打火石加入到硫酸銅溶液后的現象是__________,其中涉及到的化學方程式______________。(任寫一個即可)
(4)同學們一致認為小明的方案不合理,經過討論他們設計了下面的實驗方案,確認了打火石中的金屬是鎂。
操作步驟 | 實驗現象 | 實驗結論 |
取一塊打磨后的“打火石”于試管中,加入少量__________溶液 | “打火石”表面有銀白色固體析出 | “打火石”中的金屬是Mg |
有關的化學方程式為_______________________。
【交流與反思】這種蠟燭燃燒時,蠟燭芯里的金屬為什么不燃燒?_______________,
這種蠟燭實際也可以熄滅,可采用的方法是_____________(填一種即可)。
【答案】 銅為紫紅色 溶液為無色 打火石表面有紅色固體附著,溶液顏色變淺(或變為無色) Mg+CuSO4=MgSO4+Cu或2Al+3CuSO4=Al2(SO4)3+3Cu(任寫一個即可) 硫酸鋁 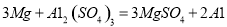 蠟燭燭芯被石蠟蒸汽包圍著,缺少氧氣,里面的金屬難以然燒 隔絕氧氣 或剪除燈芯 或用濕抹布蓋滅、用沙土蓋滅等(其他合理答案均可)
蠟燭燭芯被石蠟蒸汽包圍著,缺少氧氣,里面的金屬難以然燒 隔絕氧氣 或剪除燈芯 或用濕抹布蓋滅、用沙土蓋滅等(其他合理答案均可)
【解析】本題考查了金屬的性質和物質燃燒的條件。
(1)甲同學切開蠟燭,取出打火石,用砂紙打磨,打火石呈銀白色,猜想一不成立,原因是銅為紫紅色;
(2)鐵與稀鹽酸反應會生成淺綠色溶液。乙同學取少量打磨后的打火石于試管中,滴加稀鹽酸,觀察現象,經過對現象的分析后,他們認為該金屬一定不是鐵,他們觀察到的現象是溶液為無色,猜想二不成立;
(3)鋁和鎂的活動性都大于銅,都能將硫酸銅中銅置換出來,生成硫酸鋁或硫酸鎂,所以可預測,將打火石加入到硫酸銅溶液后的現象是打火石表面有紅色固體附著,溶液顏色變淺(或變為無色),其中涉及到的化學方程式2Al+3CuSO4=Al2(SO4)3+3Cu或Mg+CuSO4=MgSO4+Cu;
(4)鎂的活動性大于鋁,鎂能將鋁鹽溶液中的鋁置換出來。取一塊打磨后的“打火石”于試管中,加入少量硫酸鋁溶液,該反應是鎂與硫酸鋁反應生成硫酸鎂和鋁,化學方程式是: 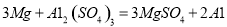 ;蠟燭芯里的金屬不燃燒原因是蠟燭燭芯被石蠟蒸汽包圍著,缺少氧氣里面的金屬難以然燒;熄滅蠟燭可采用的方法是隔絕氧氣 或剪除燈芯 或用濕抹布蓋滅、用沙土蓋滅等(其他合理答案均可)。
;蠟燭芯里的金屬不燃燒原因是蠟燭燭芯被石蠟蒸汽包圍著,缺少氧氣里面的金屬難以然燒;熄滅蠟燭可采用的方法是隔絕氧氣 或剪除燈芯 或用濕抹布蓋滅、用沙土蓋滅等(其他合理答案均可)。
【題型】科學探究題
【結束】
36
某化學興趣小組同學為回收一塊質量為40 g的銅鋅合金中的銅,將該合金放人燒杯中,逐漸加入稀硫酸至不再產生氣泡時,恰好用去稀硫酸100 g,燒杯內剩余固體27 g。請完成下列計算:
(1)40 g銅鋅合金中鋅的質量是________g 。
(2)計算所用稀硫酸中溶質的質量分數為_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com