
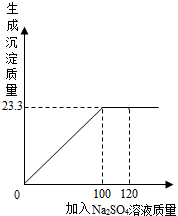
 將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2mL水中(ρ水=1lg/cm3),向所得溶液中滴加質量分數為14.2%的Na2SO4溶液,至恰好完全反應,下圖是所加Na2SO4溶液質量與生成沉淀質量的關系圖.
將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2mL水中(ρ水=1lg/cm3),向所得溶液中滴加質量分數為14.2%的Na2SO4溶液,至恰好完全反應,下圖是所加Na2SO4溶液質量與生成沉淀質量的關系圖.| 20g |
| 200g |


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:初中化學 來源: 題型:
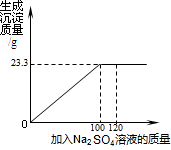 將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2g水中,向所得溶液中滴加質
將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2g水中,向所得溶液中滴加質查看答案和解析>>
科目:初中化學 來源: 題型:
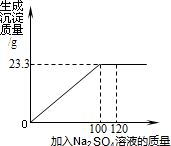 將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2g水中,向所得溶液中滴加一定質量分數的Na2SO4溶液.下圖是所加Na2SO4溶液質量與生成沉淀質量的關系圖,計算:
將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2g水中,向所得溶液中滴加一定質量分數的Na2SO4溶液.下圖是所加Na2SO4溶液質量與生成沉淀質量的關系圖,計算:查看答案和解析>>
科目:初中化學 來源: 題型:
 (2013?桂平市二模)將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2mL水中(水的密度 1g/cm3),向所得溶液中滴加質量分數為14.2%的Na2SO4溶液,至恰好完全反應.如圖是所加Na2SO4溶液質量與生成沉淀質量的關系圖,計算:
(2013?桂平市二模)將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2mL水中(水的密度 1g/cm3),向所得溶液中滴加質量分數為14.2%的Na2SO4溶液,至恰好完全反應.如圖是所加Na2SO4溶液質量與生成沉淀質量的關系圖,計算:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
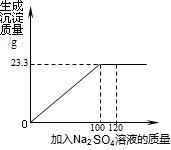 將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2g水中,向所得溶液中滴加質
將29.1g由NaCl和BaCl2組成的固體混合物溶解于94.2g水中,向所得溶液中滴加質查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com