
分析 I.根據物質的性質和用途來確定物質的名稱,然后根據物質化學式的寫法來分析;
II.(1)根據物質的性質決定物質的用途來分析;
(2)鎂的金屬活動性比鐵、銅強,在氯化銅和氯化亞鐵的混合溶液中加入一定質量的鎂粉,鎂先與氯化銅溶液反應生成氯化鎂溶液和銅,氯化銅反應完,若還有鎂粉,鎂才能與氯化亞鐵溶液反應生成氯化鎂溶液和鐵,據此結合題意進行分析解答;
Ⅲ.根據原子個數=$\frac{元素的質量}{該元素的相對原子質量}$,先根據含C70.5%、H 9.5%、N 7.0%、Mg 3.0%,其余為O,求出氧的質量分數,再進行計算.
解答 解:I.(1)金剛石硬度很大,常用于割玻璃,金剛石是一種碳的單質,其化學式為C;故填:C;
(2)人體胃液中含有的酸是鹽酸,其化學式為HCl;故填:HCl;
(3)熟石灰具有堿的通性,常用于改變土壤的酸堿性,將適量的熟石灰加入土壤,可以中和酸性,改變土壤的酸堿性,故填:Ca(OH)2;
(4)氮氣的化學性質很穩定,常溫下很難跟其他物質發生反應,常用來做焊接金屬時保護氣,故填:N2;
II.(1)A.鉑金飾品是利用金的金屬光澤和延展性;B.鐵鍋是利用鐵的導熱性;C.鋁制導線是利用鋁的導電性;故填:B;
(2)鎂的金屬活動性比鐵、銅強,在氯化銅和氯化亞鐵的混合溶液中加入一定質量的鎂粉,鎂先與氯化銅溶液反應生成氯化鎂溶液和銅,氯化銅反應完,若還有鎂粉,鎂才能與氯化亞鐵溶液反應生成氯化鎂溶液和鐵.
①由于不知加入鎂粉的質量,可能是鎂與氯化銅溶液、氯化亞鐵溶液恰好完全反應,均生成氯化鎂溶液,故濾液中一定含有的溶質是氯化鎂,其化學式為:MgCl2.
②濾渣中一定含有銀,可能含有鐵和鎂(過量剩余的),銅不與稀鹽酸反應,鐵能與稀鹽酸反應生成氫氣,向濾渣中滴加稀鹽酸,有氣泡產生,則濾渣中一定含有的物質是銅和鐵(化學式分別是Cu、Fe),可能含有鎂.
故答案為:①MgCl2;②Cu、Fe或Cu、Fe、Mg;
Ⅲ.確定氧元素的質量分數:1-(70.5%+9.5%+7.0%+3.0%)=10%;
確定葉綠素的相對分子質量.由于鎂元素的質量分數最小且相對原子質量最大,所以葉綠素分子中的鎂原子個數最小.如果葉綠素中有一個鎂原子,則其相對分子質量為$\frac{24}{3.0%}$=800,已知該葉綠素相對分子質量為750~850之間,所以符合題意,即葉綠素的相對分子質量為800.
則一個葉綠素分子中含各類原子的個數為:
C:$\frac{800×70.5%}{12}$=47;
H:$\frac{800×9.5%}{1}$=76;
N:$\frac{800×7.0%}{14}$=4;
Mg:$\frac{800×3.0%}{24}$=1;
O:$\frac{800×10%}{16}$=5.
故葉綠素的化學式為:C47H76O5N4Mg.
故答案為:C47H76O5N4Mg.
點評 本題難度不是很大,熟練掌握金屬的化學性質、綜合考慮各種出現的情況是正確解答此類題的關鍵.


 應用題點撥系列答案
應用題點撥系列答案 狀元及第系列答案
狀元及第系列答案 同步奧數系列答案
同步奧數系列答案科目:初中化學 來源: 題型:填空題
| 實驗操作 | 實驗現象 | 實驗結論 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 固體A、B的溶解度曲線如圖所示.
固體A、B的溶解度曲線如圖所示.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
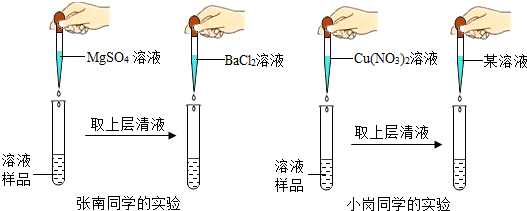
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 如圖所示(夾持儀器略去,K1、K2均關閉):打開K1,待液體全部流下,立即關閉K1,觀察到產生大量氣泡,且燒杯中丁的溶液變渾濁.充分反應后,打開K1和K2,使液體全部流入錐形瓶,瓶中無明顯現象.
如圖所示(夾持儀器略去,K1、K2均關閉):打開K1,待液體全部流下,立即關閉K1,觀察到產生大量氣泡,且燒杯中丁的溶液變渾濁.充分反應后,打開K1和K2,使液體全部流入錐形瓶,瓶中無明顯現象.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 64% | B. | 40% | C. | 36% | D. | 69.5% |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com