
| �ӟ� |
| ����� |
| ||
| ||
| ||
| �ӟ� |
| ����� |
| ||
| ||
| 11 |
| 2 |
| ||
| ||


 ��x��܇ϵ�д�
��x��܇ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ��2012�ý��Kʡ������(sh��)�(y��n)���о��꼉(j��)�W(xu��)�����п�ԇ���W(xu��)ԇ������������ �}�ͣ�̽���}
��14�֣�ijУ���W(xu��)�dȤС�M���^�ƉA�S�@��������Ϣ����(du��)���P(gu��n)��(w��n)�}�M(j��n)���о���
���a(ch��n)Ʒԭ����
ԓ�S���á������ƉA�������a(ch��n)�����a(ch��n)Ʒ�������A��Na2CO3���ͻ���NH4Cl��
���a(ch��n)ԭ���ǣ���NH3��CO2ͨ���ʳ�}ˮ�еõ�NaHCO3���w��NH4Cl��Һ������(y��ng)�Ļ��W(xu��)����ʽ�飺 ������x��NaHCO3���ӟ��Ƶü��A��
�����a(ch��n)���̡�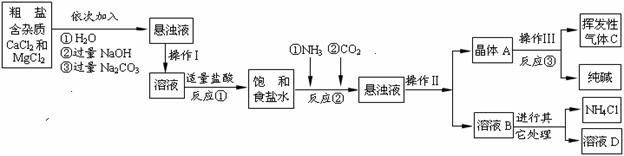
|
| ���|(zh��) | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| �ܽ�� | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
| | ��(sh��)�(y��n)һ | ��(sh��)�(y��n)�� | ��(sh��)�(y��n)�� | ��(sh��)�(y��n)�� |
| ���w�������Һ�|(zh��)�� | 100g | 100g | 100g | 100g |
| ����CaCl2��Һ�|(zh��)�� | 10g | 20g | 30g | 40g |
| ���ɵij������|(zh��)�� | 4g | �� | 10g | 10g |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ��2011-2012�W(xu��)�꽭�Kʡ���꼉(j��)�W(xu��)�����п�ԇ���W(xu��)ԇ���������棩 �}�ͣ�̽���}
��14�֣�ijУ���W(xu��)�dȤС�M���^�ƉA�S�@��������Ϣ����(du��)���P(gu��n)��(w��n)�}�M(j��n)���о���
���a(ch��n)Ʒԭ����
ԓ�S���á������ƉA�������a(ch��n)�����a(ch��n)Ʒ�������A��Na2CO3���ͻ���NH4Cl��
���a(ch��n)ԭ���ǣ���NH3��CO2ͨ���ʳ�}ˮ�еõ�NaHCO3���w��NH4Cl��Һ������(y��ng)�Ļ��W(xu��)����ʽ�飺 ������x��NaHCO3���ӟ��Ƶü��A��
�����a(ch��n)���̡�

|
�� NH4Cl NH3��+HCl��
�� ��֪20��r(sh��)���P(gu��n)���|(zh��)���ܽ�����£����wָ1�w�eˮ�����ܽ�Ě��w�w�e��
|
���|(zh��) |
NaCl |
NaHCO3 |
NH4Cl |
NH3 |
CO2 |
|
�ܽ�� |
36.0g |
9.6g |
37.2g |
710 |
0.9 |
����(w��n)�}ӑՓ��
�Ų������У���ͬ���������Q�� ������(y��ng)���аl(f��)���˃ɂ�(g��)����(y��ng)����������һ��(g��)���W(xu��)����ʽ�� ������(y��ng)�ټ��m�����}�ᣬ�m����ָ ��
�ƙz�(y��n)�]�l(f��)�Ԛ��wC�ķ��� ��
���������a(ch��n)�����п�ѭ�h(hu��n)ʹ�õ��� ������̖(h��o)����
A���]�l(f��)�Ԛ��wC B����ҺD C���������V D������NH4Cl
���M�ɴ_����
�� �Qȡһ���|(zh��)���ļ��A��Ʒ����(j��ng)��γ�ּӟ���ٷQ�أ��|(zh��)���o(w��)׃����
�� ��ȡ�������A��Ʒ�����m��ˮ����Ʒ��ȫ�ܽ⣬��ԓ��Һ�м����^(gu��)��ϡHNO3���ٵμ�AgNO3��Һ���а�ɫ��������������(sh��)�(y��n)�ɴ_�����A��Ʒ�����s�|(zh��) �������W(xu��)ʽ����
�������y(c��)����
|
|
��(sh��)�(y��n)һ |
��(sh��)�(y��n)�� |
��(sh��)�(y��n)�� |
��(sh��)�(y��n)�� |
|
���w�������Һ�|(zh��)�� |
100g |
100g |
100g |
100g |
|
����CaCl2��Һ�|(zh��)�� |
10g |
20g |
30g |
40g |
|
���ɵij������|(zh��)�� |
4g |
�� |
10g |
10g |
�Qȡԓ���A��Ʒ44 g���w������ˮ���400g��Һ��ƽ���֞��ķݣ�Ȼ��քe����һ���|(zh��)����?j��n)?sh��)��CaCl2��Һ����(sh��)�(y��n)��(sh��)��(j��)Ҋ����
Ո(q��ng)�������Д�(sh��)��(j��)�ش�Ӌ(j��)�㣺
�ţ�= g��
���ڌ�(sh��)�(y��n)���У���ȫ����(y��ng)��������Һ�����|(zh��)�Ȼ��c���|(zh��)����?j��n)?sh��)�Ƕ��٣�(Ҫ��Ӌ(j��)���^(gu��)�̣��Y(ji��)������0.1%)
�����Y(ji��)��˼��
Ո(q��ng)ͨ�^(gu��)Ӌ(j��)�㲢�Y(ji��)���±��Д�˼��A��Ʒ�ȼ�(j��)�� Ʒ�����������A�����y(c��)���У���CaCl2��Һ�Ğ�BaCl2��Һ���y(c��)���`���(hu��)�pС��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ���x����
ijУ���W(xu��)�dȤС�M���^�ƉA�S�@��������Ϣ����(du��)���P(gu��n)��(w��n)�}�M(j��n)���о���
���a(ch��n)Ʒԭ����
ԓ�S���á������ƉA�������a(ch��n)�����a(ch��n)Ʒ——���A��Na2CO3���ͻ���NH4Cl��
���a(ch��n)ԭ���ǣ���NH3��CO2ͨ���ʳ�}ˮ�еõ�NaHCO3���w��NH4Cl��Һ������(y��ng)�Ļ��W(xu��)����ʽ�飺 ������x��NaHCO3���ӟ��Ƶü��A��
�����a(ch��n)���̡�
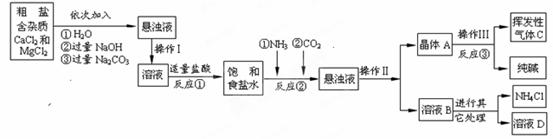
|
�� NH4Cl NH3��+HCl��
�� ��֪20��r(sh��)���P(gu��n)���|(zh��)���ܽ�����£����wָ1�w�eˮ�����ܽ�Ě��w�w�e��
| ���|(zh��) | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| �ܽ�� | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
����(w��n)�}ӑՓ��
�Ų������У���ͬ���������Q�� ������(y��ng)���аl(f��)���˃ɂ�(g��)����(y��ng)����������һ��(g��)���W(xu��)����ʽ�� ������(y��ng)�ټ��m�����}�ᣬ�m����ָ ��
�ƙz�(y��n)�]�l(f��)�Ԛ��wC�ķ��� ��
���������a(ch��n)�����п�ѭ�h(hu��n)ʹ�õ��� ������̖(h��o)����
A���]�l(f��)�Ԛ��wC B����ҺD C���������V D������NH4Cl
���M�ɴ_����
�� �Qȡһ���|(zh��)���ļ��A��Ʒ����(j��ng)��γ�ּӟ���ٷQ�أ��|(zh��)���o(w��)׃����
�� ��ȡ�������A��Ʒ�����m��ˮ����Ʒ��ȫ�ܽ⣬��ԓ��Һ�м����^(gu��)��ϡHNO3���ٵμ�AgNO3��Һ���а�ɫ��������������(sh��)�(y��n)�ɴ_�����A��Ʒ�����s�|(zh��) �������W(xu��)ʽ����
�������y(c��)����
| ��(sh��)�(y��n)һ | ��(sh��)�(y��n)�� | ��(sh��)�(y��n)�� | ��(sh��)�(y��n)�� | |
| ���w�������Һ�|(zh��)�� | 100g | 100g | 100g | 100g |
| ����CaCl2��Һ�|(zh��)�� | 10g | 20g | 30g | 40g |
| ���ɵij������|(zh��)�� | 4g | �� | 10g | 10g |
�Qȡԓ���A��Ʒ44 g���w������ˮ���400g��Һ��ƽ���֞��ķݣ�Ȼ��քe����һ���|(zh��)����?j��n)?sh��)��CaCl2��Һ����(sh��)�(y��n)��(sh��)��(j��)Ҋ����
Ո(q��ng)�������Д�(sh��)��(j��)�ش�Ӌ(j��)�㣺
�ţ�= g��
���ڌ�(sh��)�(y��n)���У���ȫ����(y��ng)��������Һ�����|(zh��)�Ȼ��c���|(zh��)����?j��n)?sh��)�Ƕ��٣�(Ҫ��Ӌ(j��)���^(gu��)�̣��Y(ji��)������0.1%)
�����Y(ji��)��˼��
Ո(q��ng)ͨ�^(gu��)Ӌ(j��)�㲢�Y(ji��)���±��Д�˼��A��Ʒ�ȼ�(j��)�� Ʒ�����������A�����y(c��)���У���CaCl2��Һ�Ğ�BaCl2��Һ���y(c��)���`���(hu��)�pС��
|

�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com