

| 實驗目的 | 實驗操作 | 現象或測定結果 | 結論或化學方程式 |
| 除去碳酸鈉 | 取少量該固體樣品溶于水配成溶液,滴加適量的______溶液,充分反應后過濾 | 有白色沉淀生成 | 有關反應的化學方程式為______ |
| 檢驗是否含有氫氧化鈉 | 用PH試紙測定反應后溶液的酸堿度,操作方法是______ | pH>7 | 該樣品中含有氫氧化鈉 |
| 106 |
| 44 |
| 32 |
| 0.44g |


科目:初中化學 來源:不詳 題型:問答題

查看答案和解析>>
科目:初中化學 來源:不詳 題型:問答題
| ||
| ||
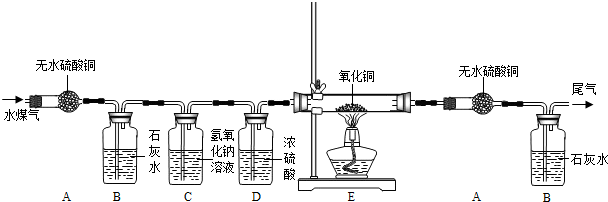
查看答案和解析>>
科目:初中化學 來源:不詳 題型:問答題
| 熔點 | 沸點 | 熱穩定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升華 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 與Ca(OH)2反應產生白色沉淀(CaC2O4) |
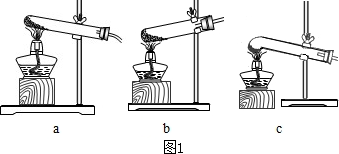
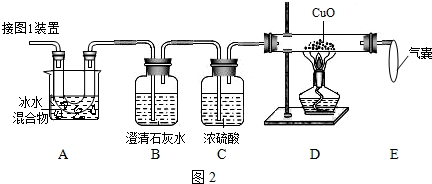
查看答案和解析>>
科目:初中化學 來源:不詳 題型:問答題
| 物質 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 顏色 | 白色 | 白色 | 淡黃色 | 白色 | 白色 | 白色 |
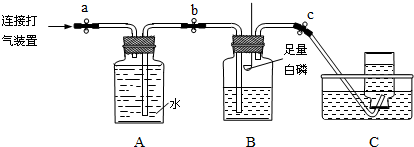
查看答案和解析>>
科目:初中化學 來源:不詳 題型:問答題
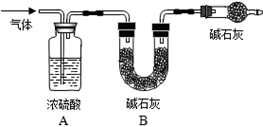
| 實驗序號 | 實驗操作 | 實驗現象 | 解釋及結論 |
| 實驗I | 用砂紙擦去鎂條表面氧化膜,將其放入盛有適量飽和碳酸氫鈉溶液的試管中 | 迅速反應,產生大量氣泡和白色不溶物 |  |
| 實驗Ⅱ | 將實驗I中收集到的氣體點燃,并在火焰上方罩一干、冷的小燒杯 | 氣體安靜燃燒、產生淡藍色火焰,燒杯內壁有水霧出現. | 該氣體是______,燃燒的化學方程式為 ______. |
查看答案和解析>>
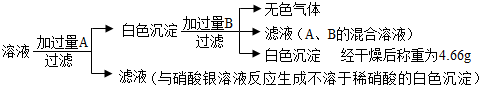
科目:初中化學 來源:不詳 題型:填空題
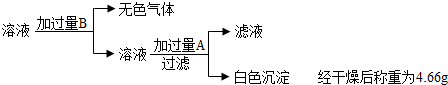
查看答案和解析>>
科目:初中化學 來源:不詳 題型:問答題
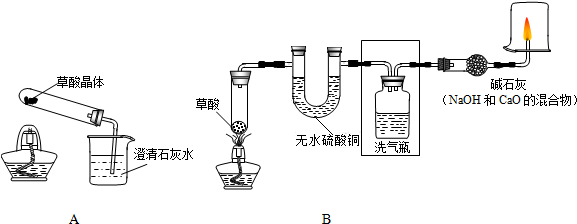
查看答案和解析>>
科目:初中化學 來源:不詳 題型:問答題
| ||
| ||
| 實驗步驟 | 實驗現象 | 實驗結論及分析 |
| ①取少量濾液于試管中,滴加足量的NaOH濃溶液后加熱,并將濕潤的紅色石蕊試紙放在試管口. | ______ | 濾液中含有NH4Cl,有關化學方程式: NaOH+NH4Cl=NaCl+NH3↑+H2O |
| ②另取少量濾液于試管中,滴加稀鹽酸. | 產生無色 無味氣體. | 濾液中含有______,有關化學方程式: ______. |
| ③另取少量濾液蒸干后充分灼燒,取灼燒后的殘余固體溶于水,滴加稀HNO3,再滴加AgNO3溶液. | 產生白色沉淀. | 濾液中含有______,濾液蒸干后充分灼燒的目的是______. |
| 實驗操作 | 實驗現象 | 實驗結論 |
| 取一定量純堿樣品配成溶液后,滴加過量的CaCl2溶液. | 產生白色沉淀. | 反應的化學方程式: ______. |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com