
| A. | 原子的質量主要集中在質子上 | B. | 構成物質的微粒只有分子和原子 | ||
| C. | 氧氣很活潑 | D. | 鑒別硬水與軟水可用肥皂水 |
 中考解讀考點精練系列答案
中考解讀考點精練系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| Fe3O4 | Fe2O3 | 鐵 | |
| 分解溫度/℃ | 1538 | 1400 | |
| 熔點點/℃ | 1535 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
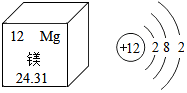 我會看,圖:原子序數是12;元素名稱是鎂;元素符號是Mg;是金屬元素(填“金屬”或“非金屬”);相對原子質量是24.31. 核電荷數12,核外有3個電子層,
我會看,圖:原子序數是12;元素名稱是鎂;元素符號是Mg;是金屬元素(填“金屬”或“非金屬”);相對原子質量是24.31. 核電荷數12,核外有3個電子層,查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 鐵在氧氣中燃燒的全過程可用如圖表示,試回答下列問題:
鐵在氧氣中燃燒的全過程可用如圖表示,試回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:推斷題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com