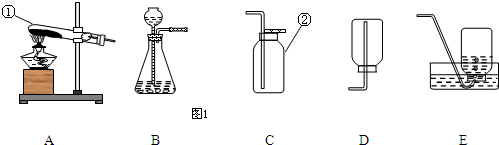
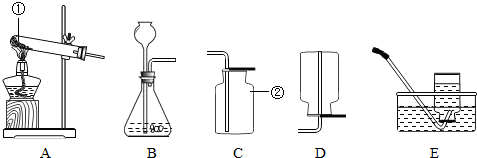
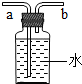
解:(1)熟記常見儀器即可儀器的名稱:①試管;②集氣瓶;
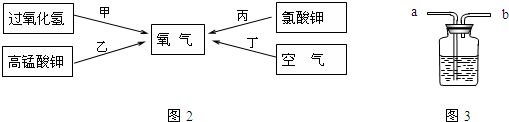
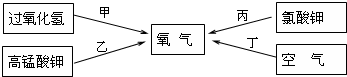
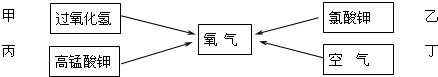
(2)雙氧水和二氧化錳混合制氧氣的文字表達式:過氧化氫
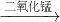
水+氧氣;高錳酸鉀受熱分解生成錳酸鉀、二氧化錳、氧氣,文字表達式:高錳酸鉀

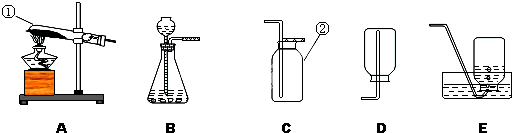
錳酸鉀+二氧化錳+氧氣;制取裝置包括加熱和不需加熱兩種,用雙氧水制氧氣不需要加熱,可以節約熱能,且另一種生成物是水,無污染,所以符合綠色化學的理念;用高錳酸鉀或氯酸鉀制氧氣需要加熱,不符符合綠色化學的理念.故選甲,選擇的發生裝置為B;要收集一瓶較純凈的氧氣應選擇的收集裝置為排水法,故選E;
(3)實驗室用高錳酸鉀制取氧氣時,排水法收集氧氣的適宜時間是:當氣泡冒出均勻后再收集;先熄滅酒精燈,試管溫度降低試管中的氣體壓強減小水會倒吸炸裂試管,所以要先移出導管再熄滅酒精燈;
(4)用空氣制取氧氣過程中,沒有新物質生成物,所以是物理變化;
(5)氯化銨固體與堿石灰固體共熱來制取氨氣需要加熱,所以選擇的發生裝置是A;氨氣的性質為密度比空氣小.NH
3極易溶于水,所以收集裝置是D.
故答案為:(1)①試管;②集氣瓶;(2)過氧化氫
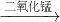
水+氧氣;高錳酸鉀

錳酸鉀+二氧化錳+氧氣;(3)當氣泡冒出均勻后再收集;防止水會倒吸炸裂試管;(4)物理;(5)A;D.
分析:(1)熟記常見儀器的名稱和作用;
(2)如果用雙氧水制氧氣就不需要加熱,可以節約熱能,且另一種生成物是水,無污染,符合綠色化學的理念;
(3)根據實驗室用排水法收集氧氣的注意事項進行解答;
(4)根據是否有新物質生成判斷,沒有新物質生成的是物理變化;
(5)根據氯化銨固體與堿石灰固體共熱來制取氨氣需要加熱以及氨氣的性質為密度比空氣小.NH
3極易溶于水來選擇收集方法進行解答.
點評:此題考查的是氣體的制取原理和裝置的選擇.只要掌握氣體的制取原理,掌握裝置選擇的依據,問題就能迎刃而解.

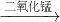 水+氧氣;高錳酸鉀受熱分解生成錳酸鉀、二氧化錳、氧氣,文字表達式:高錳酸鉀
水+氧氣;高錳酸鉀受熱分解生成錳酸鉀、二氧化錳、氧氣,文字表達式:高錳酸鉀 錳酸鉀+二氧化錳+氧氣;制取裝置包括加熱和不需加熱兩種,用雙氧水制氧氣不需要加熱,可以節約熱能,且另一種生成物是水,無污染,所以符合綠色化學的理念;用高錳酸鉀或氯酸鉀制氧氣需要加熱,不符符合綠色化學的理念.故選甲,選擇的發生裝置為B;要收集一瓶較純凈的氧氣應選擇的收集裝置為排水法,故選E;
錳酸鉀+二氧化錳+氧氣;制取裝置包括加熱和不需加熱兩種,用雙氧水制氧氣不需要加熱,可以節約熱能,且另一種生成物是水,無污染,所以符合綠色化學的理念;用高錳酸鉀或氯酸鉀制氧氣需要加熱,不符符合綠色化學的理念.故選甲,選擇的發生裝置為B;要收集一瓶較純凈的氧氣應選擇的收集裝置為排水法,故選E;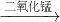 水+氧氣;高錳酸鉀
水+氧氣;高錳酸鉀 錳酸鉀+二氧化錳+氧氣;(3)當氣泡冒出均勻后再收集;防止水會倒吸炸裂試管;(4)物理;(5)A;D.
錳酸鉀+二氧化錳+氧氣;(3)當氣泡冒出均勻后再收集;防止水會倒吸炸裂試管;(4)物理;(5)A;D.

 高效智能課時作業系列答案
高效智能課時作業系列答案