
如圖所示,實驗裝置足以維持實驗期間小白鼠的生命活動,瓶口密封,忽略水蒸氣和溫度變化對實驗結果的影響。經數小時實驗后,U形管A、B兩處的液面會出現下列哪種情況( )
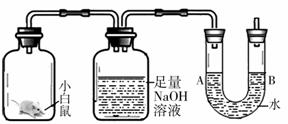 A.A處下降,B處上升
A.A處下降,B處上升
B.A、B兩處都下降
C.A處上升,B處下降
D.A、B兩處都不變
科目:初中化學 來源: 題型:
探究水蒸氣通過灼熱的木炭后,得到的混合氣體的主要成分。
【提出猜想】該混合氣體主要成分為CO、CO2、H2和H2O。
【查閱資料】a.濃硫酸可作干燥劑。 b.氫氣在加熱的條件下與氧化銅反 應生成銅和水。
應生成銅和水。
 【實驗過程】設計實驗裝置如下:(部分夾持儀器已略去;假設每個裝置里的藥品足量,反應充分)。
【實驗過程】設計實驗裝置如下:(部分夾持儀器已略去;假設每個裝置里的藥品足量,反應充分)。
裝置A中無水硫酸銅變藍,寫出該反應的化學方程式 (11) ,裝置B中澄清石
灰水變渾濁,寫出該反應的化學方程式 (12) ,由此得出混合氣體中含有CO2和
H2O氣體; ②通過觀察裝置D、E中的現象后 ,為了確認混合氣體中含有氫氣,裝置C
中的試劑是 (13) 。為了證明CO氣體的存在,裝置F中試劑是 (14) 。
【實驗結論】猜想正確。
查看答案和解析>>
科目:初中化學 來源: 題型:
用鋅、氧化銅、稀硫酸作原料制取銅,有下列兩種途徑:
(1)Zn 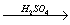 H2
H2 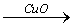 Cu; (2)CuO
Cu; (2)CuO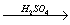 CuSO4
CuSO4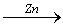 Cu
Cu
若用這兩種方法制得相同質量的銅時,下列敘述符合實驗結果的是 ( )
A.消耗相同質量的氧化銅 B.消耗相同質量的鋅
C.消耗相同質量的硫酸 D.生成的硫酸鋅質量相同
查看答案和解析>>
科目:初中化學 來源: 題型:
有甲、乙、丙三種金屬,將甲投入丙的硫酸鹽溶液中,有丙析出。將乙、丙兩種金屬分別投入硫酸銅溶液中,丙的表面有紅色物質析出,乙的表面沒有明顯變化。 則甲、乙、丙三種金屬活動性順序排列正確的是( )
則甲、乙、丙三種金屬活動性順序排列正確的是( )
A.甲>乙>丙 B.甲>丙>乙 C.丙>乙>甲 D.丙>甲>乙
查看答案和解析>>
科目:初中化學 來源: 題型:
下列有關二氧化碳的說法正確的是( )
A.二氧化碳是引發酸雨的“罪魁”
B.二氧化碳固體可用于人工降雨
C.二氧化碳可使紫色石蕊試液變藍
D.二氧化碳有毒不能制作碳酸飲料
查看答案和解析>>
科目:初中化學 來源: 題型:
下表是Ca(OH)2和NaOH的溶解度數據。請回答下列問題:
| 溫度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
(1)依據上表數據,繪制Ca(OH)2和NaOH的溶解度曲線,下圖中能表示NaOH溶解度曲線的是 (填A或B)。
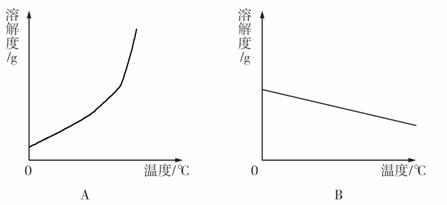
(2)要想把一 瓶接近飽和的Ca(OH)2溶液變成飽和溶液,具體措施有:
瓶接近飽和的Ca(OH)2溶液變成飽和溶液,具體措施有:
①加入氫氧化鈣,②升高溫度,③降低溫度,④加入水,⑤蒸發水后再恢復到原溫度,⑥加入生石灰。
其中措施正確的是 。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃時,191g 飽和NaO H溶液,蒸發10g水后,再降溫到20℃,可析出NaOH晶體的質量為 。
H溶液,蒸發10g水后,再降溫到20℃,可析出NaOH晶體的質量為 。
(4)現有20℃時Ca(OH)2的飽和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此時溶液中溶質的質量分數 乙 甲(填“>”、“<”或“=”)。
(5)現有60℃時含Ca(OH)2和N aOH兩種溶質的飽和溶液,若要得到較純凈的NaOH晶體,應采取的物理方法是 。
aOH兩種溶質的飽和溶液,若要得到較純凈的NaOH晶體,應采取的物理方法是 。
(6)20℃時,欲測定NaOH溶液的pH,若先將pH試紙用蒸餾水潤濕,再進行測定,則所測溶液的pH (填“偏大”、“偏小”或“不受影響”)。
查看答案和解析>>
科目:初中化學 來源: 題型:
下表呈現的是部分元素的原子結構示意圖、主要化合價等信息。
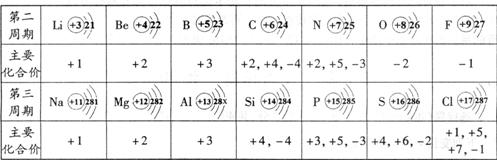
下列敘述錯誤的是( )
A.鋁原子結構示意圖的最外層有3個電子
B.元素的正化合價數一定等于原子的最外層電子數
C.核電荷數分別為8和14的元素,組成化合物的化學式為SiO2
D.同一周期中,原子的核外電子層數相同,最外層電子數從左向右逐漸增多
查看答案和解析>>
科目:初中化學 來源: 題型:
“鳳凰”號火星探測器圓滿完成任務,向地面發回數量堪稱史無前例的圖像和數據,為人類探索火星提供了寶貴的科學資料。請完成14~16題。
(1) “鳳凰”號探測器發回的最新照片上顯示,火星上確有液態水存在。下列微粒模型示意圖可表示構成水的微粒的是 (填標號)。
a. b.
b. c.
c. d.
d.
(2)火星上含有豐富的二氧化碳和鎂資源。科學家設想,鎂可作為未來火星上的燃料,因為鎂能在二氧化碳中燃燒放出大量的熱,同時生成氧化鎂和碳。該反應的化學方程式為 。
(3)火星北極的土壤呈弱堿性。如果火星具備作物生長的條件,下表所列作物較適宜在火星北極種植的有 。
| 作物名稱 | 蘆筍 | 草莓 | 蘿卜 | 馬鈴薯 |
| 適宜生長的pH | 5.5~7.8 | 5.5~6.5 | 5~8 | 5.6~6 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com