
【題目】向53g質量分數為10%的碳酸鈉溶液中逐滴加入質量分數為5%的稀鹽酸,生成二氧化碳的質量隨加入鹽酸質量的變化關系如圖所示.(不考慮CO2的溶解) 已知:
OB段反應的化學方程式為Na2CO3+HCl═NaCl+NaHCO3
BD段(不含B點)反應的化學方程式為NaH CO3+HCl═NaCl+H2O+CO2↑
請回答:
(1)53g質量分數為10%的碳酸鈉溶液中溶質質量為g.
(2)A點對應溶液中溶質有(填化學式).
(3)B點橫坐標為.(計算結果保留1位小數,下同)
(4)假設C點橫坐標為54.75,計算C點對應的二氧化碳質量.(寫出計算過程)
【答案】
(1)5.3
(2)Na2CO3、NaCl、NaHCO3
(3)36.5
(4)解:設C點對應的二氧化碳質量為y.
NaHCO3+ | HCl═NaCl+H2O+ | CO2↑ |
36.5 | 44 | |
(54.75g﹣36.5g)×5% | y |
![]() 解得:y=1.1g
解得:y=1.1g
【解析】解:(1)53g質量分數為10%的碳酸鈉溶液中溶質質量為:53g×10%=5.3g.(2)由生成二氧化碳的質量隨加入鹽酸質量的變化關系可知,在如圖A點時,溶液中碳酸鈉部分與鹽酸反應生成了氯化鈉和碳酸氫鈉,所以,對應溶液中溶質有:Na2CO3、NaCl、NaHCO3 . (3)由生成二氧化碳的質量隨加入鹽酸質量的變化關系可知,在如圖B點時,溶液中碳酸鈉恰好與鹽酸反應生成了氯化鈉和碳酸氫鈉, 設與碳酸鈉反應生成了氯化鈉和碳酸氫鈉的鹽酸的質量為x
Na2CO3+ | HCl═NaCl+NaHCO3 |
106 | 36.5 |
5.3g | x×5% |
![]() 解得x=36.5g(4)設C點對應的二氧化碳質量為y.
解得x=36.5g(4)設C點對應的二氧化碳質量為y.
NaHCO3+ | HCl═NaCl+H2O+ | CO2↑ |
36.5 | 44 | |
(54.75g﹣36.5g)×5% | y |
![]() 解得:y=1.1g
解得:y=1.1g
故答為:(1)5.3;(2)Na2CO3、NaCl、NaH CO3;(3)36.5;(4)C點對應的二氧化碳質量未1.1g.
(1)根據溶質的質量分數計算;(2)根據生成二氧化碳的質量隨加入鹽酸質量的變化關系分析A點對應溶液中溶質;(3)根據在B點時Na2CO3與鹽酸恰好反應生成了氯化鈉和碳酸氫鈉計算分析;(4)根據碳酸氫鈉與鹽酸反應的方程式及參加該反應鹽酸的質量計算C點對應的二氧化碳質量.


科目:初中化學 來源: 題型:
【題目】下列關于水的說法不正確的是 ( )
A. 水是一種化學資源
B. 電解水產生了氫氣和氧氣,說明水是由氫氣和氧氣組成的
C. 水分子保持水的化學性質
D. 用肥皂水可以區別硬水和軟水
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】元素是化學的重要觀念之一。下列有關元素的說法中錯誤的是( )
A. 元素是具有相同核電荷數的一類原子的總稱
B. 同種元素的原子核內質子數與中子數一定相等
C. 元素的原子序數與該元素原子核電荷數在數值上相同
D. 在物質發生化學變化時,原子的種類不變,元素的種類也不會改變
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】鑒別下列物質時,所選用的試劑或方法不正確的是( )
A. 氮氣和氧氣(帶火星的木條) B. 白酒和白醋(聞氣味)
C. 碳粉和二氧化錳(在空氣中加熱) D. 黃金和黃銅(觀察顏色)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在M+N→鹽+水的反應中,M和N不可能是( )
A. HCl和NaOH B. CO2和Ca(OH)2 C. H2SO4和Fe2O3 D. AgNO3和BaCl2
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A~H是初中化學常見的物質,已知A為黑色固體單質,G為紫紅色固體單質,B為紅棕色粉末,H為藍色的硫酸鹽溶液.它們的轉化關系如圖所示,回答問題: 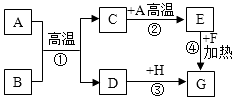
(1)B的化學式為 , H中溶質的化學式;
(2)反應①的化學反應方程式為;該反應中氧化劑是(填物質名稱);
(3)反應①~③中為置換反應的是(填序號);
(4)反應②是(填“放熱”或“吸熱”)反應.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】可以鑒別出空氣、氧氣、二氧化碳三瓶氣體的最佳方法是
A. 分別加入適量澄清石灰水 B. 用帶火星木條分別伸入瓶中
C. 觀察三種氣體的顏色 D. 用燃著的木條分別伸入瓶中
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com