

分析 根據質量守恒定律可知,過程中質量的減少是因為生成了氫氣,所以可以求算氫氣的質量,根據氫氣的質量和對應的化學方程式求算氫化鈣的質量,進而求算對應的質量分數.
解答 解:
根據質量守恒定律可求,生成氫氣的質量為20g+30g-48.4g=1.6g
設氫化鈣的質量為x
CaH2+2H2O═Ca(OH)2+2H2↑
42 4
x 1.6g
$\frac{42}{4}$=$\frac{x}{1.6g}$
x=16.8g
該樣品中氫化鈣的質量分數為$\frac{16.8g}{20g}$×100%=84%
答:
(1)生成氫氣的質量是 1.6g.
(2)該樣品中氫化鈣的質量分數84%.
點評 根據化學方程式計算時,第一要正確書寫化學方程式,第二要使用正確的數據,第三計算過程要完整.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | Fe→Fe(OH)3 | B. | H2SO4→HCl | C. | BaCl2→Ba(NO3)2 | D. | CuSO4→Cu(OH)2 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 一定有Ag生成 | B. | 所得溶液中一定有Zn2+、Cu2+ | ||
| C. | 一定有Cu生成 | D. | 所得溶液中一定有Cu2+、Ag+ |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
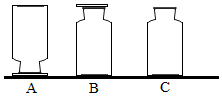 如圖所示,在實驗臺上放置三瓶氣體,集氣瓶A盛有C02、O2、H2中 的一種,集氣瓶B盛有這三種氣體中的另一種.小剛和小強想對瓶中氣體進行探究.
如圖所示,在實驗臺上放置三瓶氣體,集氣瓶A盛有C02、O2、H2中 的一種,集氣瓶B盛有這三種氣體中的另一種.小剛和小強想對瓶中氣體進行探究.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
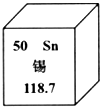
| A. | 原子序數是50 | B. | 相對原子質量是118.7 | ||
| C. | 屬于非金屬元素 | D. | 元素符號為Sn |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com