
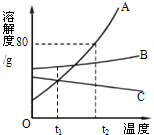
 溶解度曲線為我們定量描述物質的溶解性強弱提供了便利.請你根據如圖的溶解度曲線回答下列問題:
溶解度曲線為我們定量描述物質的溶解性強弱提供了便利.請你根據如圖的溶解度曲線回答下列問題: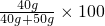 %=44.4%.
%=44.4%.

 暑假作業暑假快樂練西安出版社系列答案
暑假作業暑假快樂練西安出版社系列答案 新活力總動員暑系列答案
新活力總動員暑系列答案 龍人圖書快樂假期暑假作業鄭州大學出版社系列答案
龍人圖書快樂假期暑假作業鄭州大學出版社系列答案科目:初中化學 來源: 題型:
 溶解度曲線為我們定量描述物質的溶解性強弱提供了便利.請你根據右圖的溶解度曲線回答下列問題:
溶解度曲線為我們定量描述物質的溶解性強弱提供了便利.請你根據右圖的溶解度曲線回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:
 (2005?徐州)溶解度曲線為我們定量描述物質的溶解性強弱提供了便利.請你根據右圖的溶解度曲線回答下列問題:
(2005?徐州)溶解度曲線為我們定量描述物質的溶解性強弱提供了便利.請你根據右圖的溶解度曲線回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com