
 某同學用圖裝置測定空氣中氧氣的體積分數.請你填寫有關空格
某同學用圖裝置測定空氣中氧氣的體積分數.請你填寫有關空格 ,但是在實驗后發現測定出的空氣中氧氣的體積分數低于
,但是在實驗后發現測定出的空氣中氧氣的體積分數低于 ,可能是由哪些原因起的?______(寫一條原因).
,可能是由哪些原因起的?______(寫一條原因).  ,從而導致測定出的空氣中氧氣的體積分數低于
,從而導致測定出的空氣中氧氣的體積分數低于 ;
;

 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案科目:初中化學 來源: 題型:閱讀理解

查看答案和解析>>
科目:初中化學 來源:2011-2012學年江西省撫州市教研室九年級上學期期末化學試卷 題型:探究題
探究性實驗是驗證化學理論的一種主要方式,也展示了化學的無窮魅力。
【提出問題】催化劑能加快反應速率,但自身質量和化學性質不變。
【查閱資料】①已知KClO3分解產生氧氣和KCl; ②KClO3和KCl都能溶于水,MnO2難溶于水;③MnO2與濃鹽酸在加熱時能產生黃綠色的Cl2.
【設計實驗】
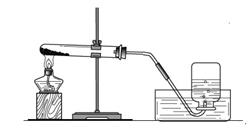
實驗一、取兩份質量相等(約5克)的KClO3分別放入兩只大試管(分別標記A和B)中,往B試管中加入質量為1.0克MnO2的,然后按圖所示組裝好儀器,加熱。結果發現加了MnO2的裝置收集滿一集氣瓶的氣體所用的時間要少。

實驗二、待裝置完全冷卻之后,將B管中物質置于燒杯中加水溶解、過濾;再將濾出物干燥、稱量得質量約為1.0克。
實驗三 、取少量濾出物與濃鹽酸置于反應裝置中(放在通風櫥中),加熱;有黃綠色氣體產生。根據以上實驗回答下列問題:
(1)實驗一說明加了MnO2之后,KClO3分解的速率更快,寫出這一反應的化學方程式:
;如何驗證集氣瓶中的氣體為氧氣 。
(2)通過上述三個實驗能說明 。
(3)某同學用KClO3和KMnO4的混合物加熱,發現產生氧氣的速度也很快,該同學就斷定KMnO4在KClO3分解反應中也能起催化作用,你認為這同學的判斷對嗎? ;為什么? 。
27.(每空1分,7分) 某化學興趣小組的同學為了探究Mg、Cu、Fe的金屬活動性順序開展了一下以下探究活動。
(1)進行試驗,獲得結論。完成如下實驗報告,并回答有關問題。
|
|
實驗方案 |
實驗現象 |
實驗結論 |
|
方 案 一 |
將Fe絲浸入CuSO4溶液中 |
Fe絲表面有紅色物質析出 |
金屬活動性:Fe_ _Cu(填“>”或“<”)該反應的反應類型屬于 ____________反應。 |
|
方 案 二 |
將Mg和Cu分別在空氣中灼燒 |
發現鎂能劇烈燃燒,而另一種不能 |
金屬活動性:Mg_ _Cu(填“>”或“<”) |
|
方 案 三 |
分別將Mg和Fe放入_________中,觀察現象 |
觀察到_ (填元素符號)產生氣泡的速度較慢 |
金屬活動性順序:Mg>Fe |
 (2)反思與交流。經過討論,該小組同學一致認為:比較金屬與酸反應產生氫氣的快慢,有兩種測定方法:
(2)反思與交流。經過討論,該小組同學一致認為:比較金屬與酸反應產生氫氣的快慢,有兩種測定方法:
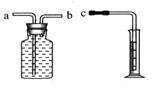
方法1是在相同時間內測量氫氣體積的大小。若用右圖所示裝置測量,則接口c應與______(填“a”或“b”)相連。
方法2是測定產生相同體積氫氣時_____________________。
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
探究性實驗是驗證化學理論的一種主要方式,也展示了化學的無窮魅力。
【提出問題】催化劑能加快反應速率,但自身質量和化學性質不變。
【查閱資料】①已知KClO3分解產生氧氣和KCl;②KClO3和KCl都能溶于水,MnO2難溶于水;③MnO2與濃鹽酸在加熱時能產生黃綠色的Cl2.
【設計實驗】
實驗一、取兩份質量相等(約5克)的KClO3分別放入兩只大試管(分別標記A和B)中,往B試管中加入質量為1.0克MnO2的,然后按圖所示組裝好儀器,加熱。結果發現加了MnO2的裝置收集滿一集氣瓶的氣體所用的時間要少。

實驗二、待裝置完全冷卻之后,將B管中物質置于燒杯中加水溶解、過濾;再將濾出物干燥、稱量得質量約為1.0克。
實驗三 、取少量濾出物與濃鹽酸置于反應裝置中(放在通風櫥中),加熱;有黃綠色氣體產生。根據以上實驗回答下列問題:
(1)實驗一說明加了MnO2之后,KClO3分解的速率更快,寫出這一反應的化學方程式:
;如何驗證集氣瓶中的氣體為氧氣 。
(2)通過上述三個實驗能說明 。
(3)某同學用KClO3和KMnO4的混合物加熱,發現產生氧氣的速度也很快,該同學就斷定KMnO4在KClO3分解反應中也能起催化作用,你認為這同學的判斷對嗎? ;為什么? 。
27.(每空1分,7分) 某化學興趣小組的同學為了探究Mg、Cu、Fe的金屬活動性順序開展了一下以下探究活動。
(1)進行試驗,獲得結論。完成如下實驗報告,并回答有關問題。
|
| 實驗方案 | 實驗現象 | 實驗結論 |
| 方 案 一 | 將Fe絲浸入CuSO4溶液中 | Fe絲表面有紅色物質析出 | 金屬活動性:Fe_ _Cu(填“>”或“<”)該反應的反應類型屬于 ____________反應。 |
| 方 案 二 | 將Mg和Cu分別在空氣中灼燒 | 發現鎂能劇烈燃燒,而另一種不能 | 金屬活動性:Mg_ _Cu(填“>”或“<”) |
| 方 案 三 | 分別將Mg和Fe放入_________中,觀察現象 | 觀察到_ (填元素符號)產生氣泡的速度較慢 | 金屬活動性順序:Mg>Fe |
 (2)反思與交流。經過討論,該小組同學一致認為:比較金屬與酸反應產生氫氣的快慢,有兩種測定方法:
(2)反思與交流。經過討論,該小組同學一致認為:比較金屬與酸反應產生氫氣的快慢,有兩種測定方法:
方法1是在相同時間內測量氫氣體積的大小。若用右圖所示裝置測量,則接口c應與______(填“a”或“b”)相連。
方法2是測定產生相同體積氫氣時_____________________。
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
 。
。| | 實驗方案 | 實驗現象 | 實驗結論 |
| 方 案 一 | 將Fe絲浸入CuSO4溶液中 | Fe絲表面有紅色物質析出 | 金屬活動性:Fe_ _Cu(填“>”或“<”)該反應的反應類型屬于 ____________反應。 |
| 方 案 二 | 將Mg和Cu分別在空氣中灼燒 | 發現鎂能劇烈燃燒,而另一種不能 | 金屬活動性:Mg_ _Cu(填“>”或“<”) |
| 方 案 三 | 分別將Mg和Fe放入_________中,觀察現象 | 觀察到_ (填元素符號)產生氣泡的速度較慢 | 金屬活動性順序:Mg>Fe |
查看答案和解析>>
科目:初中化學 來源:2012屆江西省撫州市教研室九年級上學期期末化學試卷 題型:探究題
探究性實驗是驗證化學理論的一種主要方式,也展示了化學的無窮魅力。
【提出問題】催化劑能加快反應速率,但自身質量和化學性質不變。
【查閱資料】①已知KClO3分解產生氧氣和KCl; ②KClO3和KCl都能溶于水,MnO2難溶于水;③MnO2與濃鹽酸在加熱時能產生黃綠色的Cl2.
【設計實驗】
實驗一、取兩份質量相等(約5克)的KClO3分別放入兩只大試管(分別標記A和B)中,往B試管中加入質量為1.0克MnO2的,然后按圖所示組裝好儀器,加熱。結果發現加了MnO2的裝置收集滿一集氣瓶的氣體所用的時間要少。
實驗二、待裝置完全冷卻之后,將B管中物質置于燒杯中加水溶解、過濾;再將濾出物干燥、稱量得質量約為1.0克。
實驗三 、取少量濾出物與濃鹽酸置于反應裝置中(放在通風櫥中),加熱;有黃綠色氣體產生。根據以上實驗回答下列問題:
(1)實驗一說明加了MnO2之后,KClO3分解的速率更快,寫出這一反應的化學方程式:
;如何驗證集氣瓶中的氣體為氧氣 。
(2)通過上述三個實驗能說明 。
(3)某同學用KClO3和KMnO4的混合物加熱,發現產生氧氣的速度也很快,該同學就斷定KMnO4在KClO3分解反應中也能起催化作用,你認為這同學的判斷對嗎? ;為什么? 。
27.(每空1分,7分) 某化學興趣小組的同學為了探究Mg、Cu、Fe的金屬活動性順序開展了一下以下探究活動。
(1)進行試驗,獲得結論。完成如下實驗報告,并回答有關問題。
| | 實驗方案 | 實驗現象 | 實驗結論 |
| 方 案 一 | 將Fe絲浸入CuSO4溶液中 | Fe絲表面有紅色物質析出 | 金屬活動性:Fe_ _Cu(填“>”或“<”)該反應的反應類型屬于 ____________反應。 |
| 方 案 二 | 將Mg和Cu分別在空氣中灼燒 | 發現鎂能劇烈燃燒,而另一種不能 | 金屬活動性:Mg_ _Cu(填“>”或“<”) |
| 方 案 三 | 分別將Mg和Fe放入_________中,觀察現象 | 觀察到_ (填元素符號)產生氣泡的速度較慢 | 金屬活動性順序:Mg>Fe |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com