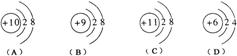
A
分析:根據(jù)稀有氣體元素的原子的結(jié)構(gòu)特點進行分析:稀有氣體的原子最外層電子數(shù)都是8個(氦為2個),都達到穩(wěn)定結(jié)構(gòu),一般情況下不宜得失電子,性質(zhì)穩(wěn)定.
解答:根據(jù)稀有氣體的原子最外層電子數(shù)的特點:原子最外層電子數(shù)都是8個(氦為2個),稀有氣體元素不易失去,也不易得到電子,由原子直接構(gòu)成.因為:原子的核外電子數(shù)=核內(nèi)質(zhì)子數(shù),故:
A、質(zhì)子數(shù)=核外電子數(shù)=2,故A正確;
B、質(zhì)子數(shù)≠核外電子數(shù),為離子,故B不符合題意;
C、雖然為原子,但為碳原子,故C錯誤;
D、質(zhì)子數(shù)≠核外電子數(shù),為離子,故D錯誤.
故選A.
點評:了解原子結(jié)構(gòu)示意圖與離子結(jié)構(gòu)示意圖的區(qū)別和聯(lián)系;熟記規(guī)律:原子核電荷數(shù)=核內(nèi)質(zhì)子數(shù)=核外電子數(shù);掌握稀有氣體元素的原子特點,







 開心蛙狀元測試卷系列答案
開心蛙狀元測試卷系列答案