
| 產品標準號:Q/JSRF0001S 準產證號:SD-013 配料表:精制食用鹽 海藻碘 亞鐵氰化鉀 氯化鈉(g/100g)≥98.00 海藻碘(以I計)/(mg/kg)18-33 亞鐵氰化鉀(以[Fe(CN)6]4-計)(mg/kg)≤10.0(2)提取金屬鎂:制取粗鹽后的苦鹵中含有豐富MgCl2等資源,如圖是從苦鹵中提取鎂的簡單流程:  上述流程中,試劑A通常用廉價的 Ca(OH)2 Ca(OH)2 (填化學式)懸濁液,沉淀B是Mg(OH)2 Mg(OH)2 ,試劑C為HCl HCl ,由無水MgCl2制取Mg的化學方程式為MgCl2
MgCl2 .
分析:根據已有的知識進行分析,從海水中獲取食鹽可以采用蒸發結晶的方法,要除去粗鹽中含有的可溶性雜質,再加入除雜試劑的時候,碳酸鈉必須加在氯化鋇的后面,以保證將過量的鋇離子除掉;根據標簽內容可以知道,每1Kg食鹽中至少含有碘元素18mg,可以計算出500g食鹽中含有碘元素的質量;根據提取鎂的方法完成此題即可. 解答:解:(1)蒸發海水達到飽和,再繼續蒸發即可得到粗鹽,要除去粗鹽中含有的可溶性雜質,再加入除雜試劑的時候,碳酸鈉必須加在氯化鋇的后面,以保證將過量的鋇離子除掉,根據標簽內容可以知道,每1Kg食鹽中至少含有碘元素18mg,可以計算出500g食鹽中含有碘元素的質量的質量為9mg,故填:蒸發,②,③,9; (2)在含有氯化鎂的苦鹵中加入氫氧化鈣能得到氫氧化鎂沉淀,氫氧化鎂與鹽酸反應生成氯化鎂,電解氯化鎂生成鎂和氯氣,故填:Ca(OH)2,Mg(OH)2,HCl,MgCl2
點評:本題考查了海水中化學資源的利用,完成此題,可以依據已有的知識進行.  
練習冊系列答案
 備戰中考寒假系列答案 備戰中考寒假系列答案
相關習題
科目:初中化學 來源: 題型: 13、海洋是巨大的資源寶庫.請你運用學過的知識回答下列問題: (1)人類所需要的下列物質,可以從海洋中獲取的是( D )①石油,②金屬礦物,③無機鹽,④淡水,⑤海洋生物,⑥可燃冰 A.①③④⑤B.①②③⑤C.③④⑤⑥D.全部 (2)人類要獲取所需要的物質,都要選擇適當的方法.請你從下列A~F中選擇一種方法,把相應的字母代號填在①~⑥前的括號內. A.蒸發結晶法 B.蒸餾法 C.過濾法 D.化學沉淀法 E.中和法 F.電解法 ①從海水中獲取淡水 B ;②從海水中獲取粗鹽 A ;③除去粗鹽中不溶性的雜質 C ;④在粗鹽純化過程中,要除去氯化鈉溶液中的少量硫酸鈉 D ;⑤在粗鹽純化過程中,要調節溶液的酸堿性 E ;⑥以氯化鎂為原料制取金屬鎂 F .(3)在上述A~F的方法中,運用了化學變化原理的有(填字母代號) DEF ;(4)對下列實驗方法的理解,不正確的是 D .A.過濾與篩子的原理是類似的,都是把顆粒大小不同的物質分離開 B.蒸發就是使液體中的分子在外界條件的影響下逸出液面 C.蒸餾就是使液體中的分子在外界條件的影響下逸出液面再重新凝結為液體 D.結晶就是利用合適的試劑把溶液中的溶質轉化為沉淀析出. 查看答案和解析>> 科目:初中化學 來源: 題型:閱讀理解 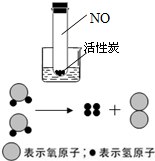 3月22日是“世界水日”,2011年“世界水日”的宣傳主題為:“城市用水:應對都市化挑戰”.水與人類的生活和生產密切相關.請回答以下相關問題: 3月22日是“世界水日”,2011年“世界水日”的宣傳主題為:“城市用水:應對都市化挑戰”.水與人類的生活和生產密切相關.請回答以下相關問題:(一)水--常用的化學試劑 (1)為驗證活性炭的吸附能力和溫度的關系,某同學將底部裝有活性炭顆粒、充滿紅棕色NO2氣體(有毒氣體)的試管插入盛有水的燒杯中(如圖),然后向燒杯中加入NH4NO3,觀察到試管中紅棕色慢慢變淡至褪色,說明 溫度越低,活性炭的吸附能力越好 溫度越低,活性炭的吸附能力越好 ;(2)電解水時,需在水中加入少量氫氧化鈉或硫酸,目的是 為了增強水的導電性 為了增強水的導電性 ,如圖是實驗室電解水的微觀示意圖,其中最小的微粒是原子 原子 ,通過該實驗可以得出的結論是水是由氫元素和氧元素組成的 水是由氫元素和氧元素組成的 .(二)海水--人類的資源寶庫 (1)獲取淡水:將海水轉化為淡水,最常用的操作方法是 蒸餾法 蒸餾法 ;(2)獲取NaCl:將海水進行 蒸發 蒸發 可得到粗鹽;為除去粗鹽中含有的Na2SO4、CaCl2等雜質,可依次進行下列操作:①溶解;②加過量的BaCl2溶液; ③加過量的Na2CO3溶液;④過濾;⑤加適量的X溶液;⑥蒸發結晶.其中適量X溶液是稀鹽酸 稀鹽酸 (填名稱);(3)提取金屬鎂:海水中含有豐富的鎂元素,如圖是從海水中提取鎂的簡單流程: 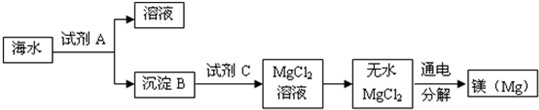 上述流程中,沉淀B是Mg(OH)2,則試劑A可以用 氫氧化鈣 氫氧化鈣 溶液,試劑C的化學式為HCl HCl ,由無水MgCl2制取Mg的化學方程式為MgCl2
MgCl2 ,屬于
分解 分解 反應.(三)清潔衛生的水--人類需要 (1)保護運河,我提建議:①生活污水處理后排放;②將工廠廢液排入運河;③使用無磷洗衣粉,④減少燃放煙花爆竹 ⑤及時清理運河中瘋長的藻類.你認為以上建議中可以采納的是 ①③④⑤ ①③④⑤ (填序號);(2)以下是污水處理成自來水的工藝流程示意圖: 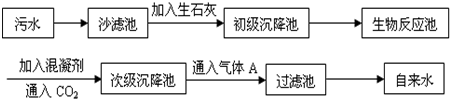 ①污水中含Ca2+、Mg2+、HCO3-等,加入生石灰后生成Ca(OH)2,進而發生若干復分解反應,初級沉降池中生成的主要沉淀是 碳酸鈣 碳酸鈣 和碳酸鎂 碳酸鎂 ;(MgCO3微溶于水)②通入CO2除了能調節自來水的pH,還能 除去過量的氫氧化鈣 除去過量的氫氧化鈣 ;③生物反應池是利用微生物直接分解水中的有機物,以除去水中過多的氮、磷等有害成分.這樣做的優點是 不會產生污染,比較環保 不會產生污染,比較環保 ;④工藝中的混凝劑常用 明礬 明礬 ,其除去懸浮固體小顆粒的過程A A ;(填編號)A.只是物理過程 B.只是化學過程 C.是物理和化學過程 ⑤氣體A是 Cl2 Cl2 (填化學式),其作用是殺菌消毒,使自來水符合衛生標準;⑥俗話說:“大災之后必有大疫”,這主要是因為災民飲用了含有大量的細菌和雜質的水后,很容易患腸道傳染病.請你設計合理方案,將被污染的水處理成能飲用的水: 加入明礬凈水、然后過濾、用氯氣殺菌消毒、最后加熱煮沸 加入明礬凈水、然后過濾、用氯氣殺菌消毒、最后加熱煮沸 .查看答案和解析>> 科目:初中化學 來源: 題型:解答題 海水是人類的資源寶庫,從海水中可獲得多種產品. |
| 產品標準號:Q/JSRF0001S 準產證號:SD-013 配料表:精制食用鹽 海藻碘 亞鐵氰化鉀 氯化鈉(g/100g)≥98.00 海藻碘(以I計)/(mg/kg)18-33 亞鐵氰化鉀(以[Fe(CN)6]4-計)(mg/kg)≤10.0 |

查看答案和解析>>
科目:初中化學 來源:2012-2013學年江蘇省揚州市邗江中學九年級(上)期末化學試卷(解析版) 題型:填空題
| 產品標準號:Q/JSRF0001S 準產證號:SD-013 配料表:精制食用鹽 海藻碘 亞鐵氰化鉀 氯化鈉(g/100g)≥98.00 海藻碘(以I計)/(mg/kg)18-33 亞鐵氰化鉀(以[Fe(CN)6]4-計)(mg/kg)≤10.0 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com