

分析 (1)根據碳酸鈉的作用進行解答;
(2)將沉淀從溶液中分離用過濾,室進行該操作時使用玻璃棒的作用是引流;根據反應情況判斷溶液中的溶質;
(3)根據工業制純堿的反應進行解答;
(4)根據碳酸氫鈉受熱分解生成物為碳酸鈉、水和二氧化碳分析;
(5)根據沉淀的質量計算碳酸鈉的質量,從而計算碳酸鈉的質量分數,判斷產品的等級.
解答 解:(1)流程圖Ⅰ是依次向粗鹽水中加入Ca(OH)2和Na2CO3,二者加入的順序不能顛倒,如果顛倒,過量的氫氧化鈣和新生成的氯化鈣無法除去;
(2)將沉淀從溶液中分離用過濾,室進行該操作時使用玻璃棒的作用是引流;流程Ⅰ中發生的反應有:Na2CO3+CaCl2═CaCO3↓+2NaCl、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,碳酸鈉過量,故過濾后所得溶液的溶質是:氯化鈉、氫氧化鈉、碳酸鈉;
(3)碳酸氫鈉達到一定濃度時,會首先從溶液中結晶析出,說明此時碳酸氫鈉的溶解度小于氯化銨;根據氯化鈉、水、氨氣和二氧化碳反應生成碳酸氫鈉和氯化銨,發生的總反應:NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl;
(4)碳酸氫鈉受熱分解生成物為碳酸鈉、水和二氧化碳,化學方程式為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(5)設產生19.7g碳酸鋇沉淀需要碳酸鈉的質量為 x
Na2CO3+Ba(OH)2═BaCO3↓+2NaOH
106 197
x 19.7g
$\frac{106}{197}=\frac{x}{19.7g}$
解之得:x=10.6g
所以樣品中Na2CO3質量分數為:$\frac{10.6g}{10.65g}$×100%=99.5%>99.2%,因此屬于優等品.
故答案為:(1)如果顛倒,過量的氫氧化鈣和新生成的氯化鈣無法除去;
(2)過濾;引流;氯化鈉、氫氧化鈉、碳酸鈉;
(3)小于;NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl;
(4)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(5)屬于優等品.
點評 本題考查利用課本知識解決新問題能力,能加深學生對課本知識的理解,訓練學生的思維能力.


科目:初中化學 來源: 題型:選擇題
| A. | “溫室效應”、“酸雨”、“臭氧空洞”等環境問題都是由大氣污染引起的 | |
| B. | 常溫下某物質的飽和溶液降溫后,可能仍然飽和 | |
| C. | 催化劑的作用是加快化學反應速率 | |
| D. | 植物生長需要較多的營養元素是氮、磷、鉀 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | FeSO4、Cu、Ag、稀硫酸 | B. | Cu、FeSO4溶液、AgNO3溶液 | ||
| C. | Fe、Ag、CuSO4溶液 | D. | Fe、Cu、稀硫酸、AgNO3溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
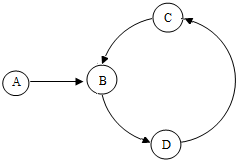 已知A、B、C、D是四種不同類別的物質且含有同一種元素,B在常溫下為液體,C為一種難溶性鹽,它們的轉化關系如圖所示.
已知A、B、C、D是四種不同類別的物質且含有同一種元素,B在常溫下為液體,C為一種難溶性鹽,它們的轉化關系如圖所示.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com