
【題目】實驗室制取氣體時需要的一些裝置如下圖所示,請回答下列問題。
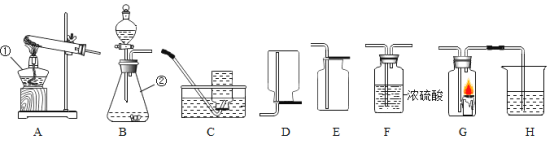
(1)寫出標有序號②的儀器名稱:②_________。
(2)實驗室制取氧氣和二氧化碳的發生裝置都可選用B裝置的原因是_______,裝置中使用分液漏斗的優點是________。
(3)若要得到干燥的氧氣,所選擇裝置的連接順序為:B→_____→_____(填字母序號)。
(4)某興趣小組的同學連接B、G、H裝置進行實驗。若實驗時G裝置中蠟燭燃燒更劇烈,H裝置中溶液變渾濁,則B裝置中反應的化學方程式為________。
【答案】錐形瓶 反應物是固體和液體,反應不需要加熱 可以控制反應速率,節約藥品 F E 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
(1)②的儀器是錐形瓶。
(2)B裝置適用于固體和液體且不需加熱制取氣體,故B裝置適用于過氧化氫和二氧化錳制氧氣,也適于石灰石和稀鹽酸制二氧化碳。裝置中使用分液漏斗的優點是可以控制反應速率,節約藥品,因為B裝置中的分液漏斗可以調液體的滴加速度,也就控制了反應物的量及反應速率。
(3)若要得到干燥的氧氣,在收集氧氣前,先用濃硫酸對氧氣進干燥,再用向上排空氣法收集,所以選擇裝置的連接順序為:B→F→E。
(4)如果B、G、H裝置進行實驗,實驗時G裝置中蠟燭燃燒更劇烈,說明B裝置制取的氣體是氧氣,蠟燭在氧氣中燃燒產生二氧化碳使H裝置中澄清石水變渾濁。故B裝置是過氧化氫和二氧化錳生成氧氣和水,化學方程式為2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。


科目:初中化學 來源: 題型:
【題目】向一定質量的AgNO3和Cu(NO3)2的混合溶液中加入鐵粉,反應過程中,測得混合物中溶液的質量與加入鐵粉的質量關系如圖所示。有關該反應過程中的下列說法正確的是
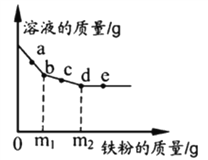
A. a點,向溶液中滴加稀鹽酸,無白色沉淀
B. c點,向過濾后得到的固體中滴加稀鹽酸,無氣泡產生
C. d點,溶液中的溶質為Fe(NO3)2和Cu(NO3)2
D. e點,過濾后得到的固體中只含有2種物質
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖是a、b、c三種物質的溶解度曲線,據圖回答下列問題:
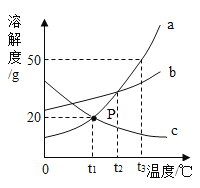
(1)三種物質的溶解度隨著溫度升高而減小的是______。
(2)t3℃時,把80 g物質a加入200g水中充分攪拌、靜置,形成的是__________(填“飽和”或“不飽和”)溶液。
(3)t3℃時,將等質量a和b的飽和溶液降到t1℃時,析出晶體的質量關系正確的是______(填字母序號)。
A a>b
B a=b
C a<b
D 不能確定
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列圖像能正確反映其對應變化關系的是( )
A.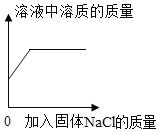 表示同一溫度下向飽和NaCl溶液中加入固體NaCl,溶液中溶質的質量變化
表示同一溫度下向飽和NaCl溶液中加入固體NaCl,溶液中溶質的質量變化
B.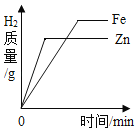 分別向等質量的鐵粉和鋅粉中加入過量的相同質量分數的稀硫酸
分別向等質量的鐵粉和鋅粉中加入過量的相同質量分數的稀硫酸
C.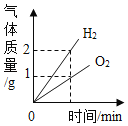 表示水電解實驗中生成氫氣與氧氣質量比
表示水電解實驗中生成氫氣與氧氣質量比
D.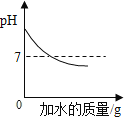 向一定溶質質量分數的氫氧化鈉溶液中不斷加水
向一定溶質質量分數的氫氧化鈉溶液中不斷加水
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某化學課堂圍繞“酸堿中和反應”,將學生分成若干小組開展探究活動。請你和他們一起完成以下實驗探究。
(演示實驗)將一定量稀鹽酸加入到盛氫氧化鈣溶液的小燒杯中。該反應的化學方程式是_____________。
(查閱資料)CaC12 滾液顯中性
(提出問題)實驗中未觀察到明顯現象,部分同學產生了疑問:反應后溶液中溶質的成分是什么?
(猜想與假設)針對疑問,甲組同學猜想如下:
猜想I:只有CaC12
猜想II:有__________
猜想III:有CaC12和Ca(OH)2
猜想IV:有CaCl2、HCl和Ca(OH)2
乙組同學對以上猜想提出質疑,認為猜想IV不合理,其理由是_________。
(實驗探究)為了驗證其余猜想,各小組進行了下列三個方案的探究。
實驗方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
實驗操作 |
|
|
|
實驗現象 | ____________ | __________ | 產生白色沉淀 |
實驗結論 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出結論)通過探究,全班同學一致確定猜想III是正確的。
(評價反思) (1)丙組同學認為滴加Na2CO3溶液產生白色沉淀,并不能證明溶液中一定含有Ca(OH)2,請你幫助他們說明原因____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】除去下列物質中混有的雜質,所用試劑和操作方法不正確的
選項 | 物質 | 所含雜質 | 除雜質選用的試劑或方法 |
A | NaCl溶液 | NaOH | 加入適量的稀鹽酸 |
B | Cu | Fe | 加入足量的稀鹽酸并過濾 |
C | CO2 | CO | 在氧氣中點燃 |
D |
| CaCl2固體 | 加入足量的水溶解并過濾、洗滌、干燥 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列有關敘述對應的化學方程式、所屬基本反應類型都正確的是( )
A.實驗室制氫氣:Zn + 2HNO3=Zn(NO3)2+H2↑ 置換反應
B.保存碳銨時應避光放在陰涼處: (NH4)2CO3=2NH3↑ + H2O + CO2↑ 分解反應
C.鹽酸除水垢的反應之一:2HCl + CaCO3=CaCl2 + CO2↑ + H2O 復分解反應
D.拉瓦錫探究質量守恒定律:2HgO=2Hg + O2↑ 分解反應
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】金屬在生產生活中其中起著巨大的作用。
(1)鋁可以用來制作炊具,這是利用了鋁的___________性。
(2)相比于黃鐵礦(主要成分FeS2),工業上選赤鐵礦(主要成分Fe2O3)為原料煉鐵的優點是______。
(3)小華同學利用如圖實驗探究金屬的性質,請你一起完成。

①圖A中集氣瓶內放入少量水的目的是___, D中除了出現鐵片逐漸溶解,還出現的現象是______。
②圖F中的物質M屬____________(填物質類別);
③如果只用一種溶液就能比較鋁、鐵、銅的金屬活動性強弱,則這種試劑是_______。
(4)為測定某鎂銅合金(假定不含其它雜質)中鎂的質量分數,小李取一塊質量為10克的鎂銅合金,放入燒杯中,向其中加入足量的稀鹽酸完全反應,反應后過濾,向濾液中加入過量的氫氧化鈉溶液,反應后過濾得沉淀,經洗滌、干燥后稱量質量為8.7克,則該合金中鎂的質量分數為多少_______? (寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某研究性學習小組在做“鎂與稀鹽酸反應”的實驗時,發現一個意外現象,試管底部有灰白色沉淀生成。
[提出問題]出現灰白色沉淀是否為偶然現象?
[設計實驗]實驗1:向4份相同體積與濃度的稀鹽酸中分別加入一定長度的鎂帶。
試管 | A | B | C | D |
鎂帶長度 | 1 cm | 2cm | 3 cm | 4cm |
實驗現象 | 快速反應產生大量氣泡,試管發熱。最終鎂帶溶解 | 快速反應產生大量氣泡,試管發熱,鎂帶溶解,出現少量白色渾濁 | 快速反應產生大量氣泡,試管發熱,鎂帶溶解,出現灰白色沉淀 | 快速反應產生大量氣泡,試管發熱,鎂帶溶解,溶液變渾濁,久置得大量灰白色沉淀 |
沉淀量 | 無沉淀生成 | 少量沉淀 | 沉淀較多 | 沉淀很多 |
據表分析,______是實驗出現“異常”的主要因素寫出產生氣泡反應的化學方程式____,實驗前用砂紙打磨鎂條的原因是______。
實驗2:將少量灰白色沉淀用蒸溜水清洗并室溫晾干。然后取樣,按圖加熱固體,用濕潤的藍色石蕊試紙檢驗氣體產物試紙變紅;若另取一端用硝酸銀溶液浸潤的玻璃棒懸于試管口,出現白色渾濁,則灰白色沉淀中一定含有______元素。
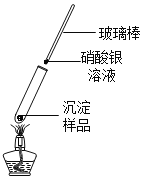
用pH計監測反應過程中溶液pH變化并讀數。實驗結果如下:
時間/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 | … | 放置過夜 |
溶液pH | 2.0 | 5.8 | 7.4 | 8.0 | 8.6 | 9.0 | 9.3 | 9.6 | 9.8 | 10.0 | 10.0 | … | 10.2 |
實驗現象 | 一 | 大量氣泡,無沉淀生成 | 鎂帶慢慢溶解,氣泡量減少 ,溶液變渾濁,燒杯內灰白色沉淀逐漸增加 | ||||||||||
氣泡減慢的原因是______,充分反應后溶液的pH____(填“>”、“<”或“=”)7。
[實驗拓展]鎂與稀鹽酸反應時.試管中還出現白霧。哪種因素會促進反應過程中出現白霧?請設計實驗進行驗證。
影響因素:____________。
實驗驗證:____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com