
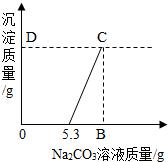
 有鹽酸和氯化鈣混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀與加入的Na2CO3質(zhì)量關系如圖.若CaCl2在混合液中的質(zhì)量分數(shù)為5.55%.
有鹽酸和氯化鈣混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀與加入的Na2CO3質(zhì)量關系如圖.若CaCl2在混合液中的質(zhì)量分數(shù)為5.55%.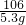 =
=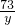
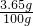 ×100%=3.65%
×100%=3.65%  =
=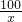 =
=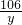


 波波熊暑假作業(yè)江西人民出版社系列答案
波波熊暑假作業(yè)江西人民出版社系列答案 學而優(yōu)暑期銜接南京大學出版社系列答案
學而優(yōu)暑期銜接南京大學出版社系列答案 Happy holiday歡樂假期暑假作業(yè)廣東人民出版社系列答案
Happy holiday歡樂假期暑假作業(yè)廣東人民出版社系列答案科目:初中化學 來源: 題型:
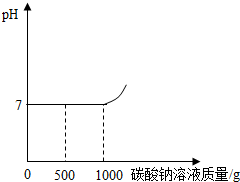
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
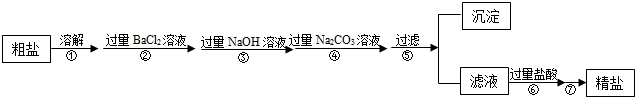
查看答案和解析>>
科目:初中化學 來源: 題型:
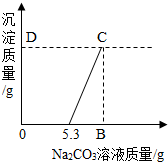 有鹽酸和氯化鈣混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀與加入的Na2CO3質(zhì)量關系如圖.若CaCl2在混合液中的質(zhì)量分數(shù)為5.55%.
有鹽酸和氯化鈣混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀與加入的Na2CO3質(zhì)量關系如圖.若CaCl2在混合液中的質(zhì)量分數(shù)為5.55%.查看答案和解析>>
科目:初中化學 來源: 題型:
有鹽酸和氯化鈣的混合溶液l00g,向混合溶液中逐滴加入10%的![]() 溶液,生成沉淀的質(zhì)量與加入
溶液,生成沉淀的質(zhì)量與加入![]() 溶液的質(zhì)量關系如圖。若
溶液的質(zhì)量關系如圖。若![]() 在混合液中的質(zhì)量分數(shù)為5.55%。求:
在混合液中的質(zhì)量分數(shù)為5.55%。求:
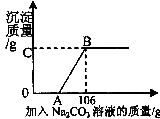
(1)在實驗過程中,有沉淀生成,還可以看到的明顯現(xiàn)象是___________
(2)C點的縱坐標所表示的質(zhì)量。
(3)原混合液中HCl的質(zhì)量分數(shù)。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com