
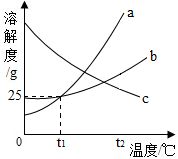
 如圖為a、b、c三種物質(均不含結晶水)的溶解度曲線,據圖回答下列問題.
如圖為a、b、c三種物質(均不含結晶水)的溶解度曲線,據圖回答下列問題.分析 ①據該溫度下a的溶解度分析解答;
②據溶解度曲線可比較同一溫度下不同物質的溶解度大小;
③據物質的溶解度隨溫度變化情況及飽和溶液中溶質的質量分數分析解答.
解答 解:①t1℃時a的溶解度是25g,即100g水中最多溶解25g的a,則50g水中最多可溶解a物質12.5g;
②t2℃時,a、b、c三種物質溶解度由大到小的順序是a>b>c;
③將t1℃時a、b、c三種物質的飽和溶液升溫至t2℃時,ab溶解度增大,溶液中溶質、溶劑質量不變,溶質的質量分數不變,c的溶解度減小,析出晶體,溶質的質量分數減小;飽和溶液中溶質的質量分數=$\frac{溶解度}{溶解度+100g}$×100%,即溶解度大則溶質的質量分數大,而升溫前a的溶解度=b的溶解度,均小于升溫后c的溶解度,所以三種溶液的溶質質量分數大小是a=b<c;
故答案為:①12.5 ②a>b>c ③a=b<c
點評 本題難度不是很大,主要考查了固體物質的溶解度曲線所表示的意義及根據溶解度曲線解決相關的問題,從而培養學生分析問題、解決問題的能力.


科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
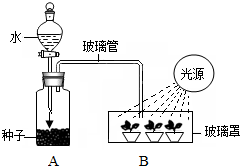 如圖中A與B兩裝置分別表示種子和幼苗進行的生理作用,A、B裝置間用玻璃管連接.請據圖回答:
如圖中A與B兩裝置分別表示種子和幼苗進行的生理作用,A、B裝置間用玻璃管連接.請據圖回答:查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 化學興趣小組對實驗室藥品柜中的一瓶鹽酸的性質和質量分數進行探究,請你參與:
化學興趣小組對實驗室藥品柜中的一瓶鹽酸的性質和質量分數進行探究,請你參與:| 實驗步驟 | 預計實驗現象 |
| 取少量溶液于試管中,滴加石蕊試液 | 溶液變紅色 |
| 另取少量溶液于試管中,把鎂條伸入溶液中 | 產生氣泡 |

查看答案和解析>>
科目:初中化學 來源: 題型:多選題
| A. | 蒸發濾液時,待蒸發皿中出現較多固體后可進行間歇加熱,盡量將水分蒸干 | |
| B. | 配制氯化鈉溶液需要經過計算、稱量、量取、溶解、裝液、貼標簽等步驟 | |
| C. | 粗鹽溶解和進行過濾操作時,都用到玻璃棒,但玻璃棒的作用不同 | |
| D. | 配制溶液時必備的儀器有托盤天平、滴管、藥匙、酒精燈、量筒、燒杯、玻璃棒等 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | HClO4、KClO3 | B. | KClO、KCl | C. | NaClO、KCl | D. | NaCl、KC1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com