
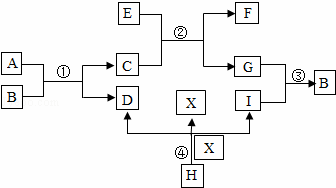
已知A、B、C、D、E、F、G、H、I、X均為初中化學常見的物質.其中E、G為常見金屬單質,E是目前世界上產量最高的金屬,G呈紫紅色,I是地殼中含量最高的元素所形成的常見氣體單質;人體胃液中含有A,可幫助消化.根據如圖所示的轉化關系,回答下列問題.(圖中反應條件均已略去,反應物和產物均已給出)
(1)E的名稱是 ,H的化學式是 ;X的作用 .
(2)寫出反應 ②的化學方程式: ;
②的化學方程式: ;
(3)實驗室檢驗I氣體的方法: .
| 物質的鑒別、推斷;常見氣體的檢驗與除雜方法;化學式的書寫及意義;書寫化學方程式、文字表達式、電離方程式 | |
| 專題: | 框圖型推斷題. |
| 分析: | 根據G為紫紅色金屬,為銅;而E為目前世界上產量最高的金屬,為鐵;I是地殼中含量最高的元素形成的常見氣體單質,所以為氧氣;A在人體胃液中可以幫助消化,所以為鹽酸,據此解答. |
| 解答: | 解:根據題意:G為“紫紅色金屬”,為銅;而“E為目前世界上產量最高的金屬”,為鐵;“I是地殼中含量最高的元素形成的常見氣體單質”,所以為氧氣.A“在人體胃液中可以幫助消化”,所以為鹽酸.由于銅(G)可以和氧氣(I)反應生成B,所以B為氧化銅.則A和B反應生成C和D為鹽酸和氧化銅反應生成水和氯化銅,而C能夠和鐵反應,所以C為氯化銅,D為水.H能夠生成水和氧氣,所以H為過氧化氫.而E、C反應即為鐵與氯化銅的反應生成氯化亞鐵(F)和銅(G). 所以轉化關系為:
因此:(1)E為鐵; H為過氧化氫,化學式為:H2O2;X是過氧化氫分解的催化劑,起到催化作用;故答案為:鐵; H2O2; (2)反應②是鐵和氯化銅反應產生氯化亞鐵和銅,故反應的方程式為:Fe+CuCl2═Cu+FeCl2; (3)檢驗氧氣用帶火星的木條,看是否復燃;故答案為:將帶火星的木條伸入試管或集氣瓶中,木條復燃,證明是氧氣. |
| 點評: | 本題為框圖式物質推斷題,完成此題,關鍵是根據題干敘述直接得出有關物質的化學式,然后根據物質間的轉化,順推或逆推得出其他物質的化學式. |


科目:初中化學 來源: 題型:
請用相關序號填空:
可選物質:A. 蛋白質,B. 小蘇打,C. 鐵粉,D. 熟石灰,E. 硝酸鉀,F. 硫酸銅
(1)治療胃酸過多 ; (2)食品袋中的“雙吸劑”
(3)牛奶中的主要營養物質是 (4)能用于改良酸性土壤的是
(5)能用于配制波爾多液的鹽是 (6)常見的復合肥是
查看答案和解析>>
科目:初中化學 來源: 題型:
化學方程式是重要的“化學語言”,下列化學方程式與文字表述均正確的是( )
|
| A. | 濃氨水遇濃鹽酸產生白霧:NH3+HCl═NH4Cl |
|
| B. | 用稀鹽酸除去鐵銹:Fe2O3+4HCl═2FeCl2+2H2O |
|
| C. | 實驗室制備CO2:CaCO3+2HCl═CaCl2+CO2↑+H2O |
|
| D. | 甲醇不充分燃燒:2CH3OH+3O2 |
查看答案和解析>>
科目:初中化學 來源: 題型:
下列除去物質所含雜質的方法不正確的是(括號內為雜質)( )
|
| A. | MnO2(KCl),加足量水溶解,過濾,洗滌,干燥 |
|
| B. | N2(O2),將氣體緩緩通過灼熱的銅網 |
|
| C. | FeSO4溶液(CuSO4),加過量Fe粉,過濾 |
|
| D. | CO2(HCl),通過NaOH溶液后用濃硫酸干燥 |
查看答案和解析>>
科目:初中化學 來源: 題型:
重鉻酸鉀(K2Cr2O7Mr=294,鉻元素為+6價,Mr表示相對分子質量)是一種重要的化工原料,在皮革工業、有機反應中都有廣泛應用.但+6價格有很強的毒性易污染環境,使用后,須用綠礬,(FeSO4•7H2O,Mr=278)將其變成毒性+3價格才能做后續處理.反應原理是:6FeSO4•7H2O+K2Cr2O7+7H2SO4═3Fe2(SO4)3+Cr2(SO4)3+K2SO4+49H2O現有1.0噸重鉻酸鉀需要處理,計算需綠礬多少噸?(寫出計算過程,結果精確到小數點后1位)
查看答案和解析>>
科目:初中化學 來源: 題型:
下列說法中正確的是( )
|
| A. | 嘗藥品的味道 |
|
| B. | 實驗剩余的藥品放回原試劑瓶中 |
|
| C. | 加熱試管里的液體時,試管口不能朝著自己或他人 |
|
| D. | 稀釋濃硫酸時,把水注入濃硫酸,并不斷攪拌 |
查看答案和解析>>
科目:初中化學 來源: 題型:
在研究酸和堿的化學性質時,某小組想證明稀硫酸與氫氧化鈉溶液混合后,雖然無明顯現象,但確實發生了化學反應,試與他們一起完成實驗方案的設計,實施和評價,并得出有關結論.
(1)探究稀硫酸與氫氧化鈉溶液的反應:
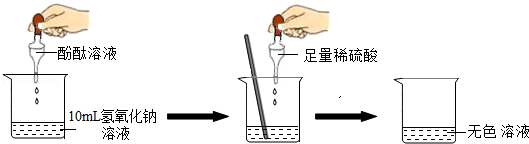
當滴入幾滴酚酞試液后,溶液由無色變為 色,根據上述實驗中顏色變化,可確定稀硫酸與氫氧化鈉溶液發生了化學變化,反應的化學方程式為:.
(2)探究上述稀硫酸與氫氧化鈉溶液反應后燒杯中的硫酸是否過量:
根據上述反應過程中溶液變成無色,不能確定稀硫酸是否過量,同學們又分別選取氯化鋇溶液、紫色石蕊試液設計實驗方案,請你判斷并分析:
| 實驗方案 | 實驗步驟 | 實驗現象 | 實驗結論 |
| 方案一 | 取樣,滴入適量的氯化鋇溶液 | 出現白色沉淀 | 稀硫酸過量 |
| 方案二 | 取樣,滴入幾滴紫色石蕊試液 | 溶液變紅 | 稀硫酸過量 |
上述設計的實驗方案中,正確的是 (填“方案一”或“方案二”)
另外一個實驗方案錯誤的原因是 ;
請你設計一個確定稀硫酸是否過量的實驗方案,你選用的藥品是 ,實驗現象及結論是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com