
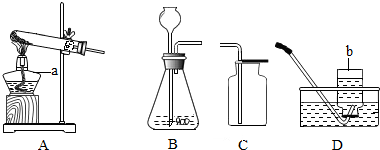
分析 (1)據常用儀器的名稱解答;
(2)據實驗室用氯酸鉀制取氧氣的原理解答;
(3)實驗室用鋅粒與稀硫酸反應生成氫氣和硫酸鋅;氫氣密度比空氣小,不易溶于水,可用排水法收集;
(4)利用98%的濃硫酸配制10%的稀硫酸,即加水進行稀釋,根據稀釋前后溶液中硫酸的質量不變,利用這一不變量進行計算;據稀釋的步驟解答;
(5)氧化鐵和鹽酸反應生成氯化鐵和水,反應后溶液是氯化鐵溶液,反應后溶液中溶質的質量分數的計算,可根據化學方程式求溶質的質量,溶液的質量可根據公式:“反應后溶液的質量=反應前加入的所有物質質量之和-雜質的質量-氣體的質量-沉淀的質量”來求出,結合已知量和方程式進行計算即可.
解答 解:(1)裝置圖中標號儀器的名稱是a酒精燈;
(2)實驗室用氯酸鉀制取氧氣的原理為:2KClO3$\frac{\underline{MnO_2}}{△}$ 2KCl+3O2↑;
(3)實驗室用鋅粒與稀硫酸反應生成氫氣和硫酸鋅,反應的方程式為Zn+H2SO4═ZnSO4+H2↑;氫氣密度比空氣小,不易溶于水,可用排水法收集;
(4)解:設需要溶質質量分數為98%的濃硫酸x,則
180g×10%=1.84g/mLx×98%,
x≈10.0mL
答:需濃硫酸的體積是10.0mL.
由濃溶液配制稀溶液時,計算的依據是溶液稀釋前后,溶質的質量不變;在實驗室用濃硫酸配制稀硫酸的主要步驟有 計算、量取、混勻、冷卻至室溫裝瓶并貼上標簽.
(5)氧化鐵和鹽酸可發生反應,所以剩余后的濾渣是樣品中的雜質,赤鐵礦石中氧化鐵的質量分數為:$\frac{(10g-2g)}{10g}$×100%=80%;
氧化鐵的質量是8g,設反應生成氯化鐵的質量為x
Fe2O3+6HCl═2FeCl3+3H2O
160 325
8g x
$\frac{160}{8g}$=$\frac{325}{x}$
x=16.25g
$\frac{16.25g}{(127.4+8)g}$×100%=12%;
答:赤鐵礦石中氧化鐵的質量分數為80%,反應后溶液中溶質的質量分數約為12%;
故答案為:(1)長頸漏斗;
(2)2KClO3$\frac{\underline{MnO_2}}{△}$ 2KCl+3O2↑;
(3)Zn+H2SO4═ZnSO4+H2↑、BD;
(4)10.0、溶液稀釋前后,溶質的質量不變、量取.
(5)氧化鐵和鹽酸可發生反應,所以剩余后的濾渣是樣品中的雜質,赤鐵礦石中氧化鐵的質量分數為:$\frac{(10g-2g)}{10g}$×100%=80%;
氧化鐵的質量是8g,設反應生成氯化鐵的質量為x
Fe2O3+6HCl═2FeCl3+3H2O
160 325
8g x
$\frac{160}{8g}$=$\frac{325}{x}$
x=16.25g
$\frac{16.25g}{(127.4+8)g}$×100%=12%;
答:赤鐵礦石中氧化鐵的質量分數為80%,反應后溶液中溶質的質量分數均為12.0%.
點評 本題主要考查了儀器的名稱、氧氣、氫氣的制取原理等,實驗設計的問題,有關實驗方案的設計和對實驗方案的評價是中考的熱點之一,解答計算時要據物質的性質和方程式細心分析解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 化學變化中分子、原子都可分 | B. | 原子是化學變化中的最小粒子 | ||
| C. | 花香四溢說明分子間有間隔 | D. | 分子可以構成物質,原子不能 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
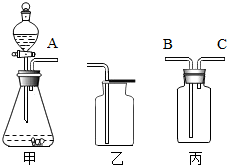 如圖是實驗室常用裝置.
如圖是實驗室常用裝置.查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 房屋倒塌 | B. | 堰塞湖形成 | C. | 震區消毒殺菌 | D. | 山體滑坡 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 將生銹鐵釘投入稀鹽酸中,溶液逐漸變黃,并有氣泡產生 | |
| B. | 硫酸銅、石灰水配制的農藥波爾多液不能用鐵制容器盛放 | |
| C. | 工業煉鐵的原理是利用CO將鐵從鐵的氧化物中置換出來 | |
| D. | “暖寶寶”的化學原理是利用鐵粉緩慢氧化放出熱量 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 計算:需要3g氯化鈉,50ml水 | |
| B. | 稱取:用托盤天平稱量所需的氯化鈉 | |
| C. | 量取:用100mL量筒量取所需的水 | |
| D. | 溶解:將稱得的氯化鈉倒入量筒溶解 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com