
在化學反應A2+BC=B+A2C中,反應物BC與生成物 B的質量關系如圖所示。將2g A2與80g BC恰好完全反應,則生成A2C的質量是
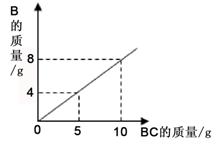
A.64g
B.18g
C.80g
D.9g
科目:初中化學 來源: 題型:
氯氣是一種有毒的氣體,實驗室制取氯氣時,可以用氫氧化鈉溶液來吸收尾氣,其反應原理為Cl2 + 2NaOH = X + NaClO + H2O, 則X 的化學式為
A. NaCl B. H2 C. HCl D. HClO
查看答案和解析>>
科目:初中化學 來源: 題型:
下圖是某同學完成《實驗活動5 一定質量分數的氯化鈉溶液的配制》中“配制
50 g質量分數為6%的氯化鈉溶液”的全過程。
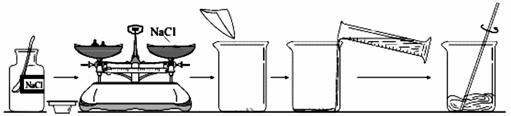
(1)圖中的錯誤有:
① ;
② 。
(2)若所配制的鹽水中NaCl 的質量分數小于6%,則可能造成誤差的原因有(至少舉
出兩點)。
① ;
②  。
。
(3)由濃溶液配制稀溶液時,計算的依據是 。要把50 g質量分數為98%的濃硫酸稀釋為質量分數為20%的硫酸,需要水的質量是 。在實驗室用濃硫酸配制稀硫酸的主要步驟有:計算、 、混勻、冷卻至室溫裝瓶并貼上標簽。
(4)取某稀硫酸樣品10g,將5%的NaOH溶液逐滴加入到樣品中,邊加邊攪拌。溶液pH的變化如圖所示。試回答:

①a點溶液中含有的離子有 。
②當pH=7時,消耗NaOH溶液中NaOH的質量為 g。
③計算稀硫酸的溶質質量分數。(寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
某研究性學習小組在實驗中發現:不僅堿溶液可以使酚酞溶液變紅,Na2CO3溶液也能使酚酞溶液變紅。堿溶液可以使酚酞溶液變紅是因為堿在水溶液中解離出OH-,那么Na2CO3溶液中究竟是哪種粒子可以使酚酞溶液變紅呢?為此他們設計了如下圖所示的3個實驗,請你和他們一起探究。
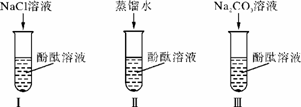
(1)實驗Ⅰ可以證明____________________________________。
(2)實驗Ⅱ加入蒸餾水的目的是____________________________;小組內有同學認為實驗Ⅱ沒必要做,你認為他們的理由是______________________________________。
(3)實驗Ⅲ滴入Na2CO3溶液,振蕩,酚酞溶液變紅,向變紅后的溶液中再逐漸滴入過量的CaCl2溶液,紅色逐漸消失,同時還觀察到___ __________________________________。
__________________________________。
由實驗Ⅰ、Ⅱ、Ⅲ得出結論:CO32-可以使酚酞溶液變紅。
(4)小組同學在與老師交流上述結論時,老師說:“其實Na2CO3溶液能使酚酞溶液變紅也是由于溶液中存在OH-”。你認為Na2CO3溶液中存在OH-的原因是______________________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
在一個密閉容器中放入M、N、Q、P四種物質,在一定條件下發生化學反應,一段時間后,測得有關數據如下表,則關于此反應認識不正確的是 ( )
| 物 質 | M | N | Q | P |
| 反應前質量(g) | 18 | 1 | 2 | 32 |
| 反應后質量(g) | X | 26 | 2 | 12 |
A.該變化的基本反應類型是分解反應 B.反應后物質M的質量為l3g
C.反應中N、P的質量比為5:4 D.物質Q可能是該反應的催化劑
查看答案和解析>>
科目:初中化學 來源: 題型:
實驗室有一瓶濃鹽酸,瓶上標簽的部分內容如下圖所示,請你根據標簽上提供的數據解答下列問題:

(1)為了證明該瓶鹽酸顯酸性,你可以采取的做法是 。(簡單描述即可)
(2)取出200g該濃鹽酸,稀釋成18.25%的稀鹽酸,需要加入水的質量為 g。
(3)現用剛配好的100g18.25%的鹽酸與足量的鋅粒完全反應,理論上可以生成氫氣的質量是多少?(反應化學方程式:Zn+2HCl= ZnCl2+H2↑)
查看答案和解析>>
科目:初中化學 來源: 題型:
下列關于氧氣的說法中正確的是( )
A.氧氣在低溫、高壓的條件下可以轉變為液體或固體
B.氧氣是植物光合作用的重要來源
C.氧氣的化學性質比較活潑,是可燃物
D.因為氧氣與氮氣的密度不同,所以工業上用分離液態空氣法制取氧氣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com