
 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
 氫氧化銅固體受熱分解能得到兩種氧化物,一種為固體,另一種是無色液體.某化學活動小組為確定這種固體產物是什么,進行了如下探究活動.
氫氧化銅固體受熱分解能得到兩種氧化物,一種為固體,另一種是無色液體.某化學活動小組為確定這種固體產物是什么,進行了如下探究活動.查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
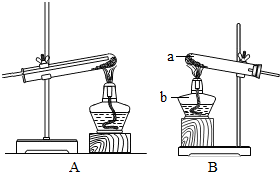
查看答案和解析>>
科目:初中化學 來源:中學學習一本通 化學 九年級下冊 人教課標 題型:013
把含有少量氧化銅、氫氧化銅的鐵粉加入稀硫酸中,加熱充分反應后,發現鐵粉有剩余.將溶液過濾,濾渣中的物質是
A.鐵
B.鐵和銅
C.銅和氧化銅
D.氧化銅和鐵
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com