
【題目】純堿是重要的化工原料 (一)制備探究:如圖是工業生產純堿的主要流程示意圖.
[查閱資料]
①粗鹽水中含有雜質MgCl2、CaCl2;
②常溫下,NH3極易溶于水,CO2能溶于水,
③NaHCO3加熱易分解,Na2CO3加熱不易分解.
(1)寫出除去粗鹽水中MgCl2的化學方程式: .
(2)在工業生產純堿工藝流程中,先“氨化”后“碳酸化”的目的是 , “碳酸化”時,NaCl、NH3、CO2和H2O相互作用析出NaHCO3 , 寫出該反應的化學方程式 .
(3)“碳酸化”后過濾獲得的NH4Cl可用作氮肥,也可先加熱NH4Cl溶液,再加入熟石灰獲得循環使用的物質是;
(4)煅燒制得純堿的化學方程式是 .
(5)(二)成分探究 [提出問題]純堿樣品中含有哪些雜質?
[猜想]
猜想一:可能含有NaHCO3; 猜想二:可能含有NaCl;猜想三:NaHCO3和NaCl
[實驗探究]確定純堿中是否含NaHCO3 . 實驗裝置和主要實驗步驟如下:
①稱量D、E裝置總質量為200.0g,檢查裝置的氣密性,將10.6 g純堿試樣放入錐形瓶中,按上圖組裝儀器,進行如下操作…………,后緩緩鼓入一段時間空氣;
②按一定要求正確操作后,加入足量稀硫酸,待錐形瓶中不再產生氣泡時,再次打開止水夾K1 , 從導管a處再次緩緩鼓入空氣;
③一段時間后再次稱量裝置D、E的總質量為204.84g.
[實驗討論]
步驟①中“如下操作”是指;
(6)裝置B中一定發生的化學反應方程式為:;
(7)裝置B中生成CO2的質量為4.84g,通過計算說明純堿中含NaHCO3(填字母).(寫出計算過程)
A.一定
B.一定不
C.可能
D.無法確定
(8)另取10.6樣品,加入a g 14.6%的鹽酸恰好完全反應,再將所得溶液蒸干后得到固體的質量為W,當W的值滿足條件時,樣品中含有NaCl.
【答案】
(1)MgCl2+2NaOH=Mg(OH)2+2NaCl
(2)有利于溶液吸收二氧化碳;NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
(3)NH3
(4)2NaHCO3=Na2CO3+H2O+CO2↑
(5)打開K1、K2 , 關閉K3
(6)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
(7)A
(8)W>0.234a
【解析】解:(1)除去粗鹽水中MgCl2用的試劑是氫氧化鈉溶液,故該反應的化學方程式為:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;(2)在工業生產純堿工藝流程中,先“氨化”后“碳酸化”的目的是有利于溶液吸收CO2氣體;氯化鈉、氨氣、二氧化碳和水反應生成碳酸氫鈉和氯化銨,反應的化學方程式為:NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;(3)“碳酸化”后過濾獲得的NH4Cl含有氮元素,所以可用作氮肥;氯化銨不穩定受熱易分解或遇到堿放出氨氣,也可先加熱NH4Cl溶液,再加入熟石灰獲得循環使用的物質是NH3(或氨氣);(4)因為碳酸氫鈉受熱分解生成碳酸鈉、水和二氧化碳,故反應的化學方程式為:2NaHCO3 ![]() Na2CO3+H2O+CO2↑;【猜想三】純堿樣品中還可能含有NaHCO3和NaCl的混合物;(5)加入樣品前還應檢查裝置氣密性;反應結束后打開止水夾K1 , 緩緩鼓入空氣的目的是將生成的二氧化碳全部送到D中;故步驟①中“如下操作”是指打開K1、K2 , 關閉K3;(6)裝置B中碳酸鈉和硫酸反應生成硫酸鈉、水和二氧化碳,故一定發生的化學反應方程式為:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;(7)根據D、E增加的質量為二氧化碳的質量,裝置B中生成CO2的質量=204.84g﹣200.0g=4.84g; 假設10.6g樣品全為碳酸鈉,生成二氧化碳的質量為x.
Na2CO3+H2O+CO2↑;【猜想三】純堿樣品中還可能含有NaHCO3和NaCl的混合物;(5)加入樣品前還應檢查裝置氣密性;反應結束后打開止水夾K1 , 緩緩鼓入空氣的目的是將生成的二氧化碳全部送到D中;故步驟①中“如下操作”是指打開K1、K2 , 關閉K3;(6)裝置B中碳酸鈉和硫酸反應生成硫酸鈉、水和二氧化碳,故一定發生的化學反應方程式為:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;(7)根據D、E增加的質量為二氧化碳的質量,裝置B中生成CO2的質量=204.84g﹣200.0g=4.84g; 假設10.6g樣品全為碳酸鈉,生成二氧化碳的質量為x.
Na2CO3+H2SO4=Na2SO4+H2O+ | CO2↑ |
106 | 44 |
10.6g | x |
則 ![]() ,解得x=4.4g.
,解得x=4.4g.
則4.4g<4.84g,所以樣品中含有碳酸氫鈉;(8)根據碳酸鈉和鹽酸反應生成氯化鈉、水和二氧化碳,假設全部是碳酸鈉求出增加的質量.
Na2CO3+ | 2HCl= | 2NaCl+H2O+CO2↑ |
73 | 117 | |
ag×14.6% | W |
則 ![]() ,解得W=0.234ag.
,解得W=0.234ag.
所以當W的值滿足條件W>0.234ag時,樣品中含有NaCl;
所以答案是:(1)MgCl2+2NaOH=Mg(OH)2+2NaCl.(2)有利于溶液吸收二氧化碳,NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl.(3)NH3 , (4)2NaHCO3 ![]() Na2CO3+H2O+CO2↑;(5)打開K1、K2 , 關閉K3;(6)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑(7)A;解題略;(8)W>0.234a.
Na2CO3+H2O+CO2↑;(5)打開K1、K2 , 關閉K3;(6)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑(7)A;解題略;(8)W>0.234a.
【考點精析】解答此題的關鍵在于理解書寫化學方程式、文字表達式、電離方程式的相關知識,掌握注意:a、配平 b、條件 c、箭號.


 開心蛙狀元作業系列答案
開心蛙狀元作業系列答案 課時掌控隨堂練習系列答案
課時掌控隨堂練習系列答案 一課一練一本通系列答案
一課一練一本通系列答案科目:初中化學 來源: 題型:
【題目】如圖1是實驗室常用的裝置,請根據裝置回答下列問題: 
(1)寫出圖1中標示儀器的名稱是①② .
(2)實驗室若要制取干燥的氧氣,應選擇裝置的連接順序為(填字 母) , 有關反應的化學方程式為;
(3)A裝置也能用于制取二氧化碳,若將二氧化碳通入E,實驗現象是;
(4)圖2裝置也可以用來收集氣體,若用此裝置收集二氧化碳,則二氧化碳應該從端通入(填“a”或“b”). 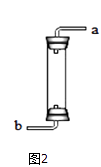
(5)工業上常用塊狀的固體電石與水混合即發生劇烈反應來制得乙炔氣體,乙炔是一種難溶于水,密度比空氣小的氣體.要制取較純凈的乙炔氣體,可選用的發生和收集裝置為 . (填字母編號)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】向Cu(NO3)2、AgNO3的混合溶液中加入一定量的鐵粉,充分反應后過濾,再向濾渣中加入稀鹽酸,發現沒有氣泡產生,則濾渣中一定含有的物質是
A. Fe、Cu B. Cu、Ag C. Cu D. Ag
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列有關實驗方案設計正確的是( )
選項 | 實驗目的 | 實驗方案 |
A | 檢驗NaOH溶液中是否含有Na2CO3 | 加入過量的稀鹽酸,觀察現象 |
B | 鑒別純棉線和羊毛線 | 觀察顏色 |
C | 除去KNO3溶液中的少量Ba(NO3)2 | 加入適量的Na2SO4溶液,過濾 |
D | 除去CO2中含有的少量CO | 點燃 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A、B、C、D、E是初中常見的五種物質,其中 D是黑色固體,且與C在一定條件下反應有紅色物質生成,E的固體俗稱干冰.①、②、③、④的反應類型分別是復分解反應、分解反應、化合反應和置換反應.圖中“一”表示兩端物質間能發生反應,“→”表示物質間的轉化關系,部分反應物、生成物及反應條件已略去.
請回答下列問題:
(1)寫出下列物質的化學式:D , E .
(2)寫出下列反應的化學方程式:
①;
④ .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com