
味精是常用的調味品,它的鮮味來自于其中的主要成分“谷氨酸鈉”(化學式是C5H8NO4Na,易溶于水,與AgNO3不反應),另外還含有NaCl(其他成分不考慮)。請回答下列問題:
(1)稱取5.0g味精配制成50g溶液,量取蒸餾水的量筒規格是 。(填字母)
A.10mL B.50mL C.100mL
(2)下圖是配制過程,正確的操作順序為 。(填序號)
 |
(3)為測定味精中NaCl的質量分數,進行如下實驗:
①向所配制的50g溶液中加入過量的 溶液(填化學式)充分反應。
②然后進行 (填操作名稱)、洗滌、干燥后稱量AgCl固體。
③在其他操作均正確的情況下,若在配制溶液過程中,仰視刻度量取蒸餾水,則所配制溶液的谷氨酸鈉質量分數 (填“偏大”、“偏小”或“無影響”),則測得的樣品中氯化鈉的質量分數 (填“偏大”、“偏小”或“無影響”)。
④經精確測定AgCl沉淀的質量為2.87g,則該味精中NaCl的質量分數為 。(計算結果保留一位小數)
科目:初中化學 來源: 題型:
為測定某含有少量NaCl的純堿晶體(Na2CO3•nH2O)樣品的組成,做了如下實驗:

根據實驗數據進行計算,寫出計算過程。
(1)樣品中含有結晶水的質量是 克。
(2)原混合物中NaC l與純堿晶體(Na2CO3•nH2O)的質量比 。
l與純堿晶體(Na2CO3•nH2O)的質量比 。
(3)化學式Na2CO3• nH2O中n= 。
查看答案和解析>>
科目:初中化學 來源: 題型:
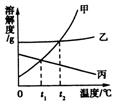
右圖是甲、乙、丙三種物質的溶解度曲線,下列說法正確的是
A.t1℃時,把甲的不飽和溶液變為飽和溶液,溶劑質量一定不變
B.t2℃時,甲、乙兩種物質飽和溶液的溶質質量分數一定相等
C.將t1℃時的甲、乙、丙三種物質的飽和溶液升溫到t2℃,三種溶液的溶
質質量分數大小關系是:甲=乙〉丙
D.若甲中混有少量乙,可采用蒸發結晶的方法提純甲
查看答案和解析>>
科目:初中化學 來源: 題型:
下列從有關實驗得到的結論中,正確的是
A.實驗室用大理石與鹽酸反應制取的CO2通入澄清石灰水而無沉淀生成,可能是因為鹽酸太濃
B.某混合氣體使灼熱的氧化銅變成紅色固體后,再導出的氣體能使澄清石灰水變渾濁,證明原氣體中一定含有一氧化碳
C.含二氧化碳、一氧化碳、氫氣、水蒸氣、氮氣的混合氣體,依次通過石灰水、灼熱的氧化銅、濃硫酸(假定每步反應完全或吸收充分),最后只剩下氮氣
D.點燃某可燃物,在火焰上罩一個冷而干燥的燒杯,燒杯的內壁有水霧出現,證明可燃物一定是H2
查看答案和解析>>
科目:初中化學 來源: 題型:
微粒是構成化學物質的基礎,下列對微粒的描述正確的是( )
|
| A. | 僅有碳原子構成的物質屬于純凈物 |
|
| B. | 原子中一定含有質子、中子、電子 |
|
| C. | NaCl是由離子構成的,所以HCl也是有離子構成的 |
|
| D. | Cl﹣的離子結構示意圖為 |
查看答案和解析>>
科目:初中化學 來源: 題型:
下列是實驗室常用的幾種儀器,請回答有關問題.
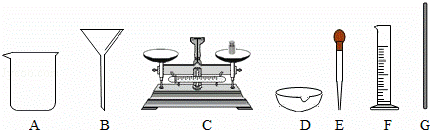
粗鹽中含少量Ca2+、Mg2+、SO42﹣和泥沙等雜質,粗鹽精制的過程中涉及常規操作步驟有:
(1)①加水溶解;②依次加入過量的BaCl2、NaOH、Na2CO3溶液;③ ;④加入適量的 ;⑤ 、冷卻結晶(填試劑或操作名稱).
(2)過濾用到的玻璃儀器有: 、 、 .
(3)蒸發時 (填“能”或“不能”)將溶液直接蒸干.
(4)配置1000g5.85%的NaCl溶液,需 gNaCl;在準確稱取固體后,用量筒量取水時,仰視讀數,則所配置溶液溶質質量分時 (填“偏高”或“偏低”)
查看答案和解析>>
科目:初中化學 來源: 題型:
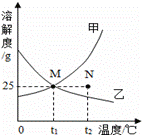
如圖為 甲、乙兩種固體物質的溶解度曲線。下列說法錯誤的是 ( )
甲、乙兩種固體物質的溶解度曲線。下列說法錯誤的是 ( )
A.甲物質的溶解度隨溫度的升高而增大
B.在t1℃時,甲、乙兩物質的溶解度相等
C.在t2℃時,N點表示甲物質的不飽和溶液
D.在t1℃時,100g乙物質的飽和溶液中溶質的質量是25g
 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com