
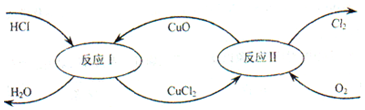
分析 (1)反應I中,氧化銅和稀鹽酸反應生成氯化銅和水;
(2)反應Ⅱ中,反應物和生成物都是一種單質和一種化合物,屬于置換反應;
(3)根據反應的化學方程式及其提供的數據可以進行相關方面的計算.
解答 解:(1)反應I中,氧化銅和稀鹽酸反應生成氯化銅和水,反應的化學方程式為:2HCl+CuO═CuCl2+H2O.
故填:2HCl+CuO═CuCl2+H2O.
(2)反應Ⅱ中,反應物和生成物都是一種單質和一種化合物,屬于置換反應.
故填:置換反應.
(3)設需要氯氣質量為x,
2Na+Cl2$\frac{\underline{\;點燃\;}}{\;}$2NaCl,
46 71
4.6g x
$\frac{46}{4.6g}$=$\frac{71}{x}$,
x=7.1g,
故填:7.1.
點評 本題主要考查物質的性質,解答時要根據各種物質的性質,結合各方面條件進行分析、判斷,從而得出正確的結論.


科目:初中化學 來源: 題型:選擇題
| 物質(括號內為雜質) | 實驗方案 | |
| A | 氮氣(氧氣) | 通過足量灼熱銅網 |
| B | 氯化鈣溶液(鹽酸) | 加入足量碳酸鈣粉末,過濾 |
| C | 鐵粉(銅粉) | 加入足量稀鹽酸,過濾,洗滌,干燥 |
| D | 氧化銅(木炭粉) | 在空氣中充分灼燒 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
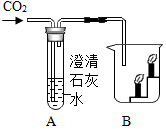
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 從溶解度曲線可以知道一定溫度下某種物質的溶解度 | |
| B. | 從金屬活動性順序表可以知道金屬活潑性的強弱 | |
| C. | 一定溫度下,向溶液中加入溶質都會使其溶質質量分數增大 | |
| D. | 配平化學方程式的依據是質量守恒定律 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com