
【題目】某興趣小組欲探究Fe、Cu、Ag、R四種金屬的活動性順序(R為未知金屬),進行了如下實驗。
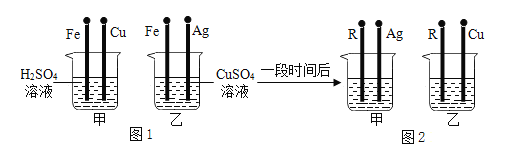
(1)如圖1,將四根金屬絲同時插入燒杯中,則甲中的現象是_____;乙中發生反應的化學方程式為_____;
(2)一段時間后,將燒杯中四根金屬絲依次替換為R、Ag、R、Cu,如圖2所示。
①若甲中出現氣泡,乙中無明顯現象,則燒杯乙中的溶質為_____(填化學式)。可得出Fe、Cu、Ag、R的活動性順序由強到弱為_____;
②若甲中無明顯現象,乙中R表面出現紅色固體,則不能推出的結論是_____(填序號)。
A R>Ag B R>Cu C R<Fe D R<H
【答案】鐵絲表面有氣體產生,溶液由無色變為淺綠色 Fe+CuSO4=FeSO4+Cu FeSO4 Fe>R>Cu>Ag D
【解析】
(1)如圖A所示,將四根金屬絲同時插入燒杯中,則甲中為鐵和硫酸反應生成氫氣,現象是鐵絲表面有氣體產生,溶液由無色變為淺綠色,乙中鐵和硫酸銅反應,反應的化學方程式是:Fe+CuSO4=FeSO4+Cu;
故填:鐵絲表面有氣體產生,溶液由無色變為淺綠色;Fe+CuSO4=FeSO4+Cu;
(2)①根據R替換鐵絲后與硫酸反應有氣泡產生,說明R的活動性大于氫;當把R置于乙裝置中無明顯現象說明乙中溶液中原來的溶質硫酸銅已與鐵絲全部反應(根據前面判斷R的活動性大于氫,如果乙中還有硫酸銅溶質,那么R將會置換出硫酸銅溶液中的銅,會有現象),所以乙中的溶質是硫酸亞鐵,從而說明R的活動性比鐵弱,由此推斷可得,四種金屬的活動性由強到弱的順序為:Fe、R、Cu、Ag;故填:FeSO4;Fe>R>Cu>Ag;
②根據“若甲中無明顯現象,乙中R表面出現紅色固體”,則可推測的結論為:“甲中R”與硫酸溶液可能反應,但較慢,不易察覺,也可能不反應,故不能推測出R<H,由于R不能置換甲中硫酸亞鐵中的鐵,故可推知R<Fe;“乙中R”與硫酸銅溶液反應,則可推測R>Cu和R>Ag.故答案為:D。


科目:初中化學 來源: 題型:
【題目】如圖所示的四個圖象,能正確反映對應變化關系的是( )
A.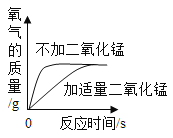 等量的兩份過氧化氫溶液,一份中加入二氧化錳
等量的兩份過氧化氫溶液,一份中加入二氧化錳
B.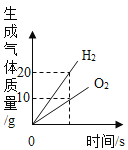 水通電產生氫氣和氧氣的質量關系
水通電產生氫氣和氧氣的質量關系
C.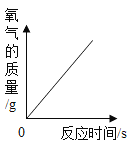 加熱一定質量的氯酸鉀和二氧化錳的混合物,氧氣的質量變化情況
加熱一定質量的氯酸鉀和二氧化錳的混合物,氧氣的質量變化情況
D.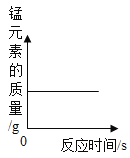 加熱高錳酸鉀,錳元素的質量的變化情況
加熱高錳酸鉀,錳元素的質量的變化情況
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】小王用圖A所示裝置對二氧化碳的滅火實驗進行探究,觀察到的現象是_____。實驗的結論是_____
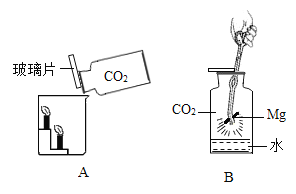
(提出問題)二氧化碳能否支持燃燒?
(猜想假設)鎂能在二氧化碳中燃燒。
(查閱資料)①氧化鎂、氫氧化鎂均是白色難溶于水的固體。
②MgO+2HCl=MgCl2+H2O
③MgCl2+2NaOH=Mg(OH)2↓+2NaCl
(實驗探究)①圖中鎂帶劇烈燃燒,冒白煙,有黑色固體生成,并放出大量的熱。
②為檢驗生成物的成分,做如下實驗。
實驗步驟 | 實驗現象 | 實驗結論和化學方程式 |
向放有生成物的廣口瓶中加入過量稀鹽酸,充分反應后過濾,在濾紙上留有黑色固體 | ||
Ⅰ:將黑色固體收集、洗滌、干燥后,點燃,在火焰上方罩一個蘸有澄清石灰水的燒杯 | a:黑色固體燃燒,燒杯內壁出現白色渾濁 | b:黑色固體是_____;反應的化學方程式是: _____、_____ |
Ⅱ:取少量濾液于試管中,逐滴加入氫氧化鈉溶液 | c:開始_____,后有白色沉淀產生 | d:白煙的成分是_____ |
(反思提高)實驗室中某些活潑金屬引起的著火,不能用二氧化碳滅火,應用細沙滅火。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖是a、b,c三種固體物質的溶解度曲線圖,請回答問題:
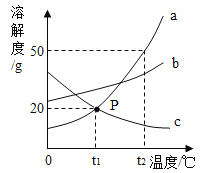
(1)圖中P點所表示的意義是_______
(2)將t2℃三種物質的飽和溶液降溫至t1℃時,溶質的質量分數由大到小的順序是_________
(3)當a物質中混有少量b.c兩種物質時,采用______的方法可以提純a
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】元素周期表是學習和研究化學的重要工具,請據圖回答下列問題。
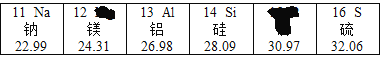
(1)圖中硅元素右側一格已被墨水沾黑,該方格中原子的元素符號是_____,該原子核內的中子數是_____;
(2)第16號元素位于元素周期表中的第_____周期;
(3)寫出與氖原子核外電子排布相同的一個陽離子的符號_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】明礬可用于凈水,是因為明礬溶于水生成的膠狀物可以_____懸浮于水中的雜質,使水澄清;新型自來水消毒劑可由下列反應制取:![]() ,則X的化學式為_____;
,則X的化學式為_____;![]() 中氯元素的化合價為_____。
中氯元素的化合價為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學課上,“魅力小組”的四位同學在老師的指導下做制取氫氧化鈉溶液的實驗。他們向盛有澄清石灰水的燒杯中加入一定量的碳酸鈉溶液,觀察到生成白色沉淀,過濾后得到無色溶液。向無色溶液中加入稀鹽酸,可能發生反應的化學方程式為_____。四位同學對反應后得到的無色溶液中的溶質成分進行了如下探究:
猜想:小紅:溶質只有NaOH;
小花:溶質有NaOH、Ca(OH)2、Na2CO3;
小剛:溶質有NaOH、Na2CO3;
小強:溶質有_____。
交流討論:經過討論,大家一直認為_____的猜想不正確,理由是_____。
于是他們設計了如下實驗方案,繼續探究:
進行實驗:
實驗步驟 | 實驗現象 | 實驗結論 |
取少量無色溶液于試管中,滴加足量稀鹽酸 | _____ | 小剛的猜想不正確 |
取少量無色溶液于試管中,滴加足量Na2CO3溶液 | _____ | 小強的猜想正確 |
反思與評價:在上述實驗過程中,要證明小強的猜想正確,還可選擇另外一種不同類別的物質_____(填化學式)進行證明。
總結與提升:通過上述實驗,四位同學總結出:
(1)反應后溶液中溶質成分中一定有_____;
(2)當設計實驗證明反應后溶液中溶質成分時,只需證明可能存在的物質即可。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】寫出下列化學用語的符號或名稱:
(1)氯原子______
(2)3個氫分子______
(3)氫氧根離子______
(4)HNO3______
(5)標出氧化銅中銅元素化合價______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】家里蒸饅頭的純堿中含有少量的氯化鈉。為測定該純堿中碳酸鈉的質量分數:取該樣品11g,全部溶液在100g水中,再逐漸滴加氯化鈣溶液,反應的情況如圖所示,A點時,過濾,得到濾液242g。(反應方程式:Na2CO3+CaCl2=CaCO3↓+2NaCl)
計算:

(1)反應生成沉淀的質量m為多少?
(2)樣品中碳酸鈉的質量分數。
(3)濾液中溶質的質量分數。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com