
生產燒堿的工廠,常用便宜的原料純堿和熟石灰制得成品。為模擬該生產過程,同學們取20gNa2CO3溶液與一定質量的飽和石灰水混合,恰好完全反應,得到4g白色沉淀。
求(1) Na2CO3中Na、C、O各元素的質量比 (2分)。
(2) Na2CO3中Na、C、O各原子個數比 (2分)。
(3)Na2CO3溶液中溶質的質量分數。(8分)
(1)23﹕6﹕24 (2)2﹕1﹕3 (3)21.2%
【解析】
試題分析:首先根據題意正確寫出化學方程式并找出其中一純凈物的質量,然后把這一純凈物的質量代入化學方程式計算有關的量。根據題意不難得出,碳酸鈉和氫氧化鈣反應生成的碳酸鈣沉淀的質量為4g,因此根據碳酸鈣的質量就可求出20g碳酸鈉溶液中碳酸鈉的質量,在應用溶質質量分數的計算公式即可得出答案。
(3)設20g碳酸鈉溶液中碳酸鈉的質量為x
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 100
x 4g
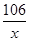 =
= 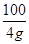
x=4.24g
碳酸鈉溶液中溶質的質量分數為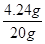 ×100%=21.2%
×100%=21.2%
答:碳酸鈉溶液中溶質的質量分數為21.2%
考點:根據化學式的計算;根據化學反應方程式的計算


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源:本溪 題型:問答題
查看答案和解析>>
科目:初中化學 來源:2011年湖南省邵陽十中中考化學模擬試卷(三)(解析版) 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com