
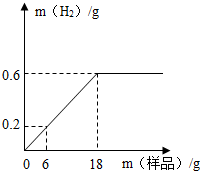
 為測定某鐵粉樣品(含少量木炭粉)中鐵的含量,往盛有219g稀鹽酸的燒杯中不斷加入鐵粉樣品,測得生成氫氣質量與所加鐵粉樣品質量的關系如下圖所示.
為測定某鐵粉樣品(含少量木炭粉)中鐵的含量,往盛有219g稀鹽酸的燒杯中不斷加入鐵粉樣品,測得生成氫氣質量與所加鐵粉樣品質量的關系如下圖所示.分析 (1)從圖象可直接讀出最終生成氫氣的質量;
(2)依據圖象可知6g樣品生成的氫氣質量是0.2g;據此依據方程式的有關計算解答即可;
(3)利用氫氣的質量可求出反應的鐵和鹽酸的質量,而后根據問題計算即可解答.
解答 解:(1)由圖象可知最終生成氫氣的質量是0.6g;
(2)依據圖象可知18g樣品生成的氫氣質量是0.6g;
設18g樣品中鐵的質量是x,反應的氯化氫的質量是y
Fe+2HCl═FeCl2+H2↑
56 73 2
x y 0.6g
$\frac{56}{x}=\frac{2}{0.6g}$,$\frac{73}{y}=\frac{2}{0.6g}$
x=16.8g y=21.9g
則18g樣品中的鐵的質量16.8g.
(3)故稀鹽酸的溶質質量分數$\frac{21.9g}{219g}$×100%=10%
故答案為:(1)0.6;(2)16.8;(3)稀硫酸的溶質質量分數是10%;
點評 解答此類問題的根本點在于對反應圖象的曲線進行分析,曲線的折點表示此時恰好完全反應.


 能考試期末沖刺卷系列答案
能考試期末沖刺卷系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 消化藥片所含物質能中和胃里過多的胃酸,某種消化藥片的標簽如圖.醫生給某胃酸過多的患者開出此藥的處方為每日三次,每次兩片.試計算此患者按處方服用該藥一天,理論上可中和多少克胃酸?
消化藥片所含物質能中和胃里過多的胃酸,某種消化藥片的標簽如圖.醫生給某胃酸過多的患者開出此藥的處方為每日三次,每次兩片.試計算此患者按處方服用該藥一天,理論上可中和多少克胃酸?查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 待鑒別物質 | 鑒別試劑 | |
| A | 碳酸鈉溶液和氫氧化鈉溶液 | 酚酞試液 |
| B | 稀硫酸和稀鹽酸 | 氯化鋇溶液 |
| C | 鐵和銅 | 稀硫酸 |
| D | 食鹽和碳酸鈉 | 鹽酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 陽離子一定帶有正電荷,陰離子一定帶負電,中子不帶電 | |
| B. | 一切原子的原子核都是由質子、中子構成的 | |
| C. | 分子、原子、離子都能直接構成物質 | |
| D. | 最外層電子數為8的粒子不一定是稀有氣體元素的原子 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com