寫出下列化學方程式:
(1)純堿制燒堿______
(2)鹽酸除水垢(成分為氫氧化鎂和碳酸鈣)______
(3)硫酸除鐵銹______
(4)小蘇打遇鹽酸______.
解:(1)工業制燒堿是用氫氧化鈣和碳酸鈉的反應來制燒堿,氫氧化鈣和碳酸鈉反應生成碳酸鈣沉淀和氫氧化鈉,故答案為:Ca(OH)2+Na2CO3=2NaOH+CaCO3↓,
(2)氫離子會與氫氧根離子和碳酸根離子反應生成水和二氧化碳,鹽酸和碳酸鈣反應生成氯化鈣、水和二氧化碳,鹽酸和氫氧化鎂反應生成氯化鎂和水,
故答案為:CaCO3+2HCl=CaCl2+H2O+CO2↑、Mg(OH)2+2HCl=MgCl2+2H2O,
(3)鐵銹的主要成分是氧化鐵,鹽酸和氧化鐵反應生成氯化鐵和水,故答案為:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,
(4)小蘇打主要成分是碳酸氫鈉,碳酸氫鈉和鹽酸反應生成氯化鈉、水和二氧化碳,故答案為:NaHCO3+HCl=NaCl+H2O+CO2↑,
分析:(1)根據工業制燒堿是用熟石灰和碳酸鈉的反應來制燒堿進行分析,
(2)根據氫離子會與氫氧根離子和碳酸根離子反應進行分析,
(3)根據酸會與金屬氧化物反應生成鹽和水來判斷,
(4)根據氫離子和碳酸氫根離子會生成水和二氧化碳進行分析.
點評:在解此類題時,首先分析應用的原理,然后是寫對化學式,注意檢查方程式的細節要求.



 閱讀快車系列答案
閱讀快車系列答案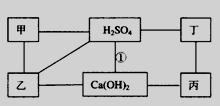 24、下圖中每條連線表示兩端的物質可以發生化學反應,甲、乙、丙、丁分別為Mg、BaCl2、Na2CO3、HCl中的一種.
24、下圖中每條連線表示兩端的物質可以發生化學反應,甲、乙、丙、丁分別為Mg、BaCl2、Na2CO3、HCl中的一種.